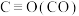名校
解题方法
1 . 有机化合物Ⅰ为一种杀菌抗炎药的主要成分,其中一种合成路线如图所示:
(1)D的分子式为_______ ;E的化学名称为_______ 。
(2)设计A→B、B→C的目的分别是_______ 、_______ 。
(3)写出F→G反应的化学方程式:_______ ;H→I的反应类型为_______ 。
(4)H的结构简式为_______ ;符合下列条件H的同分异构体有_______ 种。 的合成路线
的合成路线_______ (无机试剂任选)。

Ⅰ. +RCl
+RCl
 +HCl;
+HCl;
定位取代基 | 烷基 | 溴原子 | 羟基 | 烷氧基 | 氨基 | 硝基 | 磺酸基 | 羧基 |
定位效应 | 邻位、对位 | 间位 | ||||||
Ⅲ.
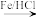
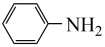 。
。
(1)D的分子式为
(2)设计A→B、B→C的目的分别是
(3)写出F→G反应的化学方程式:
(4)H的结构简式为
①分子中存在 ;②
;②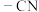 直接连在苯环上;③在核磁共振氢谱中有4组峰,面积比为3∶2∶2∶2。
直接连在苯环上;③在核磁共振氢谱中有4组峰,面积比为3∶2∶2∶2。
 的合成路线
的合成路线
您最近一年使用:0次
昨日更新
|
32次组卷
|
3卷引用:黑龙江省大庆市让胡路区大庆中学2024届高三下学期5月期中化学试题
名校
2 . I.请根据化学能和热能、电能相关的知识,问答下列问题:
(1)下列变化中,属于放热反应的是______ (填序号)。
①液态水汽化
②Ba(OH)2•8H2O与固体NH4Cl混合
③浓H2SO4稀释
④C+H2O(g) CO+H2
CO+H2
⑤生石灰跟水反应
⑥碳酸钠粉末滴少量水
(2)Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:______ 。
(3)已知:
CO(g)+2H2(g)=CH3OH(g) △H1=-90.8kJ•mol-1
2H2(g)+O2(g)=2H2O(1)△H2=-571.6kJ•mol-1
H2O(g)=H2(g)+ O2(g) ΔH3=+241.8kJ•mol-1
O2(g) ΔH3=+241.8kJ•mol-1
根据上述反应CH3OH(g)+O2(g)=CO(g)+2H2O(g) △H=______ kJ•mol-1。
(4)某实验小组设计用50mL0.50mol/L盐酸跟50mL0.55mol/LNaOH溶液进行中和反应,测得的中和热为△H1。若用等浓度的醋酸代替盐酸,测得的中和热为△H2;若用浓硫酸代替盐酸,测得的中和热为△H3,下列说法正确的是______ 。
(5)某化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示。______ (填“能”或“不能”)确定三种物质A2(g)、B2(g)、AB(g)中,最稳定的是AB(g)。
②根据图可知A2(g)和B2(g)生成1molAB(g)的焓变△H为______ kJ•mol-1。
II.为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如图:______ (填离子或分子的化学式)。丙装置中负极反应式为______ 。
(7)当甲装置导线中转移0.3mol电子时,正极生成气体______ L(标准状况下);假设开始时乙装置中两电极质量相等,导线中转移0.3mol电子时,两电极质量相差______ g。
(8)科学家制造出了一种使用固体电解质的燃料电池,其效率很高,可用于航天航空。如图所示装置中,以稀土金属材料为惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导O2-。则d电极上的电极反应式为______ 。
(1)下列变化中,属于放热反应的是
①液态水汽化
②Ba(OH)2•8H2O与固体NH4Cl混合
③浓H2SO4稀释
④C+H2O(g)
 CO+H2
CO+H2⑤生石灰跟水反应
⑥碳酸钠粉末滴少量水
(2)Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:
(3)已知:
CO(g)+2H2(g)=CH3OH(g) △H1=-90.8kJ•mol-1
2H2(g)+O2(g)=2H2O(1)△H2=-571.6kJ•mol-1
H2O(g)=H2(g)+
 O2(g) ΔH3=+241.8kJ•mol-1
O2(g) ΔH3=+241.8kJ•mol-1根据上述反应CH3OH(g)+O2(g)=CO(g)+2H2O(g) △H=
(4)某实验小组设计用50mL0.50mol/L盐酸跟50mL0.55mol/LNaOH溶液进行中和反应,测得的中和热为△H1。若用等浓度的醋酸代替盐酸,测得的中和热为△H2;若用浓硫酸代替盐酸,测得的中和热为△H3,下列说法正确的是
| A.△H1>△H2>△H3 | B.△H3>△H1>△H2 |
| C.△H2>△H1>△H3 | D.△H1=△H2>△H3 |
(5)某化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示。

②根据图可知A2(g)和B2(g)生成1molAB(g)的焓变△H为
II.为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如图:


(7)当甲装置导线中转移0.3mol电子时,正极生成气体
(8)科学家制造出了一种使用固体电解质的燃料电池,其效率很高,可用于航天航空。如图所示装置中,以稀土金属材料为惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导O2-。则d电极上的电极反应式为

您最近一年使用:0次
名校
解题方法
3 . 环己烯是有机合成的一种重要的化工原料。醇脱水是合成烯烃的常用方法,某实验小组以环己醇合成环己烯的制备流程如下:
Ⅰ.环己烯的制备与提纯
(1)操作1的装置如图所示。(加热和夹持装置已略去)
①A处所选仪器为___________ 。
A.蛇形冷凝管 B.球形冷凝管 C.直形冷凝管
②烧瓶B中进行的反应也可以用浓硫酸做催化剂,请写出在浓硫酸催化下制备环己烯的化学反应方程式:___________ 。该实验在选择催化剂时,选用 而不用浓硫酸的原因为
而不用浓硫酸的原因为___________ 。(写出一条合理即可)
③该实验在制备环己烯时,可能会生成的副产物为___________ 。(写出一个即可)
④操作1中装置韦氏分馏柱的作用为___________ 。
(2)操作2的名称为___________ 。
(3)操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和碎瓷片,___________ (填序号);弃去前馏分,收集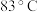 的馏分,当蒸馏结束后
的馏分,当蒸馏结束后___________ (填序号)。
A. 先通冷凝水,再加热 B. 先加热,再通冷凝水
C. 先撤掉酒精灯,再关闭冷凝水 D. 先关闭冷凝水,再撤掉酒精灯
(4)饱和食盐水的作用___________。
Ⅱ.环己烯的性质及含量的测定
(5)实验中,参加反应的环己醇的质量为 ,最终通过操作3蒸馏得到纯净环己烯为
,最终通过操作3蒸馏得到纯净环己烯为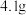 。本实验制得的环己烯的产率为
。本实验制得的环己烯的产率为___________ 。(结果精确至1%)

Ⅰ.环己烯的制备与提纯
(1)操作1的装置如图所示。(加热和夹持装置已略去)

①A处所选仪器为
A.蛇形冷凝管 B.球形冷凝管 C.直形冷凝管
②烧瓶B中进行的反应也可以用浓硫酸做催化剂,请写出在浓硫酸催化下制备环己烯的化学反应方程式:
 而不用浓硫酸的原因为
而不用浓硫酸的原因为③该实验在制备环己烯时,可能会生成的副产物为
④操作1中装置韦氏分馏柱的作用为
(2)操作2的名称为
(3)操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和碎瓷片,
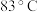 的馏分,当蒸馏结束后
的馏分,当蒸馏结束后A. 先通冷凝水,再加热 B. 先加热,再通冷凝水
C. 先撤掉酒精灯,再关闭冷凝水 D. 先关闭冷凝水,再撤掉酒精灯
(4)饱和食盐水的作用___________。
| A.增大水层密度,加速有机相与水相分层 |
| B.降低环己烯在水中的溶解度,便于分离 |
| C.洗涤,除去环己烯中的杂质 |
| D.增大环己烯在水中的溶解度,便于分离 |
Ⅱ.环己烯的性质及含量的测定
(5)实验中,参加反应的环己醇的质量为
 ,最终通过操作3蒸馏得到纯净环己烯为
,最终通过操作3蒸馏得到纯净环己烯为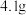 。本实验制得的环己烯的产率为
。本实验制得的环己烯的产率为
您最近一年使用:0次
名校
4 . 按要求填空
(1)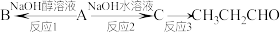
①反应1的反应类型___________ 。
②物质B的名称___________ 。
③反应3的条件___________ 。
(2)某有机物结构如下图所示,分子中处于同一直线的碳原子最多有___________ 个, 该烃与氢气反应最多消耗
该烃与氢气反应最多消耗___________ mol氢气。 ,若A的一种同分异构体B只能由一种烯烃C加氢得到,且核磁共振氢谱只有两组峰,存在顺反异构体。写出C的反式异构体结构简式:
,若A的一种同分异构体B只能由一种烯烃C加氢得到,且核磁共振氢谱只有两组峰,存在顺反异构体。写出C的反式异构体结构简式:___________ 。
(4)分子式为 且属于芳香族化合物的同分异构体有
且属于芳香族化合物的同分异构体有___________ 种。
(5)BN晶体的晶胞如下图,已知B原子半径为 ,N原子半径为
,N原子半径为 ,BN属于
,BN属于___________ 晶体,试表示BN晶体的空间利用率计算式___________ 。
(1)
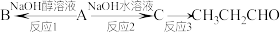
①反应1的反应类型
②物质B的名称
③反应3的条件
(2)某有机物结构如下图所示,分子中处于同一直线的碳原子最多有
 该烃与氢气反应最多消耗
该烃与氢气反应最多消耗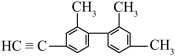
 ,若A的一种同分异构体B只能由一种烯烃C加氢得到,且核磁共振氢谱只有两组峰,存在顺反异构体。写出C的反式异构体结构简式:
,若A的一种同分异构体B只能由一种烯烃C加氢得到,且核磁共振氢谱只有两组峰,存在顺反异构体。写出C的反式异构体结构简式:(4)分子式为
 且属于芳香族化合物的同分异构体有
且属于芳香族化合物的同分异构体有(5)BN晶体的晶胞如下图,已知B原子半径为
 ,N原子半径为
,N原子半径为 ,BN属于
,BN属于
您最近一年使用:0次
名校
5 . 下列说法正确的是

| A.由气态氨气转化为固态铵盐的过程称为氮的固定 |
| B.用CO2和饱和NaHCO3溶液,使用如图装置可实现喷泉实验 |
| C.密闭容器中充入1molN2和3molH2,充分反应后生成2molNH3 |
| D.燃煤中加入生石灰可以减少SO2的排放 |
您最近一年使用:0次
名校
6 . 下表为元素周期表的一部分,请用化学用语回答下列问题:______ 。
(2)写出③的最高价氧化物的水化物的电子式______ ;实验室中盛放其水溶液的试剂瓶不能用玻璃塞,请用化学方程式说明原因______ 。
(3)②的最简单氢化物与④的单质混合,在光照条件下发生反应生成多种氯代烃,该反应类型为______ ;请写出生成CH3Cl的化学方程______ 。
(4)为确定①与②形成的化合物X的分子式,取一定量的X充分燃烧,将产物依次通过浓硫酸、浓碱液,实验结束后,称得浓硫酸增重7.2g,浓碱液增重15.4g。则X的分子式为______ ;X的同分异构体个数为______ ;请写出其中含有3个甲基(-CH3)的同分异构体的结构简式____________ 。
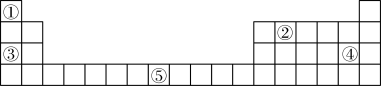
(2)写出③的最高价氧化物的水化物的电子式
(3)②的最简单氢化物与④的单质混合,在光照条件下发生反应生成多种氯代烃,该反应类型为
(4)为确定①与②形成的化合物X的分子式,取一定量的X充分燃烧,将产物依次通过浓硫酸、浓碱液,实验结束后,称得浓硫酸增重7.2g,浓碱液增重15.4g。则X的分子式为
您最近一年使用:0次
名校
7 . 2023年杭州亚运会主火炬使用了零碳甲醇燃料,其制备共消耗了16万吨CO2。该甲醇的制备反应及副反应如下:
ⅰ. (放热反应)
(放热反应)
ⅱ. (吸热反应)
(吸热反应)
(1)键能是指断裂1mol化学键生成气态原子吸收的热量,几种化学键的键能如表所示。
若CO2与足量H2发生反应转化为1molCO和水蒸气时吸收热量为42kJ,则
______ 。
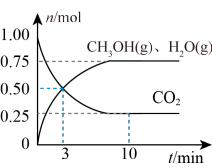
(2)在某温度下,向体积为1L的恒容密闭容器中充入3molH2和1molCO2,发生反应ⅰ,其中CO2(g)、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化如下图所示:______ 。
②下列措施一定可以提高甲醇生成速率的是______ 。
A.降低反应温度 B.缩小容器的容积
C.将产生的水蒸气及时移走 D.使用合适的催化剂
③下列选项能作为判断该反应达到平衡状态的依据的是______ 。
A.容器中CO2的体积分数不变
B.容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中混合气体的平均相对分子质量不变
E.单位时间内,断裂3molH-H键,同时生成2molH-O键
(3)以甲醇为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池。下图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。______ 极,B极的电极反应式为____________ 。
ⅰ.
 (放热反应)
(放热反应)ⅱ.
 (吸热反应)
(吸热反应)(1)键能是指断裂1mol化学键生成气态原子吸收的热量,几种化学键的键能如表所示。
化学键 | H-O | C=O(CO2) | H-H |
|
键能/ | 462.8 | 803.0 | 436.0 | x |

(2)在某温度下,向体积为1L的恒容密闭容器中充入3molH2和1molCO2,发生反应ⅰ,其中CO2(g)、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化如下图所示:
②下列措施一定可以提高甲醇生成速率的是
A.降低反应温度 B.缩小容器的容积
C.将产生的水蒸气及时移走 D.使用合适的催化剂
③下列选项能作为判断该反应达到平衡状态的依据的是
A.容器中CO2的体积分数不变
B.容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中混合气体的平均相对分子质量不变
E.单位时间内,断裂3molH-H键,同时生成2molH-O键
(3)以甲醇为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池。下图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。

您最近一年使用:0次
名校
8 . 按要求完成下列试题:
(1)新戊烷用系统命名法时的名称:____________ 。
(2)写出乙炔和溴水按物质的量之比为1:1反应的化学方程式:____________ 。
(3)工业合成氨的化学方程式:____________ 。
(4)铁和稀硝酸按物质的量之比为1:1反应的离子方程式:____________ 。
(5)分子式为C6H14的烃结构中含有4个甲基,且一氯代物只有两种的结构简式为:____________ 。
(1)新戊烷用系统命名法时的名称:
(2)写出乙炔和溴水按物质的量之比为1:1反应的化学方程式:
(3)工业合成氨的化学方程式:
(4)铁和稀硝酸按物质的量之比为1:1反应的离子方程式:
(5)分子式为C6H14的烃结构中含有4个甲基,且一氯代物只有两种的结构简式为:
您最近一年使用:0次
名校
9 . 以下说法错误的是
| A.苯的邻二氯代物只有一种证明苯没有单双键交替的结构 |
| B.甲苯使高锰酸钾溶液褪色说明苯环对甲基有影响 |
C.CH3CHBrCH2CH3与 的醇溶液共热反应有机产物有2种(不考虑顺反异构) 的醇溶液共热反应有机产物有2种(不考虑顺反异构) |
| D.甲苯在一定条件下发生硝化反应产物只有TNT一种 |
您最近一年使用:0次
名校
解题方法
10 . 化学与生产生活密切相关,以下说法错误的是
| A.蒽、萘属于苯的同系物,二者均为重要的化工原料 |
| B.可利用乙炔在氧气中燃烧时,形成的氧炔焰来焊接或切割金属 |
| C.聚氯乙烯绝缘性好,耐化学腐蚀,可制成电线外面的绝缘材料 |
| D.2,4,6-三硝基甲苯是一种烈性炸药,广泛用于国防、采矿、筑路、水利建设等 |
您最近一年使用:0次