名校
1 . 一种铜的溴化物立方晶胞如图所示。若该晶体密度为 ,化合物式量为M。下列说法中错误的是
,化合物式量为M。下列说法中错误的是
 ,化合物式量为M。下列说法中错误的是
,化合物式量为M。下列说法中错误的是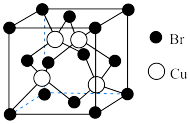
A.晶胞的边长为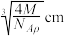 | B.该化合物的化学式为 |
C.基态 原子价层电子排布式为 原子价层电子排布式为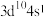 | D.在晶体中与 距离最近且相等的 距离最近且相等的 有12个 有12个 |
您最近一年使用:0次
名校
解题方法
2 . 一定条件下,O2得电子转化为超氧自由基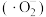 ,并实现如图所示的转化:
,并实现如图所示的转化:
(1)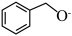 中有
中有___________ 种不同化学环境的氢原子。
(2)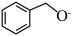 转化为
转化为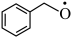 是
是___________ (填“氧化”或“还原”)反应。
(3)写出图示转化总反应的化学方程式:___________ 。
(4)用现代仪器区分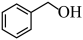 与
与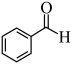 的方法是
的方法是___________ 。
(5)已知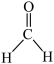 分子中所有原子都在同一平面内,则
分子中所有原子都在同一平面内,则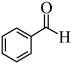 中至多有
中至多有___________ 个原子共平面。
(6)已知10.8g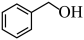 在足量O2中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重
在足量O2中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重___________ g和___________ g。
(7)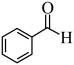 继续氧化产物(C7H6O2)与
继续氧化产物(C7H6O2)与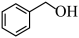 反应的化学方程式:
反应的化学方程式:___________ 。
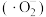 ,并实现如图所示的转化:
,并实现如图所示的转化: 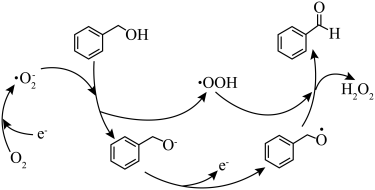
(1)
 中有
中有(2)
 转化为
转化为 是
是(3)写出图示转化总反应的化学方程式:
(4)用现代仪器区分
 与
与 的方法是
的方法是(5)已知
 分子中所有原子都在同一平面内,则
分子中所有原子都在同一平面内,则 中至多有
中至多有(6)已知10.8g
 在足量O2中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重
在足量O2中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重(7)
 继续氧化产物(C7H6O2)与
继续氧化产物(C7H6O2)与 反应的化学方程式:
反应的化学方程式:
您最近一年使用:0次
2024-05-22更新
|
121次组卷
|
3卷引用:山西省运城市三晋卓越联盟2023-2024学年高二下学期期中考试化学试题
名校
解题方法
3 . 已知有下列类物质(黑点表示碳原子,氢原子已省略)。下列说法错误的是
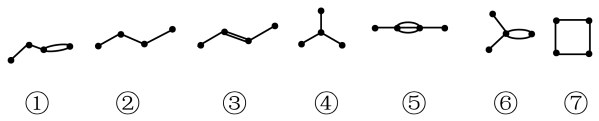
| A.①的名称为1-丁烯 | B.①③⑥互为同分异构体 |
| C.④与②互为同系物 | D.⑦的核磁共振氢谱只有一组峰 |
您最近一年使用:0次
2024-05-22更新
|
124次组卷
|
3卷引用:山西省运城市三晋卓越联盟2023-2024学年高二下学期期中考试化学试题
名校
解题方法
4 . 某单烯烃与水加成产物的结构简式为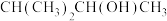 ,则关于该烯烃的说法正确的是
,则关于该烯烃的说法正确的是
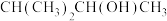 ,则关于该烯烃的说法正确的是
,则关于该烯烃的说法正确的是| A.一定为2-甲基-2-丁烯 | B.分子中所有原子共平面 |
| C.与HBr反应的产物只有一种 | D.不可能有顺反异构体 |
您最近一年使用:0次
2024-05-21更新
|
135次组卷
|
2卷引用:山西省运城市三晋卓越联盟2023-2024学年高二下学期期中考试化学试题
5 . 1.8g某有机物(只含C、H、O三种元素中的两种或三种)完全燃烧后先后通过Y、X管,其中X管增重1.76g,Y管增重0.36g;该有机物的蒸汽密度相对于氢气为45,其核磁共振氢谱显示只有一组峰,红外光谱图中可以找到C-C、C=O和O-H的吸收峰。下列关于该有机物的说法正确的是
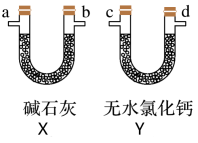
| A.属于醇类 | B.能使溴水褪色 |
| C.能发生酯化反应 | D.不能使石蕊溶液变红 |
您最近一年使用:0次
2024-05-21更新
|
78次组卷
|
2卷引用:山西省运城市三晋卓越联盟2023-2024学年高二下学期期中考试化学试题
名校
解题方法
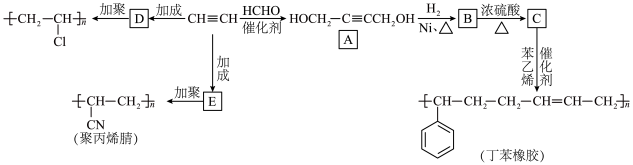
6 . 以乙炔为原料,可制备多种有机物,转化关系如图所示:
(1)实验室可用电石与水反应制取乙炔,写出反应的化学方程式:_______ 。
(2)B中只含有一种官能团,B的结构简式为_______ 。
(3)已知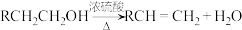 ,R为烃基,推测C的结构简式为
,R为烃基,推测C的结构简式为_______ 。
(4)下列关于丁苯橡胶的说法正确的是_______(填字母)。
(5)CH≡CH生成A的反应类型为_______ ,分子中含有2个-CHO的A的同分异构体有_______ 种(不含立体异构)。
(6)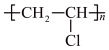 的名称为
的名称为_______ ,写出E生成聚丙烯腈的化学方程式:_______ 。
(1)实验室可用电石与水反应制取乙炔,写出反应的化学方程式:
(2)B中只含有一种官能团,B的结构简式为
(3)已知
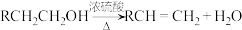 ,R为烃基,推测C的结构简式为
,R为烃基,推测C的结构简式为(4)下列关于丁苯橡胶的说法正确的是_______(填字母)。
| A.属于高分子化合物 | B. 丁苯橡胶完全加成需要 丁苯橡胶完全加成需要 |
| C.与苯互为同系物 | D.能使酸性高锰酸钾溶液褪色 |
(5)CH≡CH生成A的反应类型为
(6)
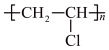 的名称为
的名称为
您最近一年使用:0次
2024-05-10更新
|
27次组卷
|
2卷引用:山西省运城市三晋卓越联盟2023-2024学年高二下学期期中考试化学试题
7 . CO是一种重要化工原料,也是一种燃料.工业上,合成 的原理为
的原理为 (正反应是放热反应).向1L恒容密闭容器中充人
(正反应是放热反应).向1L恒容密闭容器中充人 和
和 ,发生上述反应.测得CO浓度随时间,温度变化如图所示.
,发生上述反应.测得CO浓度随时间,温度变化如图所示.
(1)温度
_______  (填“>” “<”或 “=”),判断依据是
(填“>” “<”或 “=”),判断依据是___________ .
(2)下列叙述能说明该反应达到平衡状态的是________(填字母).
(3)a点:正反应速率逆反应速率__________ (填“>” “<”或 “=”,下同),逆反应速率:a_____ b.
(4) 温度下,2~6min内
温度下,2~6min内 的平均反应速率为
的平均反应速率为__________  .
.
(5) 温度下,CO平衡转化率为
温度下,CO平衡转化率为______________ .
(6)CO空气碱性燃料电池放电效率高,写出负极的电极反应式:_____________ .
 的原理为
的原理为 (正反应是放热反应).向1L恒容密闭容器中充人
(正反应是放热反应).向1L恒容密闭容器中充人 和
和 ,发生上述反应.测得CO浓度随时间,温度变化如图所示.
,发生上述反应.测得CO浓度随时间,温度变化如图所示.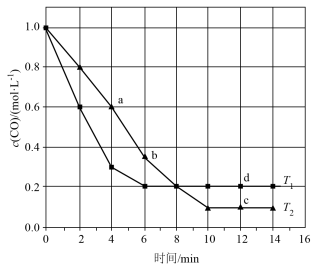
(1)温度

 (填“>” “<”或 “=”),判断依据是
(填“>” “<”或 “=”),判断依据是(2)下列叙述能说明该反应达到平衡状态的是________(填字母).
| A.混合气体密度不随时间变化 |
| B.气体总压强不随时间变化 |
C. 体积分数不随时间变化 体积分数不随时间变化 |
D.CO消耗速率等于 生成速率 生成速率 |
(3)a点:正反应速率逆反应速率
(4)
 温度下,2~6min内
温度下,2~6min内 的平均反应速率为
的平均反应速率为 .
.(5)
 温度下,CO平衡转化率为
温度下,CO平衡转化率为(6)CO空气碱性燃料电池放电效率高,写出负极的电极反应式:
您最近一年使用:0次
8 . 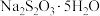 俗称“大苏打”,它是一种常用的试剂.
俗称“大苏打”,它是一种常用的试剂.
(1)工业上,常用 溶液吸收尾气中的
溶液吸收尾气中的 ,氧化产物为
,氧化产物为 .写出离子方程式:
.写出离子方程式:__________________ .理论上,能发生的氧化还原反应都可以设计成原电池.如果将上述反应设计成原电池,则正极反应式为____________ .
(2)已知: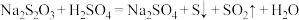
某小组设计实验探究影响化学反应速率的外界因素:
①
_________ ,设计实验I,Ⅱ的目的是_________ .
②实验测得: .由实验I、Ⅲ得出结论是
.由实验I、Ⅲ得出结论是________________ .
③根据表格信息,__________ (填“能”或“不能”)比较a和d的大小,原因是________ .
(3)已知: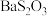 是白色难溶物.大苏打易变质生成
是白色难溶物.大苏打易变质生成 .设计实验证明某大苏打样品是否变质:
.设计实验证明某大苏打样品是否变质:__________________ .
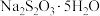 俗称“大苏打”,它是一种常用的试剂.
俗称“大苏打”,它是一种常用的试剂.(1)工业上,常用
 溶液吸收尾气中的
溶液吸收尾气中的 ,氧化产物为
,氧化产物为 .写出离子方程式:
.写出离子方程式:(2)已知:
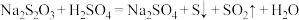
某小组设计实验探究影响化学反应速率的外界因素:
| 序号 | 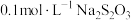 溶液 溶液 | 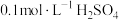 溶液 溶液 | 蒸馏水 | 温度 | 变浑浊时间 |
| I |  |  | 0 | 35℃ | a s |
| II |  | 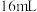 | V mL | 35℃ | b s |
| III |  |  | 0 | 45℃ | c s |
| IV |  |  | 5 mL | 40℃ | d s |

②实验测得:
 .由实验I、Ⅲ得出结论是
.由实验I、Ⅲ得出结论是③根据表格信息,
(3)已知:
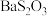 是白色难溶物.大苏打易变质生成
是白色难溶物.大苏打易变质生成 .设计实验证明某大苏打样品是否变质:
.设计实验证明某大苏打样品是否变质:
您最近一年使用:0次
9 . 某小组利用图1装置探究X和Y的反应.
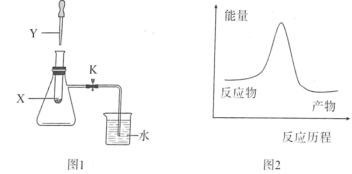
A.若X为 ,Y为盐酸,导管形成一段液柱,则能量变化如图2 ,Y为盐酸,导管形成一段液柱,则能量变化如图2 |
B.若X为 ,Y为水.烧杯中产生气泡,则能量变化如图2 ,Y为水.烧杯中产生气泡,则能量变化如图2 |
| C.若X为铜铁合金,Y为稀硫酸,烧杯中产生气泡,则X和Y的反应是吸热反应 |
D.若X为铝粉,Y为 溶液,烧杯中产生气泡,则该反应的反应物断键吸收的能量高于生成物成键释放的能量 溶液,烧杯中产生气泡,则该反应的反应物断键吸收的能量高于生成物成键释放的能量 |
您最近一年使用:0次
10 . 部分含氮物质“价-类”关系如图所示.下列叙述错误的是
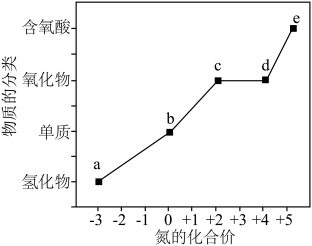
| A.c、d分别与a在一定条件下都可以生成b |
| B.浓e溶液贮存于棕色瓶并存放在阴凉处 |
| C.实验室用氯化铵和消石灰共热制备a |
| D.在灼热铂丝作用下浓a溶液在空气中一步生成d |
您最近一年使用:0次



