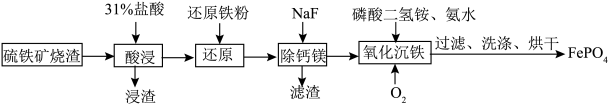
1 . 磷酸铁(FePO4)常用作电极材料、陶瓷等。以硫铁矿烧渣(主要成分)Fe2O3、SiO2,少量的Fe3O4、CaO、MgO)为原料制备磷酸铁的流程如下: ,
, ,
, 。
。
回答下列问题:
(1)基态 核外电子排布式为
核外电子排布式为________ 。
(2)浸渣的主要成分为________ (填化学式)。
(3)检验“还原”之后的溶液中是否含 的操作是
的操作是________ 。
(4)经测定“除钙镁”后的溶液中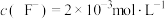 ,则溶液中
,则溶液中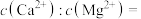
________ 。
(5)写出“氧化沉铁”时反应的离子方程式:________ 。纯净磷酸铁呈白色,而实际制备的磷酸铁产品略带棕黄色,可能是产品中混有________ (填化学式)杂质。
(6)若1t硫铁矿烧渣中含amolFe2O3、bmolFe3O4,按上述流程理论上最多可生产________ (用含a、b的算式表示)kg的FePO4。
(7)CaF2晶体的晶胞结构如图所示,晶体中相邻的8个F-形成的最小正方体的体积与晶胞体积的比是________ 。
 ,
, ,
, 。
。回答下列问题:
(1)基态
 核外电子排布式为
核外电子排布式为(2)浸渣的主要成分为
(3)检验“还原”之后的溶液中是否含
 的操作是
的操作是(4)经测定“除钙镁”后的溶液中
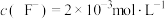 ,则溶液中
,则溶液中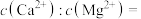
(5)写出“氧化沉铁”时反应的离子方程式:
(6)若1t硫铁矿烧渣中含amolFe2O3、bmolFe3O4,按上述流程理论上最多可生产
(7)CaF2晶体的晶胞结构如图所示,晶体中相邻的8个F-形成的最小正方体的体积与晶胞体积的比是
您最近一年使用:0次
2024-09-18更新
|
370次组卷
|
4卷引用:山西省运城市康杰中学2024-2025学年高三上学期一模考试 化学试题
名校
2 . H2S是一种有毒气体,利用H2S与CH4的反应可将其转化为有价值的H2、S2等。发生的反应有:
反应ⅰ: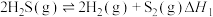
反应ⅱ:
回答下列问题:
(1)CO2中心原子价层电子对数为________ 。
(2)已知相关化学键的键能如下表:
反应ⅰ: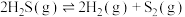 的
的
________ kJ⋅mol-1。
(3)一定温度下,在体积为2L的刚性容器中,充入1molCH4和2molH2S,发生反应i和反应ⅱ,5min时反应达到平衡,H2S的平衡转化率为40%, 。
。
①下列叙述中能说明反应ⅱ达到平衡状态的是________ (填字母)。
A. B.混合气体的密度不再变化
B.混合气体的密度不再变化
C.断裂1molC—H的同时生成1molC=S D.混合气体的平均摩尔质量不再变化
②0~5min内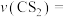
________ mol⋅L-1⋅min-1。
③此温度下,反应ⅱ的平衡常数Kx=________ (Kx是以平衡物质的量分数代替平衡浓度计算的平衡常数)。
(4)在常压和不同温度下,将H2S和CH4按照2∶1的体积比充入热解器中,用N2稀释,发生反应ⅰ和反应ⅱ。反应相同时间后,H2、S2和CS2的体积分数随温度的变化关系如图所示。
________ (填“>”“<”或“=”)0,低于1000℃时反应ⅱ________ (填“能”或“不能”)发生。
②1050℃时,H2的体积分数为________ 。
③温度高于1100℃时,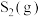 体积分数减小的原因是
体积分数减小的原因是________ 。
反应ⅰ:
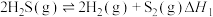
反应ⅱ:

回答下列问题:
(1)CO2中心原子价层电子对数为
(2)已知相关化学键的键能如下表:
化学键 | H—H | H—S | S2(化学键视为S—S) |
键能/(kJ·mol-1) | 436 | 339 | 298 |
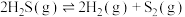 的
的
(3)一定温度下,在体积为2L的刚性容器中,充入1molCH4和2molH2S,发生反应i和反应ⅱ,5min时反应达到平衡,H2S的平衡转化率为40%,
 。
。①下列叙述中能说明反应ⅱ达到平衡状态的是
A.
 B.混合气体的密度不再变化
B.混合气体的密度不再变化C.断裂1molC—H的同时生成1molC=S D.混合气体的平均摩尔质量不再变化
②0~5min内
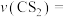
③此温度下,反应ⅱ的平衡常数Kx=
(4)在常压和不同温度下,将H2S和CH4按照2∶1的体积比充入热解器中,用N2稀释,发生反应ⅰ和反应ⅱ。反应相同时间后,H2、S2和CS2的体积分数随温度的变化关系如图所示。
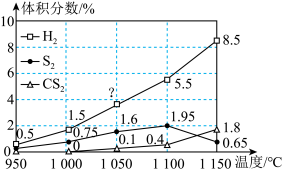

②1050℃时,H2的体积分数为
③温度高于1100℃时,
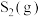 体积分数减小的原因是
体积分数减小的原因是
您最近一年使用:0次
2024-09-16更新
|
163次组卷
|
4卷引用:山西省运城市康杰中学2024-2025学年高三上学期一模考试 化学试题
名校
解题方法
3 . 一种以HCOOH为燃料的电池装置如图所示,下列说法正确的是
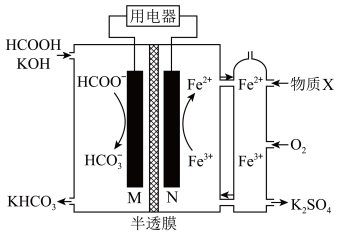
| A.放电时,电极M上发生还原反应 |
| B.理论上消耗HCOOH与O2的物质的量相等 |
| C.放电过程中需补充的物质X为KOH |
| D.理论上,若有1molHCOO—反应时,则有2molK+通过半透膜 |
您最近一年使用:0次
2024-09-04更新
|
233次组卷
|
3卷引用:山西省运城市康杰中学2024-2025学年高三上学期一模考试 化学试题
名校
解题方法
4 . 化学实验室安全至关重要。下列说法正确的是
| A.实验室制备NO2时应该在通风橱中进行 |
| B.苯酚不慎沾在手上,先用水冲洗,再用乙醇冲洗 |
| C.金属钠着火,立即用CO2灭火器进行灭火 |
D.具有 标识的化学品为易燃类物质,应注意防火 标识的化学品为易燃类物质,应注意防火 |
您最近一年使用:0次
2024-09-04更新
|
105次组卷
|
2卷引用:山西省运城市康杰中学2024-2025学年高三上学期一模考试 化学试题
5 . 图1为γ-AgI立方晶胞结构(Ag+未画出),晶胞中I-处于顶点和面心;γ-AgI晶胞沿x、y、z轴方向的投影均如图2所示,已知NA表示阿伏加德罗常数的值。γ-AgI晶胞的密度为ρg⋅cm-³,下列说法正确的是
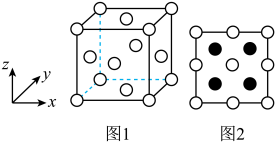
| A.Ag与Cu同族,Ag在元素周期表中位于d区 |
| B.Ag+填充在I-构成的正四面体空隙中 |
| C.与I-等距离且最近的I-有6个 |
D.晶胞中两个最近的Ag+之间的距离为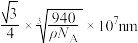 |
您最近一年使用:0次
2024-09-02更新
|
83次组卷
|
3卷引用:山西省运城市康杰中学2024-2025学年高三上学期一模考试 化学试题
名校
解题方法
6 . 已知氨氮废水中氮元素多以 和NH3⋅H2O的形式存在。某工厂用稍过量NaClO溶液处理氨氮废水的流程如下:
和NH3⋅H2O的形式存在。某工厂用稍过量NaClO溶液处理氨氮废水的流程如下:
 和NH3⋅H2O的形式存在。某工厂用稍过量NaClO溶液处理氨氮废水的流程如下:
和NH3⋅H2O的形式存在。某工厂用稍过量NaClO溶液处理氨氮废水的流程如下: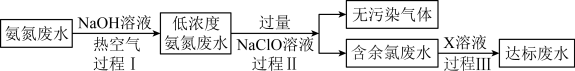
| A.过程Ⅰ鼓入热空气的作用是降低氨气溶解度,使氨气逸出 |
| B.过程Ⅱ中无污染气体为N2 |
| C.过程Ⅱ后含余氯废水的碱性增强 |
| D.过程Ⅲ加入的溶液X可能是Na2SO3溶液 |
您最近一年使用:0次
2024-09-02更新
|
144次组卷
|
2卷引用:山西省运城市康杰中学2024-2025学年高三上学期一模考试 化学试题
7 . 我国科研人员通过对嫦娥五号钻采岩屑月壤的观察分析,首次发现天然形成的少层石墨烯(2∼7层),研究成果发表在2024年6月份NationalScienceReview(国家科学评论)期刊上。这一发现为人类认识月球的地质活动和演变历史以及月球的环境特点提供了新见解。下列说法错误的是
A.天宫空间站使用石墨烯存储器,石墨烯与足球烯( )互为同素异形体 )互为同素异形体 |
B.月壤中的嫦娥石[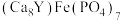 ],其成分属于无机盐 ],其成分属于无机盐 |
C.嫦娥五号、嫦娥六号探测器均装有太阳能电池板,其主要成分是高纯 |
| D.长征五号遥八运载火箭使用了煤油液氧推进剂,其中煤油是煤经过干馏获得的产物 |
您最近一年使用:0次
名校
解题方法
8 . 分子筛是一种高度有序的孔道结构材料,可实现对水分子的选择性吸附。E是一种重要的药物中间体,可由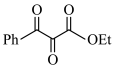 通过如图路线进行合成:
通过如图路线进行合成:
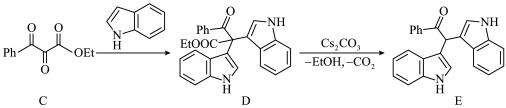
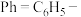 ,
,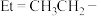 。下列说法错误的是
。下列说法错误的是| A.D中含有4种官能团 |
B.1mol分子C最多可与5mol 加成 加成 |
| C.C→D的过程中加入分子筛,可有效提高D的产率 |
| D.E的核磁共振氢谱有16组峰 |
您最近一年使用:0次
名校
解题方法
9 . 化学物质的研究与社会发展息息相关,下列说法错误的是
| A.我国中核集团核理化院获得公斤级丰度为99%的100Mo产品,其中100Mo与98Mo互为同位素 |
| B.2023年诺贝尔化学奖授予“发现和合成量子点”的研究者,纳米量子点分散到溶剂中形成的分散系可能具有丁达尔效应 |
| C.镁铝合金是建造航空母舰的主体材料,可以在N2的保护下由镁、铝熔融后煅烧而成 |
| D.制作“青玉交龙纽”玉玺的材料的主要成分属于无机非金属材料 |
您最近一年使用:0次
10 . 工业上用电解乙烯的方法制取环氧乙烷( ),中间隔膜为阴离子交换膜,电极B上生成环氧乙烷,电解质溶液均为食盐水,其电解工作原理如图所示。下列说法不正确的是
),中间隔膜为阴离子交换膜,电极B上生成环氧乙烷,电解质溶液均为食盐水,其电解工作原理如图所示。下列说法不正确的是
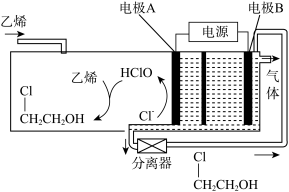
A.电极 为阳极 为阳极 |
B.左侧电解池电解一段时间后溶液的 降低 降低 |
C.电极B发生的电极反应只有2ClCH2CH2OH+2e-=2 +H2↑+2Cl- +H2↑+2Cl- |
D.乙烯生成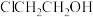 的反应类型为加成反应 的反应类型为加成反应 |
您最近一年使用:0次



