名校
1 .  恒容密闭容器中通入A、B各
恒容密闭容器中通入A、B各 ,在一定温度下进行反应:
,在一定温度下进行反应: ,
, ,
, 时达到平衡,生成
时达到平衡,生成 。下列说法不正确的是
。下列说法不正确的是
 恒容密闭容器中通入A、B各
恒容密闭容器中通入A、B各 ,在一定温度下进行反应:
,在一定温度下进行反应: ,
, ,
, 时达到平衡,生成
时达到平衡,生成 。下列说法不正确的是
。下列说法不正确的是A.①体系气体密度不变;②A的体积分数不变;③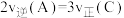 ,三种现象均可以说明该反应达到平衡 ,三种现象均可以说明该反应达到平衡 |
| B.①增加D的质量;②向体系中充入He;③抽出A减小体系压强,三种操作都不能增大逆反应速率 |
C. 末时,C的平均反应速率为 末时,C的平均反应速率为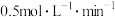 |
| D.保持其他条件不变,若换成1L的容器,平衡时A的转化率不变 |
您最近一年使用:0次
名校
2 . 史料记较,我国在明代就有了利用绿矾(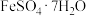 )和硝酸钾制备硝酸的工艺,其主要流程如图所示。已知“煅烧”后产生三种气态氧化物。下列说法正确的是
)和硝酸钾制备硝酸的工艺,其主要流程如图所示。已知“煅烧”后产生三种气态氧化物。下列说法正确的是
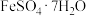 )和硝酸钾制备硝酸的工艺,其主要流程如图所示。已知“煅烧”后产生三种气态氧化物。下列说法正确的是
)和硝酸钾制备硝酸的工艺,其主要流程如图所示。已知“煅烧”后产生三种气态氧化物。下列说法正确的是
A.理论上制得1mol  需要空气的体积约为28L 需要空气的体积约为28L |
B.加入 制得硝酸的原理是硫酸的酸性强于硝酸 制得硝酸的原理是硫酸的酸性强于硝酸 |
| C.该流程中涉及化合、分解、置换、复分解四种基本反应类型 |
D.“吸收”过程中发生的反应之一为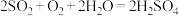 |
您最近一年使用:0次
3 . 乙烯是来自石油的重要的化工原料,乙烯的产量通常用来衡量一个国家的石油化工发展水平。
(1)反应③产物的官能团名称是______ 。
(2)反应①、⑥的反应类型分别为______ 、______ 。
(3)反应①和反应②的反应方程式分别为______ 、______ 。
(4)反应④得到的产物聚乙烯用来制造塑料,其单体是乙烯,而乙烯的碳原子最少的同系物也可以通过聚合反应得高聚物,也可以用来制塑料,该高聚物结构简式为______ 。
(5)工业上制备一氯乙烷有以下两种方案:
Ⅰ.乙烷与氯气反应; Ⅱ.乙烯与氯化氢反应。
你认为最合理的方案是______ (填代号),理由是______ 。

(1)反应③产物的官能团名称是
(2)反应①、⑥的反应类型分别为
(3)反应①和反应②的反应方程式分别为
(4)反应④得到的产物聚乙烯用来制造塑料,其单体是乙烯,而乙烯的碳原子最少的同系物也可以通过聚合反应得高聚物,也可以用来制塑料,该高聚物结构简式为
(5)工业上制备一氯乙烷有以下两种方案:
Ⅰ.乙烷与氯气反应; Ⅱ.乙烯与氯化氢反应。
你认为最合理的方案是
您最近一年使用:0次
4 . 糖类、脂肪和蛋白质是维持人体生命活动所需的三大营养物质。以下叙述正确的是
| A.淀粉和纤维素互为同分异构体 |
| B.油脂在碱性条件下的水解反应又叫做皂化反应 |
| C.能使蛋白质变性的物质有重金属盐、酒精、NaCl等 |
| D.淀粉、纤维素、油脂、蛋白质都是高分子化合物 |
您最近一年使用:0次
名校
解题方法
5 . 硫、氮的氧化物是主要的大气污染物,对大气的影响之一是导致酸雨,下列有关酸雨的说法不正确的是
| A.二氧化硫、二氧化氮是形成酸雨的主要因素 |
| B.在酸雨形成过程中没有发生氧化还原反应 |
| C.煤和石油的燃烧、汽车尾气等是酸雨污染物的主要来源 |
| D.酸雨的危害有破坏农作物,使土壤、湖泊酸化以及加速建筑物、桥梁的腐蚀等 |
您最近一年使用:0次
名校
解题方法
6 . 下列有关含氮物质的化学用语正确的是
A. 的结构式:N=N 的结构式:N=N | B.中子数为7的氮原子: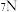 |
C. 的结构示意图: 的结构示意图: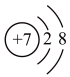 | D. 的电子式: 的电子式: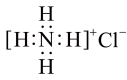 |
您最近一年使用:0次
今日更新
|
60次组卷
|
2卷引用:安徽省六安第二中学河西校区2023-2024学年高一下学期期中考试化学试题
名校
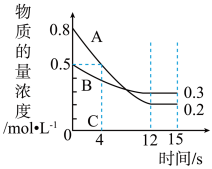
7 . 在体积固定为2 L的密闭容器中投入一定量的A和B,两种气体的物质的量浓度随时间变化的曲线如图所示,已知物质C也为气体。则:___________ (填“>”、“<”或“=”)逆反应速率;该反应达到最大限度的时间是___________ s。经测定,前4 s内v(C)=0.05 mol·L-1·s-1,则该反应的化学方程式为___________ 。
(2)从反应开始到12 s内,A的转化率为___________ 。
(3)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,反应相同时间后,测得三个容器中的反应速率分别为:甲:v(A)=0.3 mol·L-1·s-1;乙:v(B)=0.12 mol·L-1·s-1;丙:v(C)=9.6 mol·L-1·min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为___________ (用甲、乙、丙表示)。
(4)一定能够判断该反应达到平衡状态的依据是___________ (填选项)。
A.该条件下,混合气体的密度不再发生变化
B.该条件下,混合气体的压强不再发生变化
C.该条件下,单位时间内消耗3 mol A的同时生成2 mol C
D.该条件下,n(A):n(B):n(C)=2:3:4
E.该条件下,混合气体颜色不再发生变化
(5)为加快上述反应速率的,可以改变的外界条件是___________ (写出一种即可)。
(2)从反应开始到12 s内,A的转化率为
(3)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,反应相同时间后,测得三个容器中的反应速率分别为:甲:v(A)=0.3 mol·L-1·s-1;乙:v(B)=0.12 mol·L-1·s-1;丙:v(C)=9.6 mol·L-1·min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为
(4)一定能够判断该反应达到平衡状态的依据是
A.该条件下,混合气体的密度不再发生变化
B.该条件下,混合气体的压强不再发生变化
C.该条件下,单位时间内消耗3 mol A的同时生成2 mol C
D.该条件下,n(A):n(B):n(C)=2:3:4
E.该条件下,混合气体颜色不再发生变化
(5)为加快上述反应速率的,可以改变的外界条件是
您最近一年使用:0次
名校
解题方法
8 . 工业上CH4(g)与CO2(g)发生反应: 。已知反应中涉及的化学键的键能(断裂或形成1 mol化学键时吸收或放出的能量)数据如表所示。下列说法正确的是
。已知反应中涉及的化学键的键能(断裂或形成1 mol化学键时吸收或放出的能量)数据如表所示。下列说法正确的是
 。已知反应中涉及的化学键的键能(断裂或形成1 mol化学键时吸收或放出的能量)数据如表所示。下列说法正确的是
。已知反应中涉及的化学键的键能(断裂或形成1 mol化学键时吸收或放出的能量)数据如表所示。下列说法正确的是| 化学键 | C—H | C=O | C≡O | H—H |
| 键能/(kJ·mol-1) | 413 | 803 | 1076 | 436 |
| A.断裂1 mol CH4中所有的化学键需要吸收的能量为413 kJ |
| B.由已知的键能数据可推出上述反应的正向反应为放热反应 |
| C.CH4(g)和CO2(g)的总能量大于CO(g)和H2(g)的总能量 |
| D.当上述反应生成1 mol H2(g)时,吸收的热量为117 kJ |
您最近一年使用:0次
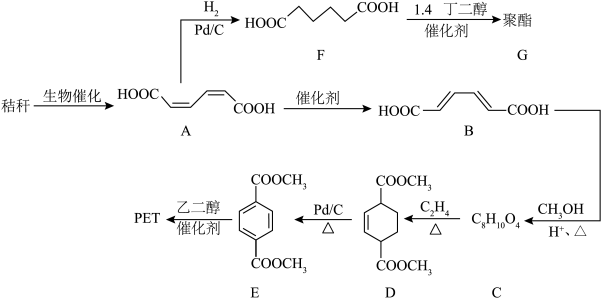
9 . 秸秆(含多糖类物质)的综合利用具有重要意义。以秸秆为原料合成聚酯类高分子的路线如图。
(1)下列有关A的说法正确的是___________ (填标号)。
a.无顺反异构体 b.实验式为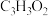
c.不能发生氧化反应 d.能与金属Na、NaOH和 反应
反应
(2)B中所含官能团的名称为___________ ,0.1molB最多可与___________ L(标准状况下) 发生加成反应。
发生加成反应。
(3)C→D的反应类型为___________ 。
(4)乙二醇的结构简式为___________ 。
(5)F→G的反应方程式为___________ 。
(6)J是E的同分异构体,符合下列条件的J的结构有___________ 种(不考虑立体异构)。
①不含 ;
;
②除苯环外不含其他环;
③能与 发生反应且0.1molJ最多可消耗0.2mol
发生反应且0.1molJ最多可消耗0.2mol 。
。
其中核磁共振氢谱显示只有三组峰且峰面积之比为1∶2∶2的结构简式为___________ 。
(7)结合所学知识并参考上述合成路线,设计仅以 为碳源合成
为碳源合成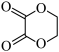 的路线
的路线___________ (无机试剂任选)。
(1)下列有关A的说法正确的是
a.无顺反异构体 b.实验式为
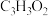
c.不能发生氧化反应 d.能与金属Na、NaOH和
 反应
反应(2)B中所含官能团的名称为
 发生加成反应。
发生加成反应。(3)C→D的反应类型为
(4)乙二醇的结构简式为
(5)F→G的反应方程式为
(6)J是E的同分异构体,符合下列条件的J的结构有
①不含
 ;
;②除苯环外不含其他环;
③能与
 发生反应且0.1molJ最多可消耗0.2mol
发生反应且0.1molJ最多可消耗0.2mol 。
。其中核磁共振氢谱显示只有三组峰且峰面积之比为1∶2∶2的结构简式为
(7)结合所学知识并参考上述合成路线,设计仅以
 为碳源合成
为碳源合成 的路线
的路线
您最近一年使用:0次
10 . 为了减缓温室效应,实现碳中和目标,可将CO2转化为二甲醚、甲醇等产品。CO2与H2制二甲醚(CH3OCH3)的主要反应如下:
反应I:
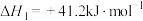
反应II:
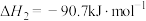
反应III:

反应IV:
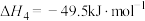
请回答下列问题:
(1)CO2(g)和H2(g)生成CH3OCH3(g)和H2O(g)的
___________ 。
(2)反应IV的反应历程如图所示(部分物质未画出)。___________ 。
(3)CO2在一定条件下催化加氢可生成CH3OH,主要发生三个反应(即反应I、II、III)。
①若在恒容密闭容器中只发生反应I,下列措施可提高H2平衡转化率的是___________ (填字母)。
a.加入催化剂 b.升高温度 c.充入惰性气体
②在某密闭容器中充入1molCO2、3molH2,在恒压(0.1MPa)下发生上述反应I、II、III,测得平衡时CO2的转化率和CH3OCH3的选择性随温度的变化如图所示。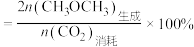 。
。
温度高于300℃时,曲线N随温度升高而升高的原因是___________ ;若Q点温度下CO的物质的量为0.08mol,则此时H2O的物质的量为___________ ,该温度下反应III的Kp=___________ (Kp为用压强表示的平衡常数,分压=总压×物质的量分数)。
反应I:

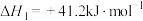
反应II:

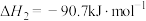
反应III:


反应IV:

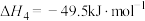
请回答下列问题:
(1)CO2(g)和H2(g)生成CH3OCH3(g)和H2O(g)的

(2)反应IV的反应历程如图所示(部分物质未画出)。

(3)CO2在一定条件下催化加氢可生成CH3OH,主要发生三个反应(即反应I、II、III)。
①若在恒容密闭容器中只发生反应I,下列措施可提高H2平衡转化率的是
a.加入催化剂 b.升高温度 c.充入惰性气体
②在某密闭容器中充入1molCO2、3molH2,在恒压(0.1MPa)下发生上述反应I、II、III,测得平衡时CO2的转化率和CH3OCH3的选择性随温度的变化如图所示。

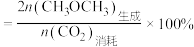 。
。温度高于300℃时,曲线N随温度升高而升高的原因是
您最近一年使用:0次



