名校
1 .  参与的乙苯耦合脱氢机理如图所示(α,β表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷,
参与的乙苯耦合脱氢机理如图所示(α,β表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷, 、
、 位点带部分负电荷)。下列说法不正确的是
位点带部分负电荷)。下列说法不正确的是
①催化剂是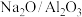 复合催化剂,如果催化剂是
复合催化剂,如果催化剂是 则主要发生乙苯的直接脱氢生成苯乙烯和氢气
则主要发生乙苯的直接脱氢生成苯乙烯和氢气
 参与的乙苯耦合脱氢机理如图所示(α,β表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷,
参与的乙苯耦合脱氢机理如图所示(α,β表示乙苯分子中C或H原子的位置:A、B为催化剂的活性位点,其中A位点带部分正电荷, 、
、 位点带部分负电荷)。下列说法不正确的是
位点带部分负电荷)。下列说法不正确的是
①催化剂是
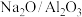 复合催化剂,如果催化剂是
复合催化剂,如果催化剂是 则主要发生乙苯的直接脱氢生成苯乙烯和氢气
则主要发生乙苯的直接脱氢生成苯乙烯和氢气②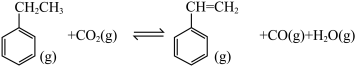

| A.反应过程中需要控制催化剂表面的酸碱性,不能太高或太低 |
B. 复合催化剂使 复合催化剂使 位点带较多负电荷,活化C-H发生耦合脱氢 位点带较多负电荷,活化C-H发生耦合脱氢 |
C.恒温恒容,其他条件不变时,适当提高 分压,可能使反应速率加快 分压,可能使反应速率加快 |
D.恒温恒压, 能提高乙苯的平衡转化率是降低了气体分压并消耗了 能提高乙苯的平衡转化率是降低了气体分压并消耗了 ,使平衡正向移动 ,使平衡正向移动 |
您最近一年使用:0次
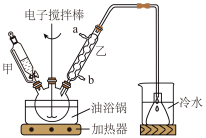
2 . 清凉茶酸乙酯(CH2CH=CHCH=CHCOOCH2CH3)是一种消毒杀菌剂,对细菌霉菌等有灭活作用。通过酯化反应制备清凉茶酸乙酯的方法如图,实验装置(部分夹持装置省略)如图所示。
Ⅱ.油浴加热,控制温度为110℃,并不断搅拌,一段时间之后停止加热和搅拌。
Ⅲ.反应混合物冷却至室温,进行操作X。
Ⅳ.在滤液中加入5%的小苏打溶液,洗涤,至混合液pH=7左右,再用蒸馏水洗涤。
V.将洗涤后混合液加入分液漏斗,进行分液。
Ⅵ.在分液后的有机层加入干燥剂,振荡,静置,过滤。
Ⅶ.对滤液进行蒸馏,收集一定温度的馏分,得到5.4mL纯净的清凉茶酸乙酯。
已知部分物质的性质如表:
(1)仪器甲的名称为______ 。
(2)写出实验中三颈烧瓶中发生的主要反应______ ,其中环己烷的作用是______ 。
(3)加热搅拌过程中忘加沸石,正确的操作是______ 。
(4)下列有关该实验过程,正确的是______ 。
(5)计算该制备实验的产率:______ (保留三位有效数字)。
Ⅱ.油浴加热,控制温度为110℃,并不断搅拌,一段时间之后停止加热和搅拌。
Ⅲ.反应混合物冷却至室温,进行操作X。
Ⅳ.在滤液中加入5%的小苏打溶液,洗涤,至混合液pH=7左右,再用蒸馏水洗涤。
V.将洗涤后混合液加入分液漏斗,进行分液。
Ⅵ.在分液后的有机层加入干燥剂,振荡,静置,过滤。
Ⅶ.对滤液进行蒸馏,收集一定温度的馏分,得到5.4mL纯净的清凉茶酸乙酯。
已知部分物质的性质如表:
| 沸点/℃ | 密度/(g•cm-3) | 水溶性 | 备注 | |
| 乙醇 | 78 | 0.789 | 混溶 | |
| 清凉茶酸 | 228 | 1.204 | 易溶 | |
| 清凉茶酸乙酯 | 195 | 0.926 | 难溶 | |
| 环己烷 | 80.7 | 0.780 | 难溶 | 挥发过程中可带出较多的水 |
(2)写出实验中三颈烧瓶中发生的主要反应
(3)加热搅拌过程中忘加沸石,正确的操作是
(4)下列有关该实验过程,正确的是
| A.乙中的进水口为a |
| B.操作X使用的玻璃仪器有玻璃棒,漏斗,烧杯 |
| C.加入小苏打是为了中和混合物中的酸性物质 |
| D.分液后的有机层加入碱石灰干燥 |
您最近一年使用:0次
解题方法
3 . 非洛地平具有扩张动脉、降低血压的作用,可用于治疗高血压。一种合成路线如下: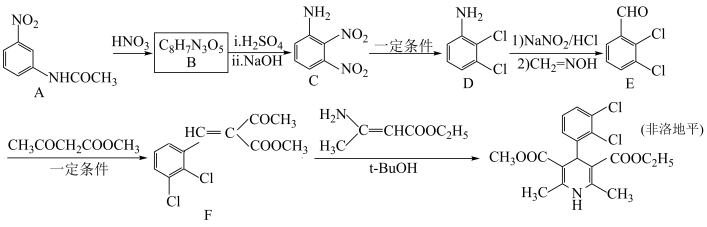
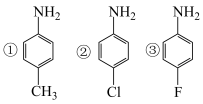
(1)已知氨基的N原子上电子云密度越大,碱性越强;卤素为吸电子基,甲基为推电子基。下列有机物碱性由强到弱排序为
(3)非洛地平中含氧官能团是
(4)E→F的化学方程式为
(5)在A的芳香族同分异构体中,同时含
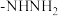 、-CHO、-OOCH结构的有
、-CHO、-OOCH结构的有(6)以苯甲醇和
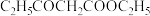 为原料合成
为原料合成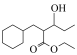 ,设计合成路线
,设计合成路线
您最近一年使用:0次
今日更新
|
93次组卷
|
3卷引用:2024届河南省百所名校仿真模拟大联考三模考试理综试题-高中化学
名校
4 . 下列说法不正确的是
| A.可用X射线衍射技术测定青蒿素分子的键长、键角,但不能测键能 |
| B.顺丁橡胶用二硫键等作用力将线型结构连接为网状结构,且硫化交联的程度越大,弹性和强度越好 |
| C.肽链通过肽键中的氧原子与氢原子之间存在的氢键作用形成蛋白质的二级结构 |
| D.质谱法可用来测定物质的部分结构信息 |
您最近一年使用:0次
名校
5 . 有机氟化学在材料科学、催化化学以及生物化学等领域引起了越来越多的重视。一种以Ni的配合物Ni(IMes)L催化氟苯的碳—氟键芳基化反应制备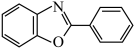 的机理如图所示。下列说法正确的是
的机理如图所示。下列说法正确的是
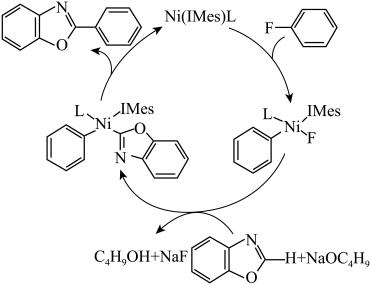
| A.该总反应原子利用率为100% |
| B.该历程涉及C-H键的断裂和形成 |
| C.该反应过程中涉及四种中间产物 |
D.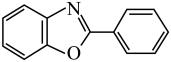 中苯环上的一氯代物7种 中苯环上的一氯代物7种 |
您最近一年使用:0次
昨日更新
|
127次组卷
|
2卷引用:2024届河南省信阳市高三下学期高考考前押题理科综合试卷-高中化学
解题方法
6 . 某工厂通过如下装置处理两个车间的废气(电极均为惰性电极),既处理了污染物,又变废为宝。下列说法正确的是
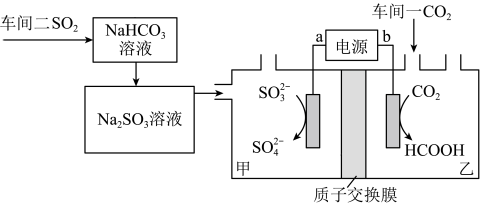
A.电极电势: |
B.工作时 由乙池移向甲池 由乙池移向甲池 |
C.通电一段时间后甲区域的 增大 增大 |
D.阴极反应式: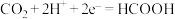 |
您最近一年使用:0次
名校
解题方法
7 . 某高分子化合物M常用于制作眼镜镜片,可由N和P两种物质合成,M、N、P的结构如图所示,下列说法正确的是
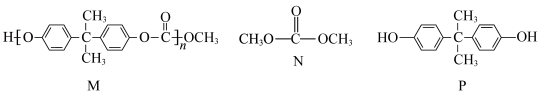
| A.N与P合成M的反应为加聚反应 | B.M的链节中在同一平面的碳原子最多有14个 |
| C.P在空气中很稳定,可以保存在广口瓶中 | D.常温下,M、N、P均易溶于水 |
您最近一年使用:0次
昨日更新
|
338次组卷
|
4卷引用:河北省2024届高三下学期普通高中学业水平选择性考试化学冲刺卷(二)
8 . 龙舟节即端午节,为中国国家法定节假日之一,并被列入《人类非物质文化遗产代表作名录》。下列有关端午节习俗中化学知识的说法错误的是
| A.黄米小枣粽子富含支链淀粉 | B.撞鸡蛋活动中鸡蛋发生了化学变化 |
| C.艾蒿中的纤维素可水解生成葡萄糖 | D.龙舟表面涂上桐油可增强其耐腐蚀性 |
您最近一年使用:0次
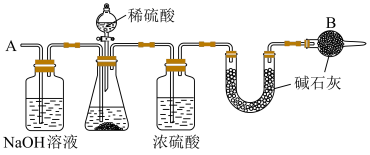
9 . 某学习小组为探究Mg与酸、碱、盐溶液的反应。完成如下实验:
回答下列问题:
(1)实验前除去镁表面氧化物的方法是______ 。
(2)实验Ⅰ的离子方程式为____________ 。
(3)经实验分析,实验Ⅲ中产生的气体为 和
和 混合气体。产生
混合气体。产生 气体的原因是
气体的原因是____________ 。
(4)该组同学们比较实验Ⅱ、Ⅲ后,分析认为:实验Ⅲ能快速反应的原因,与溶液中白色沉淀有关。为探究其成分,设计了如下实验。
取出镁条,将沉淀过滤、洗涤、低温烘干,得到纯净固体 。将一半固体放入锥形瓶中,按如图连接好装置。滴加稀硫酸到无气体放出为止,在
。将一半固体放入锥形瓶中,按如图连接好装置。滴加稀硫酸到无气体放出为止,在 处通入足量空气。最后称量
处通入足量空气。最后称量 形管增重
形管增重 。将另一半固体高温灼烧,最后剩余固体氧化物为
。将另一半固体高温灼烧,最后剩余固体氧化物为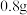 。
。____________ 。
②固体充分高温灼烧后,需要放在______ (填仪器名称)中冷却后才能称量。称量时______ (选填“是”“不是”)采用托盘天平称量。
(5)依据以上分析,实验Ⅲ中发生反应的方程式为____________ 。通过以上实验得出结论: 置换氢气与
置换氢气与 、温度、
、温度、 与溶液接触面积有关,在
与溶液接触面积有关,在 溶液中,生成的沉淀能破坏
溶液中,生成的沉淀能破坏 表面覆盖的
表面覆盖的 ,从而较快进行。
,从而较快进行。
编号 | 操作 | 现象 |
Ⅰ | 将镁条放入 | 迅速放出大量气体,试管壁发热 |
Ⅱ | 将镁条放入pH为 | 无明显现象 |
Ⅲ | 将镁条放入pH为 | 放出气体,溶液中有白色沉淀生成 |
(1)实验前除去镁表面氧化物的方法是
(2)实验Ⅰ的离子方程式为
(3)经实验分析,实验Ⅲ中产生的气体为
 和
和 混合气体。产生
混合气体。产生 气体的原因是
气体的原因是(4)该组同学们比较实验Ⅱ、Ⅲ后,分析认为:实验Ⅲ能快速反应的原因,与溶液中白色沉淀有关。为探究其成分,设计了如下实验。
取出镁条,将沉淀过滤、洗涤、低温烘干,得到纯净固体
 。将一半固体放入锥形瓶中,按如图连接好装置。滴加稀硫酸到无气体放出为止,在
。将一半固体放入锥形瓶中,按如图连接好装置。滴加稀硫酸到无气体放出为止,在 处通入足量空气。最后称量
处通入足量空气。最后称量 形管增重
形管增重 。将另一半固体高温灼烧,最后剩余固体氧化物为
。将另一半固体高温灼烧,最后剩余固体氧化物为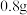 。
。
②固体充分高温灼烧后,需要放在
(5)依据以上分析,实验Ⅲ中发生反应的方程式为
 置换氢气与
置换氢气与 、温度、
、温度、 与溶液接触面积有关,在
与溶液接触面积有关,在 溶液中,生成的沉淀能破坏
溶液中,生成的沉淀能破坏 表面覆盖的
表面覆盖的 ,从而较快进行。
,从而较快进行。
您最近一年使用:0次
10 . 某反应体系只有六种粒子: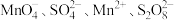 (无色)、
(无色)、 和
和 。随着反应进行,其中两种离子浓度与时间关系如图所示。下列叙述错误的是
。随着反应进行,其中两种离子浓度与时间关系如图所示。下列叙述错误的是
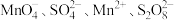 (无色)、
(无色)、 和
和 。随着反应进行,其中两种离子浓度与时间关系如图所示。下列叙述错误的是
。随着反应进行,其中两种离子浓度与时间关系如图所示。下列叙述错误的是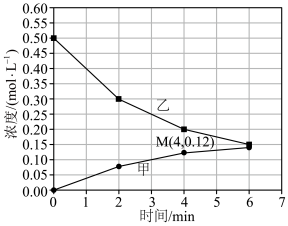
A.图中乙代表 ,甲代表 ,甲代表 |
| B.若溶液由无色变为紫红色,则反应已发生 |
C.每消耗 乙时转移 乙时转移 电子 电子 |
D.该反应为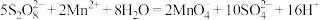 |
您最近一年使用:0次

 稀硫酸中
稀硫酸中 的
的 溶液中
溶液中

