1 . 下列有关物质的性质与用途具有对应关系的是( )
| A.FeCl3溶液显酸性,可用于刻蚀电路板 | B.CaO具有吸水性,可用作食品脱氧剂 |
| C.NH4Cl具有酸性,可用于金属除锈 | D.活性炭具有还原性,可用于水质净化 |
您最近一年使用:0次
2020-05-14更新
|
226次组卷
|
4卷引用:湖北省2020年荆、荆、襄、宜四地七校考试联盟高一联考化学模拟试题
2 . 下列有关物质性质与用途具有对应关系的是( )
| A.铁的强度大,可用铁罐贮运浓硫酸 |
| B.明矾溶液呈酸性,可用于净化水质 |
| C.Al2O3熔点高,可用作耐高温材料 |
| D.浓硫酸具有强氧化性,可用于干燥CO2 |
您最近一年使用:0次
2019·湖南湘潭·一模
3 . 化学在生活中有着广泛的应用。下列对应关系或运用错误的是( )
| 选项 | 化学性质 | 实际应用 |
| A | ClO2具有强氧化性 | 自来水消毒杀菌 |
| B | 碳酸钠能与盐酸反应 | 治疗胃酸过多 |
| C | NaHCO3受热分解并且生成气体 | 焙制糕点 |
| D | Al(OH)3分解吸收大量热量并有H2O生成 | 阻燃胶合板 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . Ⅰ.某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5 μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系________ (填“属于”或“不属于”)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断待测试样为_____ (填“酸”或“碱”)性,表示该试样酸碱性的c(H+)或c(OH-)=______ mol·L-1。
Ⅱ.氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(3)“维生素C可以将食物中的Fe3+转化为Fe2+,说明维生素C______ 具有(填“氧化性”或“还原性”)。
(4)二氧化氯是一种高效消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中每生成1molClO2分子,转移电子的数目为_____ 。
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是_____ 。
A.O2 B.FeCl2 C.KCl D.KMnO4
(1)PM2.5分散在空气中形成的分散系
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ |  |  |  | Cl- |
| 浓度/mol·L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
Ⅱ.氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(3)“维生素C可以将食物中的Fe3+转化为Fe2+,说明维生素C
(4)二氧化氯是一种高效消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中每生成1molClO2分子,转移电子的数目为
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐(
 ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是A.O2 B.FeCl2 C.KCl D.KMnO4
您最近一年使用:0次
2024-02-14更新
|
58次组卷
|
2卷引用:河南省漯河市高级中学2023-2024学年高一上学期模拟预测化学试题
解题方法
5 . 有关物质的转化关系如图所示。C为常见的调味品,D是常见的无色液体。E、F、H和J均为气体,其中H和J为单质,且两者在一定条件下可生成E。
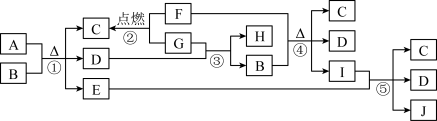
(1)物质的性质决定物质的用途。物质I的溶液可用作家用消毒剂、漂白液,是因为物质I具有__ 性。
(2)写出反应①的化学方程式:_____ 。
(3)写出反应③的化学方程式,并用单线桥表示电子转移的方向和数目 :___ 。
(4)写出反应④的离子方程式:____ 。
(5)写出反应⑤的化学方程式:____ 。

(1)物质的性质决定物质的用途。物质I的溶液可用作家用消毒剂、漂白液,是因为物质I具有
(2)写出反应①的化学方程式:
(3)写出反应③的化学方程式,
(4)写出反应④的离子方程式:
(5)写出反应⑤的化学方程式:
您最近一年使用:0次
6 . 过氧化钠在供氧、防腐、除臭、微量分析等多方面有着重要用途,工业生产过氧化钠的方法是将除去二氧化碳且干燥后的空气通入熔融的钠(温度180~200℃) 中得到氧化钠,然后增加空气流量并迅速升高温度至300~400℃即可得到过氧化钠。某化学兴趣小组模拟工业流程制备过氧化钠的装置如图所示。
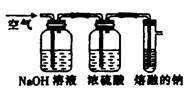
请回答下列相关问题。
(1)浓硫酸的作用是______________ 。
(2)升温至300~400 ℃时发生主要反应的化学方程式是______________ 。
(3)下列选项中的加热方式适合该实验的是_____ (填字母)。
A.水浴 B.油浴(100~260℃) C.控温电炉(150~500℃) D. 酒精喷灯(1000~1200℃)
(4)若要提高产品纯度,需在具支试管后添加一个装置,该装置应该是________ 。
(5)在具支试管后添加(4)中所要求的装置后,某同学还认为制得的过氧化钠中还含有少量的某种杂质,该杂质是________ (填化学式)。

请回答下列相关问题。
(1)浓硫酸的作用是
(2)升温至300~400 ℃时发生主要反应的化学方程式是
(3)下列选项中的加热方式适合该实验的是
A.水浴 B.油浴(100~260℃) C.控温电炉(150~500℃) D. 酒精喷灯(1000~1200℃)
(4)若要提高产品纯度,需在具支试管后添加一个装置,该装置应该是
(5)在具支试管后添加(4)中所要求的装置后,某同学还认为制得的过氧化钠中还含有少量的某种杂质,该杂质是
您最近一年使用:0次
7 . 下列物质的主要成分及用途均对应正确的是
| 选项 | A | B | C | D |
| 物质 | 碳酸氢铵 | 漂白粉 | 赤铁矿 | 双氧水 |
| 主要成分 | (NH4)2CO3 | NaClO | Fe3O4 | H2O2 |
| 用途 | 作氮肥 | 作消毒剂 | 炼铁、制磁铁 | 杀菌消毒 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-02-07更新
|
198次组卷
|
2卷引用:山东省新高考2017级模拟选课调考高一化学试题
解题方法
8 . 下图可设计成多种用途的电化学装置。下列分析正确的是
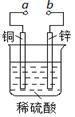

| A.当a和b用导线连接时,溶液中的SO42-向铜片附近移动 |
| B.将a与电源正极相连可以保护锌片,这叫牺牲阳极的阴极保护法 |
| C.当a和b用导线连接时,铜片上发生的反应为:2H++2e-=H2↑ |
| D.a和b用导线连接后,电路中通过0.02mol电子时,产生0.02mol气体 |
您最近一年使用:0次
2016-12-09更新
|
437次组卷
|
3卷引用:河北省邯郸市磁县第二中学2019-2020学年高一下学期线上教学检测化学试卷



