2022高一·上海·专题练习
解题方法
1 . 某工厂生产硫酸,使用一种含杂质为25%的黄铁矿样品。已知黄铁矿与氧气反应的化学方程式为4FeS2+11O2 2Fe2O3+8SO2 若取1吨该矿石,可制得98%的浓硫酸
2Fe2O3+8SO2 若取1吨该矿石,可制得98%的浓硫酸_______ 吨(设生产过程中硫损失2%)。(提示:用关系式法或原子守恒法进行计算)
 2Fe2O3+8SO2 若取1吨该矿石,可制得98%的浓硫酸
2Fe2O3+8SO2 若取1吨该矿石,可制得98%的浓硫酸
您最近一年使用:0次
2022高一·上海·专题练习
解题方法
2 . 298K时,向V升真空容器中通入n摩SO2和m摩H2S。
(1)若n=2,则当m=_______ 时,反应后容器内气体的密度最小。
(2)若2n>m,则反应后氧化产物与还原产物的质量差为_______ 克。
(3)若5n=m,且反应后氧化产物与还原产物的质量和为48克,则n+m=_______ 。
(1)若n=2,则当m=
(2)若2n>m,则反应后氧化产物与还原产物的质量差为
(3)若5n=m,且反应后氧化产物与还原产物的质量和为48克,则n+m=
您最近一年使用:0次
3 . 已知可逆反应CO(g)+H2O(g) CO2(g)+H2(g),平衡常数为K。
CO2(g)+H2(g),平衡常数为K。
(1)557℃时,若起始浓度:CO为1mol·L-1,H2O为1.5mol·L-1,平衡时CO转化率为60%,则H2O的转化率为___________ ;K值为___________ 。
(2)557℃时,若起始浓度改为:CO为1mol·L-1,H2O为3mol·L-1,平衡时H2O的转化率为___________ 。
 CO2(g)+H2(g),平衡常数为K。
CO2(g)+H2(g),平衡常数为K。(1)557℃时,若起始浓度:CO为1mol·L-1,H2O为1.5mol·L-1,平衡时CO转化率为60%,则H2O的转化率为
(2)557℃时,若起始浓度改为:CO为1mol·L-1,H2O为3mol·L-1,平衡时H2O的转化率为
您最近一年使用:0次
2022-08-27更新
|
625次组卷
|
5卷引用:2.2.1 化学平衡常数-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)
(已下线)2.2.1 化学平衡常数-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第09讲 化学平衡常数(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)福建省莆田第十五中学2019-2020学年高二上学期期末考试化学试题(已下线)2.2.2 化学平衡常数(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)河北省邯郸市魏县2022-2023学年高二上学期期末考试化学试题
4 . 磷在氧气中燃烧可能生成两种固态氧化物P2O3和P2O5。现将3.1 g单质磷(P)在3.2 g氧气中燃烧至反应物耗尽,放出X kJ的热量。
(1)反应后生成物的组成是_______ (用化学式表示)。
(2)已知单质磷的燃烧热为Y kJ·mol-1,则1 mol P与O2反应生成固态P2O3的反应热ΔH=_______ 。
(3)若3.1 g磷在3.6 g氧气中燃烧至反应物耗尽,放出Z kJ的热量,则X_______ Z(填“<”“>”或“=”)。
(4)磷的两种氧化物中较稳定的是_______ 。
(1)反应后生成物的组成是
(2)已知单质磷的燃烧热为Y kJ·mol-1,则1 mol P与O2反应生成固态P2O3的反应热ΔH=
(3)若3.1 g磷在3.6 g氧气中燃烧至反应物耗尽,放出Z kJ的热量,则X
(4)磷的两种氧化物中较稳定的是
您最近一年使用:0次
2022高二·上海·专题练习
5 . SF6是一种优良的绝缘气体,分子结构中只存在S—F键。已知:1 mol S(s)转化为气态硫原子吸收的能量为280 kJ,断裂1 mol F—F、S—F键需吸收的能量分别为160 kJ、330 kJ。则常温下1 mol硫单质与3 mol F2发生反应S(s)+3F2(g)=SF6(g)时的反应热△H =_______ 。
您最近一年使用:0次
2022高二·上海·专题练习
解题方法
6 . 用H2或CO可以催化还原NO,以达到消除污染的目的。已知在一定温度下:
N2(g)+O2(g)=2NO(g) ΔH1=+180.5kJ·mol-1 ①
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6kJ·mol-1 ②
2H2(g)+2NO(g)=N2(g)+2H2O(l) ΔH3 ③
(1)在该温度下反应①属于_______ 反应(填“吸热”或“放热”)
(2)在该温度下反应①消耗28 g N2(g)时,ΔH1′=_______ 。
(3)在该温度下反应②生成1 mol H2O(l)时,ΔH2′=_______ 。
(4)在该温度下反应③的ΔH3 =_______ 。
N2(g)+O2(g)=2NO(g) ΔH1=+180.5kJ·mol-1 ①
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6kJ·mol-1 ②
2H2(g)+2NO(g)=N2(g)+2H2O(l) ΔH3 ③
(1)在该温度下反应①属于
(2)在该温度下反应①消耗28 g N2(g)时,ΔH1′=
(3)在该温度下反应②生成1 mol H2O(l)时,ΔH2′=
(4)在该温度下反应③的ΔH3 =
您最近一年使用:0次
2022高二·上海·专题练习
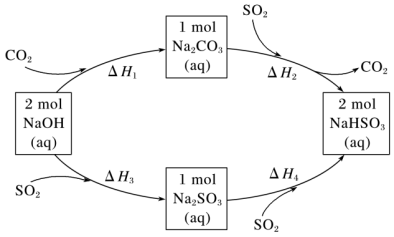
7 . 用NaOH溶液吸收热电企业产生的废气时,涉及如下转化,由下图关系可得:ΔH4=_______ 。

您最近一年使用:0次
2022高二·上海·专题练习
8 . 葡萄糖是人体所需能量的重要来源之一,设它在人体组织中完全氧化物时的热化学方程式为:C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l) ΔH=-2800kJ·mol-1。计算100g葡萄糖在人体组织中完全氧化时产生的热量_______ 。
您最近一年使用:0次
2022高二·上海·专题练习
9 . 已知:H2(g)、CH3OH(l)的燃烧热(ΔH)分别为-285.8kJ·mol-1和-726.5kJ·mol-1;CH3OH(l)=CH3OH(g) ΔH=35.2kJ·mol-1;H2O(l)=H2O(g) ΔH=44kJ·mol-1。求反应CO2(g)+3H2(g)=CH3OH(g)+H2O(g)的ΔH=_______ 。
您最近一年使用:0次
2022高一·上海·专题练习
解题方法
10 . 物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)标准状况下,含有相同氧原子数的CO和CO2 的体积之比为_______ 。
(2)100mL硫酸钠溶液中n(Na+)=0.2mol,则其中c(SO )=
)=_______ 。
(3)6.72 L(标准状况)CO 与一定量的Fe2O3恰好完全反应,生成Fe的质量为_______ g。
(4)某气体氧化物的化学式为RO2,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为_______ ,R的相对原子质量为_______ 。
(5)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO ,测得Na+、Mg2+ 和Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(SO
,测得Na+、Mg2+ 和Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(SO )=
)=_______
(6)有等体积的NaCl、CaCl2、AlCl3三种溶液,分别与足量的AgNO3溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为_______ 。
(7)V mL Al2(SO4)3溶液中含Al3+ ag,取0.5V mL溶液稀释到2V mL,则稀释后溶液中SO 的物质的量浓度是
的物质的量浓度是_______ mol·L-1。
(8)标准状况下11.2 L HCl的物质的量是_______ mol。将这些气体溶于水中配成1 L溶液,所得盐酸的物质的量浓度是_______ mol/L。
(9)将190 g MgCl2溶于水配制成1 L溶液。该溶液中MgCl2的物质的量浓度为_______ ,要配制1 mol·L-1的MgCl2溶液500 mL,需该溶液的体积为_______ 。
(1)标准状况下,含有相同氧原子数的CO和CO2 的体积之比为
(2)100mL硫酸钠溶液中n(Na+)=0.2mol,则其中c(SO
 )=
)=(3)6.72 L(标准状况)CO 与一定量的Fe2O3恰好完全反应,生成Fe的质量为
(4)某气体氧化物的化学式为RO2,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为
(5)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO
 ,测得Na+、Mg2+ 和Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(SO
,测得Na+、Mg2+ 和Cl-的物质的量浓度依次为:0.2mol•L-1、0.25mol•L-1、0.4mol•L-1,则c(SO )=
)=(6)有等体积的NaCl、CaCl2、AlCl3三种溶液,分别与足量的AgNO3溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为
(7)V mL Al2(SO4)3溶液中含Al3+ ag,取0.5V mL溶液稀释到2V mL,则稀释后溶液中SO
 的物质的量浓度是
的物质的量浓度是(8)标准状况下11.2 L HCl的物质的量是
(9)将190 g MgCl2溶于水配制成1 L溶液。该溶液中MgCl2的物质的量浓度为
您最近一年使用:0次



