1 . 将 4 g NaOH 溶解在 10 mL 水中,稀释至 1 L 后取出 10 mL,其物质的量浓度是_______ 。
您最近一年使用:0次
2 . 回答下列问题
(1)同温同压下,同体积的氨气和硫化氢气体的质量比是_______ ,原子个数之比是_______ 。
(2)同质量的氨气和硫化氢气体的体积比是_______ ,所含氢原子个数比为_______ 。
(3)若氨气和硫化氢所含氢原子个数相同,它们的物质的量之比为_______ 。
(4)甲烷(CH4)与氧气的质量比为 1∶4 时极易爆炸,此时甲烷与氧气的体积之比为_______ 。
(1)同温同压下,同体积的氨气和硫化氢气体的质量比是
(2)同质量的氨气和硫化氢气体的体积比是
(3)若氨气和硫化氢所含氢原子个数相同,它们的物质的量之比为
(4)甲烷(CH4)与氧气的质量比为 1∶4 时极易爆炸,此时甲烷与氧气的体积之比为
您最近一年使用:0次
3 . 36.3 g 某硝酸盐 R(NO3)3 含有 0.45 mol 硝酸根离子,则金属 R 的摩尔质量为_______ 。
您最近一年使用:0次
2023-02-26更新
|
192次组卷
|
3卷引用:上海市华东政法大学附属松江高级中学2022-2023学年高一下学期开学考化学试题
上海市华东政法大学附属松江高级中学2022-2023学年高一下学期开学考化学试题(已下线)专题02 物质的量-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(上海专用)上海市徐汇中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
4 . 当有多种物质参与反应时,理清各反应的先后顺序对解决问题甚为关键。
取盐酸与氯化铜的混合溶液27g放入烧杯中,逐滴滴入质量分数为20%的氢氧化钠溶液,产生沉淀质量与滴入氢氧化钠溶液质量关系如图所示。
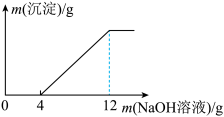
(1)滴入氢氧化钠溶液的质量在0~4g时,发生反应的化学方程式为_______ 。
(2)与氯化铜反应的氢氧化钠的质量为_______ g。
(3)原混合溶液中氯化铜的质量分数为_______ 。
现有盛88.4g 和NaOH混合溶液的大烧杯,向其中滴加质量分数为9.8%的
和NaOH混合溶液的大烧杯,向其中滴加质量分数为9.8%的 溶液,充分搅拌,烧杯中溶液的质量与滴加
溶液,充分搅拌,烧杯中溶液的质量与滴加 溶液的质量关系如图所示:
溶液的质量关系如图所示:
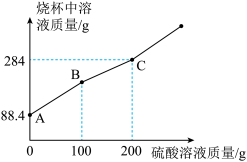
(4)AB段和BC段的实验现象为:AB段_______ ,BC段_______ 。
(5)反应完全后,生成气体的质量为_______ g。
(6)C点时可知所得溶液为不饱和溶液,则溶液中溶质的质量分数为_______ 。
取盐酸与氯化铜的混合溶液27g放入烧杯中,逐滴滴入质量分数为20%的氢氧化钠溶液,产生沉淀质量与滴入氢氧化钠溶液质量关系如图所示。

(1)滴入氢氧化钠溶液的质量在0~4g时,发生反应的化学方程式为
(2)与氯化铜反应的氢氧化钠的质量为
(3)原混合溶液中氯化铜的质量分数为
现有盛88.4g
 和NaOH混合溶液的大烧杯,向其中滴加质量分数为9.8%的
和NaOH混合溶液的大烧杯,向其中滴加质量分数为9.8%的 溶液,充分搅拌,烧杯中溶液的质量与滴加
溶液,充分搅拌,烧杯中溶液的质量与滴加 溶液的质量关系如图所示:
溶液的质量关系如图所示:
(4)AB段和BC段的实验现象为:AB段
(5)反应完全后,生成气体的质量为
(6)C点时可知所得溶液为不饱和溶液,则溶液中溶质的质量分数为
您最近一年使用:0次
名校
解题方法
5 . 工业上用甲烷(CH4)、乙烷(C2H6)的混合气体与水蒸气用催化剂进行转化反应生产氢气,反应原理:CxHy+H2O→CO+CO2+H2(未配平)。已知反应后的气体经干燥后组成如下表所示:
(1). 若反应后的气体为100mol,则反应过程中消耗H2O的物质的量为多少____ ?
(2). 计算原混合气体中甲烷与乙烷的物质的量之比____ 。
| 组成 | CH4 | C2H6 | CO | CO2 | H2 |
| 物质的量分数 | 18% | 2% | 16% | 4% | 60% |
(1). 若反应后的气体为100mol,则反应过程中消耗H2O的物质的量为多少
(2). 计算原混合气体中甲烷与乙烷的物质的量之比
您最近一年使用:0次
6 . 近来,《饮用天然矿泉水》新标准引起热议,其中备受争议的溴酸盐是一种致癌物,新标准中溴酸盐极值为0.01mg/L。已知在酸性条件下有以下反应:
①2 +I2===2
+I2===2 +Br2
+Br2
②2 +10Br-+12H+===I2+5Br2+6H2O
+10Br-+12H+===I2+5Br2+6H2O
③5Br-+ +6H+===3Br2+3H2O
+6H+===3Br2+3H2O
请回答下列问题:
(1)有同学根据反应①得出氧化性:I2>Br2的结论,请说明该结论错误的理由是:_________ 。
(2)反应②中: →l2发生的是
→l2发生的是__________ 反应(氧化、还原)。
现向含6mol的KI的硫酸溶液中逐滴滴加KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量有如图的关系:
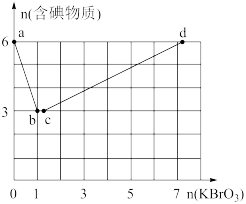
(3)完成a→b阶段的反应方程式,并标出电子转移的方向和数目:I-+BrO3-+H+→ ,________ 。
(4)b→c阶段只有一种元素化合价发生了改变,反应中氧化产物和还原产物的物质的量之比为______ 。
(5)a→b、b→c、c→d阶段的还原剂分别是______ 、_______ 、______ ,依次发生的这些反应,说明有关物质(l2、Br2、I-、Br-)还原性由强到弱的顺序是________ 。
①2
 +I2===2
+I2===2 +Br2
+Br2②2
 +10Br-+12H+===I2+5Br2+6H2O
+10Br-+12H+===I2+5Br2+6H2O③5Br-+
 +6H+===3Br2+3H2O
+6H+===3Br2+3H2O请回答下列问题:
(1)有同学根据反应①得出氧化性:I2>Br2的结论,请说明该结论错误的理由是:
(2)反应②中:
 →l2发生的是
→l2发生的是现向含6mol的KI的硫酸溶液中逐滴滴加KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量有如图的关系:

(3)完成a→b阶段的反应方程式,并标出电子转移的方向和数目:I-+BrO3-+H+→ ,
(4)b→c阶段只有一种元素化合价发生了改变,反应中氧化产物和还原产物的物质的量之比为
(5)a→b、b→c、c→d阶段的还原剂分别是
您最近一年使用:0次
解题方法
7 . 已知20℃时氯化钠的溶解度为36克。在该温度下,将碳酸钠与氯化钠的混合物17.2克,放入19克水中使其完全溶解,然后加入36.5克质量分数为20%的盐酸溶液,恰好完全反应。求:
(1)生成二氧化碳的质量________ ;
(2)反应后所得溶液的溶质的质量分数________ 。
(1)生成二氧化碳的质量
(2)反应后所得溶液的溶质的质量分数
您最近一年使用:0次
11-12高三上·黑龙江·期中
名校
8 . 粉末状试样A是由 和Fe2O3组成的混合物。进行如下实验:
和Fe2O3组成的混合物。进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;
②另取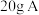 全部溶于
全部溶于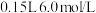 盐酸中,固体全部溶解,得溶液C;
盐酸中,固体全部溶解,得溶液C;
③将①中得到的单质B和溶液C反应,放出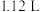 (标况)气体。同时生成溶液D,还残留有固体物质B;
(标况)气体。同时生成溶液D,还残留有固体物质B;
④用 溶液检查时,溶液D不变色。
溶液检查时,溶液D不变色。
请填空:
(1)①中引发铝热反应的实验操作是____________ ,产物中的单质B是___________________ 。
(2)②中所发生反应的化学方程式是____________ 、____________ 。
(3)③中所发生反应的离子方程式是____________ 、____________ 。
(4)若溶液D的体积仍视为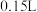 ,则该溶液中
,则该溶液中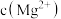 为
为____________ ,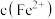 为
为____________ 。
 和Fe2O3组成的混合物。进行如下实验:
和Fe2O3组成的混合物。进行如下实验:①取适量A进行铝热反应,产物中有单质B生成;
②另取
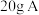 全部溶于
全部溶于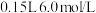 盐酸中,固体全部溶解,得溶液C;
盐酸中,固体全部溶解,得溶液C;③将①中得到的单质B和溶液C反应,放出
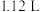 (标况)气体。同时生成溶液D,还残留有固体物质B;
(标况)气体。同时生成溶液D,还残留有固体物质B;④用
 溶液检查时,溶液D不变色。
溶液检查时,溶液D不变色。请填空:
(1)①中引发铝热反应的实验操作是
(2)②中所发生反应的化学方程式是
(3)③中所发生反应的离子方程式是
(4)若溶液D的体积仍视为
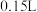 ,则该溶液中
,则该溶液中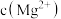 为
为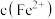 为
为
您最近一年使用:0次
2020-04-03更新
|
604次组卷
|
14卷引用:上海市青浦二中2016届高三上学期8月摸底考试化学试题
上海市青浦二中2016届高三上学期8月摸底考试化学试题(已下线)2014-2015学年上海市闵行区八校高二上学期期中联考化学试卷上海市吴淞中学2017-2018学年高二上第一次月考化学试题(已下线)上海市华东师范大学第二附属中学2018-2019学年高二上学期期末考试化学试题(已下线)2012届黑龙江省哈师大附中高三上学期期中考试化学试卷(已下线)2012-2013广西柳州铁一中高一上学期段考化学试卷2017届宁夏石嘴山三中高三上第二次适应性考试化学卷山西省阳高县第一中学2018届高三上学期第二次月考化学试题高中化学人教版 必修2 第四章 化学与自然资源的开发利用 第一节 开发利用金属矿物和海水资源 金属矿物的开发利用(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第2讲 镁、铝及其重要化合物【押题专练】河南省固始县第一中学2018-2019学年高一上学期12月月考化学试题步步为赢 高一化学暑假作业:作业十六 开发利用金属矿物和海水资源鲁教版高中化学必修1第四章《材料家族中的元素》测试卷2(已下线)【教材实验热点】12 铝热反应
名校
9 . 为测定一置于空气中的某硫酸酸化的FeSO4溶液中Fe2+被氧化的百分率,某同学准确量取pH=1(忽略Fe2+、Fe3+的水解)的FeSO4溶液200mL,加入过量BaCl2溶液,充分反应后过滤、洗涤、干燥,得到沉淀28.0g;再另取同样的FeSO4溶液200mL,向其中加入过量NaOH溶液,搅拌使其充分反应,待沉淀全部变为红褐色后,过滤、洗涤并灼烧所得固体,最终得固体8.0g.
(1)写出反应中涉及的化学方程式(至少3个)__ 、__ 、__
(2)通过计算,填写下表:
注:c(Fe2+、Fe3+)表示Fe2+和Fe3+的总的物质的量的浓度
(3)计算原溶液中Fe2+被氧化的百分率__ .
(1)写出反应中涉及的化学方程式(至少3个)
(2)通过计算,填写下表:
| c(H+) | c(SO42﹣) | c(Fe2+、Fe3+) |
注:c(Fe2+、Fe3+)表示Fe2+和Fe3+的总的物质的量的浓度
(3)计算原溶液中Fe2+被氧化的百分率
您最近一年使用:0次
19-20高一·浙江·阶段练习
名校
解题方法
10 . 某同学用一定质量分数的Na2CO3溶液做“Na2CO3+CaCl2═2NaCl+CaCO3↓”的实验。其五次实验结果如下表所示:
根据实验结果回答下列问题:
(1)哪几次反应碳酸钠有剩余(填序号)______________ 。
(2)表中X的值是______________ 。
(3)试计算碳酸钠溶液中溶质的质量分数______________ 。
根据实验结果回答下列问题:
| 实验次数 | 氯化钙质量/g | 碳酸钠溶液的质量/g | 碳酸钙的质量/g |
| 1 | 5.55 | 200 | 5 |
| 2 | 11.1 | 200 | 10 |
| 3 | 22.2 | 200 | 20 |
| 4 | 33.3 | 250 | 25 |
| 5 | 55.5 | 400 | X |
(1)哪几次反应碳酸钠有剩余(填序号)
(2)表中X的值是
(3)试计算碳酸钠溶液中溶质的质量分数
您最近一年使用:0次



