解题方法
1 . 工业上常以铝土矿为原料来冶炼金属铝。已知:铝土矿的主要成分是 (其中含有
(其中含有 、
、 等杂质)。为检测某铝土矿样品中
等杂质)。为检测某铝土矿样品中 的含量,进行如下实验过程:
的含量,进行如下实验过程:
①取矿样10.0g加入过量稀盐酸溶解,过滤弃去不溶残渣。
②将滤液稀释并在250mL容量瓶中定容后,取25.0mL逐滴加入 的NaOH溶液。得到如右图所示的变化关系。
的NaOH溶液。得到如右图所示的变化关系。___________ 。
(2)最后所得不溶于NaOH溶液的沉淀的化学式为___________ ,其物质的量为___________ 。
(3)该铝土矿样中 的质量分数为
的质量分数为___________ 。
 (其中含有
(其中含有 、
、 等杂质)。为检测某铝土矿样品中
等杂质)。为检测某铝土矿样品中 的含量,进行如下实验过程:
的含量,进行如下实验过程:①取矿样10.0g加入过量稀盐酸溶解,过滤弃去不溶残渣。
②将滤液稀释并在250mL容量瓶中定容后,取25.0mL逐滴加入
 的NaOH溶液。得到如右图所示的变化关系。
的NaOH溶液。得到如右图所示的变化关系。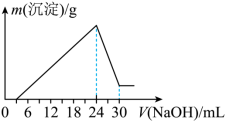
(2)最后所得不溶于NaOH溶液的沉淀的化学式为
(3)该铝土矿样中
 的质量分数为
的质量分数为
您最近一年使用:0次
2 . 化学兴趣小组为测定某大理石样品中CaCO3的含量,进行如下实验:取18.0g样品置于烧杯中,向其中加入质量分数为5%的稀盐酸(样品中杂质不与盐酸反应),测得生成气体的质量与加入盐酸的质量关系如图所示,请回答下列问题。
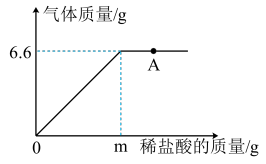
(1)实验室现有质量分数为30%的盐酸50.0g,最多可配制质量分数为5%的盐酸___________ g。
(2)图中“A”点的溶质是___________ (填化学式)。
(3)计算该样品中CaCO3的质量分数。_________ (写出计算过程,结果精确到0.1%)

(1)实验室现有质量分数为30%的盐酸50.0g,最多可配制质量分数为5%的盐酸
(2)图中“A”点的溶质是
(3)计算该样品中CaCO3的质量分数。
您最近一年使用:0次
解题方法
3 . SO2在生产生活中有重要的应用,处理不当会造成环境污染。回答下列问题:
(1)标准状况下16.0gSO2的体积为______ L,与______ molH2O中所含氧原子数相等。
(2)为测定某工厂废气中SO2的含量,课外小组的同学将废气样品经过管道通入密闭容器中的100mL0.1000mol•L-1的酸性高锰酸钾溶液。反应原理为:5SO2+2MnO +2H2O=5SO
+2H2O=5SO +2Mn2++4H+。
+2Mn2++4H+。
①该反应中被还原的元素是_____ 。
②100mL该酸性高锰酸钾溶液恰好完全反应时,转移电子的数目为______ 。
③若通入管道的废气样品为am3时,酸性高锰酸钾溶液恰好褪色,则该废气样品中SO2的含量为______ g•m-3(用含a的表达式表示,假定样品中其它气体均不参与反应,SO2可被溶液充分吸收)。
④实验需240mL0.500mol•L-1的硫酸溶液,使用的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、_____ ;需用量筒量取密度为1.84g•cm-3,质量分数为98%的浓硫酸_____ mL;若定容时俯视刻度线,则所配溶液的浓度______ (填“偏高”、“偏低”或“不变”)。
(1)标准状况下16.0gSO2的体积为
(2)为测定某工厂废气中SO2的含量,课外小组的同学将废气样品经过管道通入密闭容器中的100mL0.1000mol•L-1的酸性高锰酸钾溶液。反应原理为:5SO2+2MnO
 +2H2O=5SO
+2H2O=5SO +2Mn2++4H+。
+2Mn2++4H+。①该反应中被还原的元素是
②100mL该酸性高锰酸钾溶液恰好完全反应时,转移电子的数目为
③若通入管道的废气样品为am3时,酸性高锰酸钾溶液恰好褪色,则该废气样品中SO2的含量为
④实验需240mL0.500mol•L-1的硫酸溶液,使用的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、
您最近一年使用:0次
解题方法
4 . I.科学研究小组的同学为测定某Na2CO3和NaHCO3混合物中Na2CO3的质量分数,进行了下列相关实验。其实验流程如下:
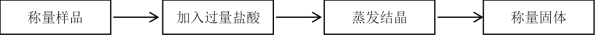
(1)该实验需要用到1.50 mol/L的稀盐酸500 mL,但实验室只有12.0 mol/L的浓盐酸。则配制稀盐酸所用浓盐酸_______ mL。
(2)若实验中测得样品质量为46.4 g,固体质量为40.95 g,请列式计算碳酸钠的质量分数_______ (保留3位有效数字)。
II.为测定某氯化亚铜样品中CuCl的含量,某同学设计如下实验:准确称取氯化亚铜样品m g,将其置于过量的FeCl3溶液中,待固体完全溶解后,加入适量稀硫酸,用a mol/L的K2Cr2O7溶液氧化反应生成的Fe2+,消耗K2Cr2O7溶液b mL,反应中 被还原为Cr3+。请列式计算样品中CuCl的质量分数
被还原为Cr3+。请列式计算样品中CuCl的质量分数_______ 。
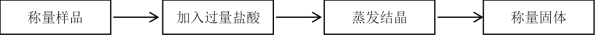
(1)该实验需要用到1.50 mol/L的稀盐酸500 mL,但实验室只有12.0 mol/L的浓盐酸。则配制稀盐酸所用浓盐酸
(2)若实验中测得样品质量为46.4 g,固体质量为40.95 g,请列式计算碳酸钠的质量分数
II.为测定某氯化亚铜样品中CuCl的含量,某同学设计如下实验:准确称取氯化亚铜样品m g,将其置于过量的FeCl3溶液中,待固体完全溶解后,加入适量稀硫酸,用a mol/L的K2Cr2O7溶液氧化反应生成的Fe2+,消耗K2Cr2O7溶液b mL,反应中
 被还原为Cr3+。请列式计算样品中CuCl的质量分数
被还原为Cr3+。请列式计算样品中CuCl的质量分数
您最近一年使用:0次
2021-01-27更新
|
261次组卷
|
2卷引用:山东省淄博市2020-2021学年高一上学期期末考试化学试题
名校
解题方法
5 . 计算:
(1)agNa2S中含b个Na+,则阿伏加德罗常数为__ (用含a、b的代数式表示)
(2)OH-与H2O数目之比为1:20的KOH水溶液中,溶质(KOH)的质量分数是__ %(结果保留一位小数)
(3)病人输液用的葡萄糖注射液是葡萄糖(化学式为C6H12O6)的水溶液,其标签上的部分内容如图所示。利用标签所提供的信息,回答下列问题:
①葡萄糖的摩尔质量为___ ;
②该注射液中葡萄糖的物质的量浓度为___ 。(保留两位小数)
③检测人的血液中葡萄糖(简称血糖)的含量,参考指标常以两种计量单位表示,即“mmol/L”和“mg/dL”(1L=10dL;1mol=1000mmol)。以“mmol/L”表示时,人的血糖正常值在3.6~6.1mmol/L之间。如果以“mg/dL”表示,血糖正常值范围是___ 。(结果保留1位小数)
(1)agNa2S中含b个Na+,则阿伏加德罗常数为
(2)OH-与H2O数目之比为1:20的KOH水溶液中,溶质(KOH)的质量分数是
(3)病人输液用的葡萄糖注射液是葡萄糖(化学式为C6H12O6)的水溶液,其标签上的部分内容如图所示。利用标签所提供的信息,回答下列问题:
| 5%葡萄糖注射液 1000mL [性状]本品为无色或几 乎无色的透明 晶体。味甜。 [规格] 1000mL, 50g。 [贮藏]密闭保存。 |
①葡萄糖的摩尔质量为
②该注射液中葡萄糖的物质的量浓度为
③检测人的血液中葡萄糖(简称血糖)的含量,参考指标常以两种计量单位表示,即“mmol/L”和“mg/dL”(1L=10dL;1mol=1000mmol)。以“mmol/L”表示时,人的血糖正常值在3.6~6.1mmol/L之间。如果以“mg/dL”表示,血糖正常值范围是
您最近一年使用:0次
6 . 过氧乙酸(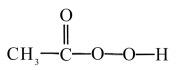 )可以有效地杀灭新冠肺炎等病毒,是一种广泛、高效、速效、廉价的消毒剂,应用广泛。回答下列回题。
)可以有效地杀灭新冠肺炎等病毒,是一种广泛、高效、速效、廉价的消毒剂,应用广泛。回答下列回题。
(1)过氧乙酸极不稳定,110℃时遇空气发生爆炸,此时发生反应的化学方程式是__________ ,所以过氧乙酸需要___________ 保存。
(2)过氧乙酸具有强氧化性,这与它的( )
)________ (填序号)键有关,向硫酸酸化的过氧乙酸溶液中加入少量KI溶液,溶液变黄,发生反应的离子方程式是_________ ,如有 过氧乙酸被还原,转移电子的物质的量是
过氧乙酸被还原,转移电子的物质的量是___________ mol。
(3)过氧乙酸可由 与
与 ,在浓硫酸催化作用下制得,反应方程式是
,在浓硫酸催化作用下制得,反应方程式是_________ ,其中浓硫酸用量(浓硫酸占反应液的体积百分数)对过氧乙酸的含量的影响如图:
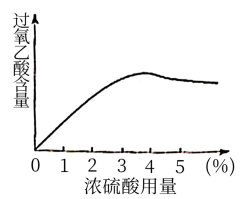
根据图表分析,浓硫酸的合适用量为___________ %(填整数)。
(4)过氧乙酸也可以用乙醛氧化法制得,反应原理为:
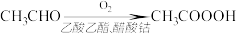
反应中乙醛的转化率为85%,生产质量分数10%的过氧乙酸溶液100kg,需要乙醛的质量为________ kg。
 )可以有效地杀灭新冠肺炎等病毒,是一种广泛、高效、速效、廉价的消毒剂,应用广泛。回答下列回题。
)可以有效地杀灭新冠肺炎等病毒,是一种广泛、高效、速效、廉价的消毒剂,应用广泛。回答下列回题。(1)过氧乙酸极不稳定,110℃时遇空气发生爆炸,此时发生反应的化学方程式是
(2)过氧乙酸具有强氧化性,这与它的(
 )
) 过氧乙酸被还原,转移电子的物质的量是
过氧乙酸被还原,转移电子的物质的量是(3)过氧乙酸可由
 与
与 ,在浓硫酸催化作用下制得,反应方程式是
,在浓硫酸催化作用下制得,反应方程式是
根据图表分析,浓硫酸的合适用量为
(4)过氧乙酸也可以用乙醛氧化法制得,反应原理为:
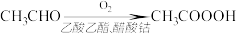
反应中乙醛的转化率为85%,生产质量分数10%的过氧乙酸溶液100kg,需要乙醛的质量为
您最近一年使用:0次
解题方法
7 . 化学兴趣小组按如图实验测定部分变质的NaOH固体中Na2CO3的含量。
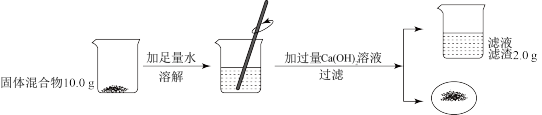
(1)根据题中信息_______ (填“能”或“不能”)计算Ca(OH)2溶液的质量分数。
(2)计算固体混合物中Na2CO3的质量_______ 。

(1)根据题中信息
(2)计算固体混合物中Na2CO3的质量
您最近一年使用:0次
8 . (1)称量一定质量表面含油污的纯铜屑(铜含量为99.84%),置于坩埚中灼烧,将油污充分氧化后除去,直至铜屑表面均呈黑色。冷却后称量,固体质量比灼烧前增加了3.2 %,固体中铜与氧化铜的质量之比为_______。(请将结果化为小数,且保留至小数点后两位)
(2)向1000克未知溶质质量分数的硫酸铜溶液中加入一定量的氢氧化钠溶液,过滤、干燥后得到蓝色固体19.6克。在所得滤液中加入过量铁粉,充分反应后,再加入足量盐酸,最后得到6.4克固体,求原溶液中硫酸铜的质量分数。(请写出计算过程)
(2)向1000克未知溶质质量分数的硫酸铜溶液中加入一定量的氢氧化钠溶液,过滤、干燥后得到蓝色固体19.6克。在所得滤液中加入过量铁粉,充分反应后,再加入足量盐酸,最后得到6.4克固体,求原溶液中硫酸铜的质量分数。(请写出计算过程)
您最近一年使用:0次
9 . 工业上“侯氏”制碱法制得的纯碱产品中常含有少量的NaCl。为测定纯碱产品中碳酸钠的含量,取23g样品置于烧杯中,加水将其溶解,然后逐滴滴入稀盐酸,当滴入200g稀盐酸时,两者恰好完全反应。生成的气体全部逸出,共收集到8.8g二氧化碳。求:
(1)所用稀盐酸中溶质的质量分数。_______
(2)23g样品中碳酸钠的质量分数(结果保留到0.1%)。_______
(1)所用稀盐酸中溶质的质量分数。
(2)23g样品中碳酸钠的质量分数(结果保留到0.1%)。
您最近一年使用:0次
20-21高一上·全国·阶段练习
10 . 医学上常用酸性高锰酸钾溶液和草酸溶液的反应用于测定血钙的含量。回答下列问题:
(1)配平以下离子方程式,并填上所需的微粒。
___ H++___ MnO4−+___ H2C2O4 ══___ CO2↑+___ Mn2++___ 。
(2)该反应中的还原剂是___ 。
(3)反应转移了0.4mol电子,则消耗KMnO4的物质的量为___ mol。
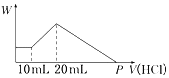
(4) 将一定质量的镁铝合金投入100mL一定物质的量浓度的盐酸中,合金全部溶解,向所得溶液中滴加5mol·L-1的NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。
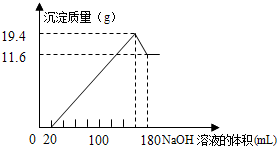
①原合金Al的质量分数是______ ;
②盐酸的物质的量浓度是________ 。

(1)配平以下离子方程式,并填上所需的微粒。
(2)该反应中的还原剂是
(3)反应转移了0.4mol电子,则消耗KMnO4的物质的量为
(4) 将一定质量的镁铝合金投入100mL一定物质的量浓度的盐酸中,合金全部溶解,向所得溶液中滴加5mol·L-1的NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液的体积关系如图所示。

①原合金Al的质量分数是
②盐酸的物质的量浓度是
您最近一年使用:0次



