真题
名校
1 . 某同学设计实验确定Al(NO3)3·xH2O的结晶水数目。称取样品7.50g,经热分解测得气体产物中有NO2、O2、HNO3、H2O,其中H2O的质量为3.06g;残留的固体产物是Al2O3,质量为1.02g。计算:
(1)x=_______ (写出计算过程)。
(2)气体产物中n(O2)_______ mol。
(1)x=
(2)气体产物中n(O2)
您最近一年使用:0次
2022-01-12更新
|
4653次组卷
|
7卷引用:2022 年1月浙江省普通高校招生选考科目考试化学试题
2022 年1月浙江省普通高校招生选考科目考试化学试题(已下线)2022年浙江1月高考真题变式题(26-31)(已下线)微专题04 以物质的量为中心的计算-备战2023年高考化学一轮复习考点微专题河南省濮阳市第一高级中学2022-2023学年高三上学期第一次月考化学试题浙江省东阳市横店高级中学2022-2023学年高三上学期10月份检测化学试题(已下线)微专题 化学计算的思想方法(已下线)第03讲 物质的量在化学方程式计算中的应用(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
2 . 联合生产是化学综合利用资源的有效方法。煅烧石灰石反应: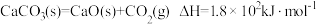 ,石灰石分解需要的能量由焦炭燃烧提供。将石灰石与焦炭按一定比例混合于石灰窑中,连续鼓入空气,使焦炭完全燃烧生成
,石灰石分解需要的能量由焦炭燃烧提供。将石灰石与焦炭按一定比例混合于石灰窑中,连续鼓入空气,使焦炭完全燃烧生成 ,其热量有效利用率为50%。石灰窑中产生的富含
,其热量有效利用率为50%。石灰窑中产生的富含 的窑气通入氨的氯化钠饱和溶液中,40%的
的窑气通入氨的氯化钠饱和溶液中,40%的 最终转化为纯碱。已知:焦炭的热值为
最终转化为纯碱。已知:焦炭的热值为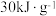 (假设焦炭不含杂质)。请回答:
(假设焦炭不含杂质)。请回答:
(1)每完全分解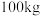 石灰石(含
石灰石(含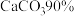 ,杂质不参与反应),需要投料
,杂质不参与反应),需要投料_______ kg焦炭。
(2)每生产106kg纯碱,同时可获得_______ 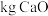 (列式计算)。
(列式计算)。
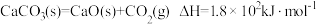 ,石灰石分解需要的能量由焦炭燃烧提供。将石灰石与焦炭按一定比例混合于石灰窑中,连续鼓入空气,使焦炭完全燃烧生成
,石灰石分解需要的能量由焦炭燃烧提供。将石灰石与焦炭按一定比例混合于石灰窑中,连续鼓入空气,使焦炭完全燃烧生成 ,其热量有效利用率为50%。石灰窑中产生的富含
,其热量有效利用率为50%。石灰窑中产生的富含 的窑气通入氨的氯化钠饱和溶液中,40%的
的窑气通入氨的氯化钠饱和溶液中,40%的 最终转化为纯碱。已知:焦炭的热值为
最终转化为纯碱。已知:焦炭的热值为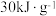 (假设焦炭不含杂质)。请回答:
(假设焦炭不含杂质)。请回答:(1)每完全分解
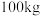 石灰石(含
石灰石(含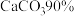 ,杂质不参与反应),需要投料
,杂质不参与反应),需要投料(2)每生产106kg纯碱,同时可获得
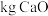 (列式计算)。
(列式计算)。
您最近一年使用:0次
真题
3 . 将3.00g某有机物(仅含C、H、O元素,相对分子质量为150)样品置于燃烧器中充分燃烧,依次通过吸水剂、CO2吸收剂,燃烧产物被完全吸收。实验数据如下表:
请回答:
(1)燃烧产物中水的物质的量为_______ mol。
(2)该有机物的分子式为_______ (写出计算过程)。
| 吸水剂 | CO2吸收剂 | |
| 实验前质量/g | 20.00 | 26.48 |
| 实验后质量/g | 21.08 | 30.00 |
(1)燃烧产物中水的物质的量为
(2)该有机物的分子式为
您最近一年使用:0次
2021-06-15更新
|
3638次组卷
|
13卷引用:2021年6月新高考浙江化学高考真题
2021年6月新高考浙江化学高考真题(已下线)考点27 饮食中的常见的有机物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题18.化学计算-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)2021年6月浙江高考化学试题变式题26-31(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)考点31 研究有机物的一般方法-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题02 阿伏加德罗常数及其化学计算 (练)-2023年高考化学二轮复习讲练测(新高考专用)第二章 物质的量化学实验基本技能 第8讲 化学计算的常用方法(已下线)【知识图鉴】单元讲练测选择性必修3第1单元02基础练(已下线)题型3 以物质的量为中心的相关计算(已下线)考点31 研究有机化合物的一般方法(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第03讲 物质的量在化学方程式计算中的应用(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
4 . 请回答下列问题:
(1)标准状况下,V L氯化氢(HCl)溶解在1 L水中(水的密度近似为1 g/mL)所得溶液的密度为ρ g/mL,则所得盐酸物质的量浓度为_______
(2)将a mol钠和a mol铝一同投入m g足量水中,所得溶液密度为d g·mL-1,该溶液中溶质质量分数为_______
(3)在200 mL氯化镁和氯化铝的混合溶液中,c(Mg2+)为0.2 mol·L-1,c(Cl-)为1.3 mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4 mol·L-1 NaOH溶液的体积为_______
(4)某铁的氧化物(FexO)1.52 g溶于足量盐酸中,向所得溶液中通入112 mL Cl2(标准状况下),恰好将Fe2+完全氧化。x值为_______
(5)向一定量的FeO、Fe、Fe3O4的混合物中加入100 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,放出224 mL(标准状况)的气体,在所得溶液中加入KSCN溶液无血红色出现。若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是_______
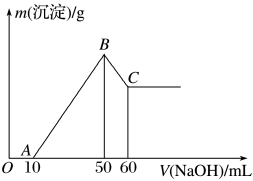
(6)某无色溶液中含有H+、Al3+、Mg2+三种阳离子,逐滴加入0.1 mol·L-1 NaOH溶液,消耗NaOH溶液体积和生成沉淀之间的关系如下图所示。则溶液中H+、Al3+、Mg2+三种阳离子的物质的量浓度之比为_______
(1)标准状况下,V L氯化氢(HCl)溶解在1 L水中(水的密度近似为1 g/mL)所得溶液的密度为ρ g/mL,则所得盐酸物质的量浓度为
(2)将a mol钠和a mol铝一同投入m g足量水中,所得溶液密度为d g·mL-1,该溶液中溶质质量分数为
(3)在200 mL氯化镁和氯化铝的混合溶液中,c(Mg2+)为0.2 mol·L-1,c(Cl-)为1.3 mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4 mol·L-1 NaOH溶液的体积为
(4)某铁的氧化物(FexO)1.52 g溶于足量盐酸中,向所得溶液中通入112 mL Cl2(标准状况下),恰好将Fe2+完全氧化。x值为
(5)向一定量的FeO、Fe、Fe3O4的混合物中加入100 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,放出224 mL(标准状况)的气体,在所得溶液中加入KSCN溶液无血红色出现。若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是
(6)某无色溶液中含有H+、Al3+、Mg2+三种阳离子,逐滴加入0.1 mol·L-1 NaOH溶液,消耗NaOH溶液体积和生成沉淀之间的关系如下图所示。则溶液中H+、Al3+、Mg2+三种阳离子的物质的量浓度之比为

您最近一年使用:0次
2022-04-04更新
|
1306次组卷
|
3卷引用:江苏省天一中学2021-2022学年高一上学期期末考试化学(强化班)试题
江苏省天一中学2021-2022学年高一上学期期末考试化学(强化班)试题(已下线)专题02 阿伏加德罗常数及其化学计算 (测)-2023年高考化学二轮复习讲练测(新高考专用)四川省泸县第四中学2022-2023学年高一上学期第三次月考化学试题
名校
解题方法
5 . 完成下列问题
(1)把盛满 和
和 的混合气体的试管倒立于水中。
的混合气体的试管倒立于水中。
①若一段时间内水上升且充满试管,则原混合气体中 和
和 的体积比是
的体积比是___________ ,若假设生成的溶质不向外扩散,且为标准状况。则所得溶液的物质的量浓度应为___________ 。(保留二位有效数字)
②若一段时间后上升的水只升到试管容积的一半,则剩余的气体为___________ (用化学式表示)。原混合气体中, 和
和 的体积比是
的体积比是___________ 。
(2)二氧化氮和氨气在一定条件下,充分反应,得到非常稳定的产物,其化学方程式为: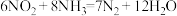 ,若
,若 和
和 的混合气体在一定条件下发生上述反应,已知实际参加反应的
的混合气体在一定条件下发生上述反应,已知实际参加反应的 比
比 少2mL,则原混合气体中
少2mL,则原混合气体中 和
和 的物质的量之比可能为___________。
的物质的量之比可能为___________。
(1)把盛满
 和
和 的混合气体的试管倒立于水中。
的混合气体的试管倒立于水中。①若一段时间内水上升且充满试管,则原混合气体中
 和
和 的体积比是
的体积比是②若一段时间后上升的水只升到试管容积的一半,则剩余的气体为
 和
和 的体积比是
的体积比是(2)二氧化氮和氨气在一定条件下,充分反应,得到非常稳定的产物,其化学方程式为:
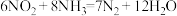 ,若
,若 和
和 的混合气体在一定条件下发生上述反应,已知实际参加反应的
的混合气体在一定条件下发生上述反应,已知实际参加反应的 比
比 少2mL,则原混合气体中
少2mL,则原混合气体中 和
和 的物质的量之比可能为___________。
的物质的量之比可能为___________。| A.3:4 | B.3:2 | C.1:2 | D.3:7。 |
您最近一年使用:0次
解题方法
6 . 现有一瓶常见一元酸形成的铵盐固体,为测定其中的含氮量可以采用“甲醛法”,即: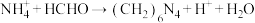 (未配平)。现称取4g该铵盐溶于水,加入足量的甲醛溶液后,再加入水配成100mL溶液。取出5mL,滴入酚酞后再逐滴滴入
(未配平)。现称取4g该铵盐溶于水,加入足量的甲醛溶液后,再加入水配成100mL溶液。取出5mL,滴入酚酞后再逐滴滴入 的NaOH溶液,当滴到25mL时溶液呈粉红色,且在半分钟内不褪色。计算:
的NaOH溶液,当滴到25mL时溶液呈粉红色,且在半分钟内不褪色。计算:
(1)过程中消耗的甲醛物质的量为_______ mol。
(2)该铵盐中氮的质量分数是_______ %。(写出计算过程)
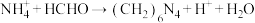 (未配平)。现称取4g该铵盐溶于水,加入足量的甲醛溶液后,再加入水配成100mL溶液。取出5mL,滴入酚酞后再逐滴滴入
(未配平)。现称取4g该铵盐溶于水,加入足量的甲醛溶液后,再加入水配成100mL溶液。取出5mL,滴入酚酞后再逐滴滴入 的NaOH溶液,当滴到25mL时溶液呈粉红色,且在半分钟内不褪色。计算:
的NaOH溶液,当滴到25mL时溶液呈粉红色,且在半分钟内不褪色。计算:(1)过程中消耗的甲醛物质的量为
(2)该铵盐中氮的质量分数是
您最近一年使用:0次
2022-05-19更新
|
896次组卷
|
3卷引用:浙江省Z20名校联盟(名校新高考研究联盟)2022届高三第三次联考化学试题
浙江省Z20名校联盟(名校新高考研究联盟)2022届高三第三次联考化学试题(已下线)专题讲座(一) 化学计算的常用方法(练)-2023年高考化学一轮复习讲练测(全国通用)浙江省Z20名校联盟2022届高三第三次联考化学试题
名校
解题方法
7 . 完成下列问题。
(1)已知完全断裂物质的量均为1mol的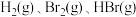 中的化学键时吸收能量分别为
中的化学键时吸收能量分别为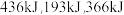 。则在该条件下,
。则在该条件下, 与
与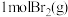 完全反应会
完全反应会_______ (填“吸收”或“放出”)_______  能量。
能量。
(2)将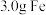 和
和 的混合粉末完全溶于
的混合粉末完全溶于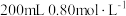 盐酸中,生成标准状况下
盐酸中,生成标准状况下 (假设气体被完全收集);反应后的溶液中滴入2滴
(假设气体被完全收集);反应后的溶液中滴入2滴 溶液后不显血红色。请通过分析计算回答:
溶液后不显血红色。请通过分析计算回答:
①则混合粉末中Fe的物质的量是_______ mol;
②若在反应后的混合液中加入锌,则理论上最多可溶解锌的质量是_______ g。
(1)已知完全断裂物质的量均为1mol的
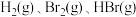 中的化学键时吸收能量分别为
中的化学键时吸收能量分别为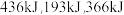 。则在该条件下,
。则在该条件下, 与
与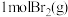 完全反应会
完全反应会 能量。
能量。(2)将
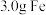 和
和 的混合粉末完全溶于
的混合粉末完全溶于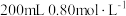 盐酸中,生成标准状况下
盐酸中,生成标准状况下 (假设气体被完全收集);反应后的溶液中滴入2滴
(假设气体被完全收集);反应后的溶液中滴入2滴 溶液后不显血红色。请通过分析计算回答:
溶液后不显血红色。请通过分析计算回答:①则混合粉末中Fe的物质的量是
②若在反应后的混合液中加入锌,则理论上最多可溶解锌的质量是
您最近一年使用:0次
8 .  在不同温度下失水和分解,随着温度升高分别生成
在不同温度下失水和分解,随着温度升高分别生成 ,现称取
,现称取 在敞口容器加热一定时间后,得到
在敞口容器加热一定时间后,得到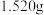 固体,测得生成的
固体,测得生成的 的体积为
的体积为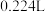 (已折算为标准标况),求:
(已折算为标准标况),求:
(1)固体的成分和物质的量比_______ 。
(2)标准状态下生成 的体积
的体积_______ 。
 在不同温度下失水和分解,随着温度升高分别生成
在不同温度下失水和分解,随着温度升高分别生成 ,现称取
,现称取 在敞口容器加热一定时间后,得到
在敞口容器加热一定时间后,得到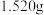 固体,测得生成的
固体,测得生成的 的体积为
的体积为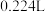 (已折算为标准标况),求:
(已折算为标准标况),求:(1)固体的成分和物质的量比
(2)标准状态下生成
 的体积
的体积
您最近一年使用:0次
9 . 以下方法常用于对废水中的苯酚进行定量测定:取 含苯酚废水,加过量溴水使苯酚完全反应,煮沸,再加入过量
含苯酚废水,加过量溴水使苯酚完全反应,煮沸,再加入过量 溶液生成三溴苯酚,再用
溶液生成三溴苯酚,再用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液 .已知
.已知 (三溴苯酚)
(三溴苯酚) .
. 和
和 溶液颜色均为无色.
溶液颜色均为无色.
(1)消耗 的物质的量为
的物质的量为________ .
(2)废水中苯酚的物质的量浓度为_______ (写出简要计算过程).
 含苯酚废水,加过量溴水使苯酚完全反应,煮沸,再加入过量
含苯酚废水,加过量溴水使苯酚完全反应,煮沸,再加入过量 溶液生成三溴苯酚,再用
溶液生成三溴苯酚,再用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液 .已知
.已知 (三溴苯酚)
(三溴苯酚) .
. 和
和 溶液颜色均为无色.
溶液颜色均为无色.(1)消耗
 的物质的量为
的物质的量为(2)废水中苯酚的物质的量浓度为
您最近一年使用:0次
解题方法
10 . 温度对反应速率的影响可用阿伦尼乌斯公式的一种形式表示: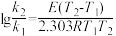 。式中k1、k2分别为温度T1、T2时某反应的速率常数;E为反应的活化能(单位:kJ/mol)(假定活化能在温度变化范围不大时是常数);R为常数8.314,单位J/(mol·K)。又对同一反应,在不同温度下反应速率常数与反应时间的关系如下:
。式中k1、k2分别为温度T1、T2时某反应的速率常数;E为反应的活化能(单位:kJ/mol)(假定活化能在温度变化范围不大时是常数);R为常数8.314,单位J/(mol·K)。又对同一反应,在不同温度下反应速率常数与反应时间的关系如下: 。
。
(1)现知在300K,鲜牛奶5小时后即变酸,但在275K的冰箱里可保存50小时,牛奶变酸反应的活化能是_______ 。
(2)若鲜牛奶存放2.5小时后即变酸,则此时温度为_______ 。
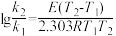 。式中k1、k2分别为温度T1、T2时某反应的速率常数;E为反应的活化能(单位:kJ/mol)(假定活化能在温度变化范围不大时是常数);R为常数8.314,单位J/(mol·K)。又对同一反应,在不同温度下反应速率常数与反应时间的关系如下:
。式中k1、k2分别为温度T1、T2时某反应的速率常数;E为反应的活化能(单位:kJ/mol)(假定活化能在温度变化范围不大时是常数);R为常数8.314,单位J/(mol·K)。又对同一反应,在不同温度下反应速率常数与反应时间的关系如下: 。
。(1)现知在300K,鲜牛奶5小时后即变酸,但在275K的冰箱里可保存50小时,牛奶变酸反应的活化能是
(2)若鲜牛奶存放2.5小时后即变酸,则此时温度为
您最近一年使用:0次



