1 . 如图所示,把试管放入盛有25 ℃石灰水饱和溶液的烧杯中,试管中开始放入几块镁条,再用滴管滴入5 mL的盐酸。试回答下列问题:
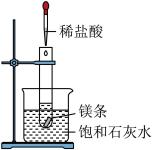
(1)实验中观察到的现象是_______ 。
(2)产生上述实验现象的原因是_______ 。
(3)写出有关的离子方程式:_______ 。
(4)如将本题中“25 ℃石灰水饱和溶液”换成“20 ℃碳酸饮料”进行探究实验,实验(1)中观察到的另一现象是_______ ,其原因是_______ 。

(1)实验中观察到的现象是
(2)产生上述实验现象的原因是
(3)写出有关的离子方程式:
(4)如将本题中“25 ℃石灰水饱和溶液”换成“20 ℃碳酸饮料”进行探究实验,实验(1)中观察到的另一现象是
您最近一年使用:0次
解题方法
2 . 影响化学反应速率的因素很多,某同学设计了以下实验研究不同浓度的硫酸对反应速率的影响。
药品:Cu、Fe、Na和不同浓度的硫酸(0.5mol·L-1、2mol·L-1、18.4mol·L-1);装置如图。

(1)用此装置进行定量实验,应选用的上述实验药品是:
第一组:___________ 和___________ 。
第二组:___________ 和___________ 。
(2)应该测定的实验数据是气体从反应开始到推动活塞达到30mL刻度时的___________ 。
(3)此实验忽视了影响反应速率的其他因素是(假设金属颗粒是均匀的):___________ 。
(4)此实验得到的结论应该是硫酸的浓度越___________ ,反应速率越___________ 。(填“高”“低”“快”“慢”)
药品:Cu、Fe、Na和不同浓度的硫酸(0.5mol·L-1、2mol·L-1、18.4mol·L-1);装置如图。

(1)用此装置进行定量实验,应选用的上述实验药品是:
第一组:
第二组:
(2)应该测定的实验数据是气体从反应开始到推动活塞达到30mL刻度时的
(3)此实验忽视了影响反应速率的其他因素是(假设金属颗粒是均匀的):
(4)此实验得到的结论应该是硫酸的浓度越
您最近一年使用:0次
22-23高一·全国·课时练习
3 . 漂白性—SO2的特性
二氧化硫的漂白性
原理:SO2与有色物质发生化合反应,生成不稳定的无色物质,这些无色物质受热易分解,从而使有色物质恢复原来的颜色。
二氧化硫的漂白性
| 实验操作 | 现象 | 结论 |
| 向实验得到的溶液中滴入1~2滴品红溶液,振荡;加热试管,再观察 | 振荡 加热后 | 二氧化硫能使品红褪色,具有漂白性。 |
您最近一年使用:0次
22-23高三·全国·课时练习
解题方法
4 . 甲、乙、丙三位同学分别用如图所示实验装置及化学药品制取氨。

回答下列问题:
(1)三位同学制取氨的化学方程式为_______ 。
(2)三位同学用向下排空气法收集氨的原因是_______ 。
(3)三位同学用如图所示装置制取氨时,其中有一位同学没有收集到氨(实验操作都正确),没有收集到氨的同学是_______ (填“甲”“乙”或“丙”)。
(4)三位同学都认为他们的实验装置还可用于加热碳酸氢铵固体来制取纯净的氨,能够达到实验目的的是_______ (填“甲”“乙”或“丙”)。

回答下列问题:
(1)三位同学制取氨的化学方程式为
(2)三位同学用向下排空气法收集氨的原因是
(3)三位同学用如图所示装置制取氨时,其中有一位同学没有收集到氨(实验操作都正确),没有收集到氨的同学是
(4)三位同学都认为他们的实验装置还可用于加热碳酸氢铵固体来制取纯净的氨,能够达到实验目的的是
您最近一年使用:0次
解题方法
5 . 写出下列原电池装置中各部分的作用并分析其电极反应和离子移动方向.
原电池装置 | 各部分作用 | 电极反应 | 离子移动方向 |
|  : : : :稀硫酸: | 负极: | |
| 正极: | |||
|  : : : : 溶液: 溶液: 溶液: 溶液:盐桥: | 负极: | |
| 正极: | |||
| 石墨: : : : : 溶液: 溶液: | 负极: | |
| 正极: |
您最近一年使用:0次
解题方法
6 . 某烃在常温下为液体,常用作油漆的溶剂。为测定该烃的分子式,将0.1mol该烃在氧气中完全燃烧,得到的二氧化碳在标准状况下体积为13.44L,得到的水的质量为5.4g。请通过计算写出该烃的分子式_______ 。若该烃不能使溴的四氯化碳溶液和酸性 溶液褪色,试推测该烃的名称并写出其结构简式
溶液褪色,试推测该烃的名称并写出其结构简式_______ 。
 溶液褪色,试推测该烃的名称并写出其结构简式
溶液褪色,试推测该烃的名称并写出其结构简式
您最近一年使用:0次
解题方法
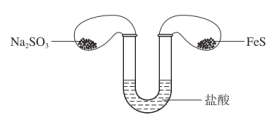
7 . 如下图所示,将两只气球中少量的 和
和 粉末同时倒入足量的盐酸中,写出反应的现象和有关的化学方程式
粉末同时倒入足量的盐酸中,写出反应的现象和有关的化学方程式_______ 。
 和
和 粉末同时倒入足量的盐酸中,写出反应的现象和有关的化学方程式
粉末同时倒入足量的盐酸中,写出反应的现象和有关的化学方程式
您最近一年使用:0次
解题方法
8 . 实验室可以用硫酸和亚硫酸钠反应来制备二氧化硫。写出反应的化学方程式_______ ,画出制备和收集二氧化硫气体的实验装置简图_______ 。
您最近一年使用:0次
22-23高一上·全国·课时练习
名校
9 . X、Y、Z、W、R五种元素的性质或结构信息如表,根据表中的信息回答下列问题:
(1)写出元素R在元素周期表中的位置:_______ 。
(2)由X、Z、R三种元素形成的化合物XRZ的分子式为_______ 。
(3)W与Z的单质在加热条件反应的化学方程式是_______ 。
(4)写出少量X的单质在盛满R的单质的集气瓶中燃烧的现象:_______ ,燃烧片刻后取出燃烧管,迅速将集气瓶倒扣在过量的烧碱溶液中,可能产生的现象是_______ ,所得溶液中存在的溶质除了过量的NaOH外,还含有的是_______ (填化学式)。
| 元素 | X | Y | Z | W | R |
| 性质或 结构信息 | 单质是最轻的气体 | 常见单质为空气中的主要成分之一 | 是海水中质量分数最大的元素 | 原子核内有11个质子 | 原子核外有3个电子层,常见单质为气体 |
(2)由X、Z、R三种元素形成的化合物XRZ的分子式为
(3)W与Z的单质在加热条件反应的化学方程式是
(4)写出少量X的单质在盛满R的单质的集气瓶中燃烧的现象:
您最近一年使用:0次
22-23高一上·全国·课后作业
解题方法
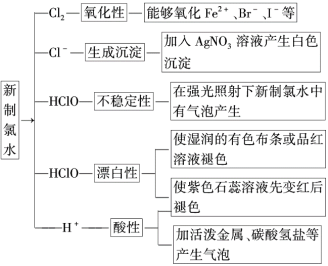
10 . 氯气与水的反应
(1)新制氯水能杀菌、消毒,是因为氯气与H2O反应,反应的化学方程式是_______ :,次氯酸具有强氧化性,能杀菌、消毒。
(2)氯水的成分:
①稳定性:
次氯酸分解反应的化学方程式为_______ 。
②强氧化性:
a.能将有色物质氧化为无色物质,作漂白剂。
b.杀菌、消毒。
③弱酸性:
HClO的酸性比H2CO3弱,向NaClO溶液中通入足量CO2,离子方程式为:_______ 。
(1)新制氯水能杀菌、消毒,是因为氯气与H2O反应,反应的化学方程式是
(2)氯水的成分:

①稳定性:
次氯酸分解反应的化学方程式为
②强氧化性:
a.能将有色物质氧化为无色物质,作漂白剂。
b.杀菌、消毒。
③弱酸性:
HClO的酸性比H2CO3弱,向NaClO溶液中通入足量CO2,离子方程式为:
您最近一年使用:0次






