解题方法
1 . 氢能源是最具前景的应用能源之一,氢气的制备和应用是目前的研究热点。回答下列问题:氨气中氢含量高,可通过氨热分解法制氢气。一定温度下,利用催化剂将 分解为
分解为 和
和 ,反应过程中的能量变化如图所示。
,反应过程中的能量变化如图所示。 键、H-H键分别需要吸收(或放出)945kJ、436kJ的热量,则断开1molN-H吸收的热量为
键、H-H键分别需要吸收(或放出)945kJ、436kJ的热量,则断开1molN-H吸收的热量为_______ kJ。
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:_______ ,在导线中电子流动方向为_______ (用a、b表示)。
②负极反应式为_______ 。
(3)电池工作时, 和
和 连续由外部供给,电池可连续不断提供电能,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
连续由外部供给,电池可连续不断提供电能,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.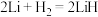
Ⅱ.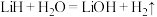
①反应Ⅰ中的还原剂是_______ ,反应Ⅱ中的氧化剂是_______ 。
②金属锂吸收的氢气与放出的氢气的物质的量之比为_______ 。
 分解为
分解为 和
和 ,反应过程中的能量变化如图所示。
,反应过程中的能量变化如图所示。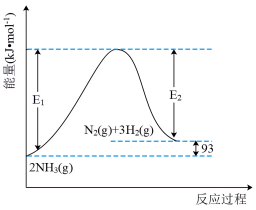
 键、H-H键分别需要吸收(或放出)945kJ、436kJ的热量,则断开1molN-H吸收的热量为
键、H-H键分别需要吸收(或放出)945kJ、436kJ的热量,则断开1molN-H吸收的热量为(2)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
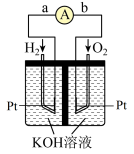
②负极反应式为
(3)电池工作时,
 和
和 连续由外部供给,电池可连续不断提供电能,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
连续由外部供给,电池可连续不断提供电能,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:Ⅰ.
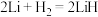
Ⅱ.
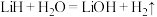
①反应Ⅰ中的还原剂是
②金属锂吸收的氢气与放出的氢气的物质的量之比为
您最近一年使用:0次
2 . 已知反应 。在实验室里,常用如下图所示装置制取并收集氨气。请回答下列问题:
。在实验室里,常用如下图所示装置制取并收集氨气。请回答下列问题:___________ (填字母代号)。
A.向上排空气法 B.向下排空气法
(2)装置与操作:检验氨气是否收集满的方法:___________ (填字母代号)。
A.用湿润的红色石蕊试纸靠近试管口,试纸变蓝,则证明集满
B.用湿润的蓝色石蕊试纸靠近试管口,试纸变红,则证明集满
(3)向氨水中滴加几滴酚酞,溶液呈___________ (填“无色”或“红色”),证明 是
是___________ (填“酸性”或“碱性”)气体。
(4)①欲制取标准状况下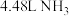 ,至少需要
,至少需要
___________ g。
②实验室制取氨气,还可采用下图中的___________ (填“A”或“B”)。
 。在实验室里,常用如下图所示装置制取并收集氨气。请回答下列问题:
。在实验室里,常用如下图所示装置制取并收集氨气。请回答下列问题:
A.向上排空气法 B.向下排空气法
(2)装置与操作:检验氨气是否收集满的方法:
A.用湿润的红色石蕊试纸靠近试管口,试纸变蓝,则证明集满
B.用湿润的蓝色石蕊试纸靠近试管口,试纸变红,则证明集满
(3)向氨水中滴加几滴酚酞,溶液呈
 是
是(4)①欲制取标准状况下
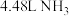 ,至少需要
,至少需要
②实验室制取氨气,还可采用下图中的

您最近一年使用:0次
名校
解题方法
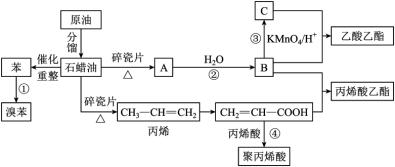
3 . 很多重要的工业原料来源于石油化工,结合下图回答有关问题:______ 。
(2)丙烯酸中碳原子杂化方式为______ ,含氧官能团的名称为______ 。
(3)写出下列反应的反应类型:②______ 、③______
(4)B、C的沸点大小关系:B______ C(填>、=或<),原因是____________ 。
(5)写出下列反应的化学方程式:
丙烯酸+B→丙烯酸乙酯:__________________ 。
反应④:__________________ 。
(6)H与C互为同系物,且H比C多2个 ,H共有
,H共有______ 种结构(不考虑立体异构)。
(2)丙烯酸中碳原子杂化方式为
(3)写出下列反应的反应类型:②
(4)B、C的沸点大小关系:B
(5)写出下列反应的化学方程式:
丙烯酸+B→丙烯酸乙酯:
反应④:
(6)H与C互为同系物,且H比C多2个
 ,H共有
,H共有
您最近一年使用:0次
4 . 如图所示,先在小烧杯中加入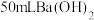 溶液,再滴入几滴酚酞溶液,接通电源,可观察到小灯泡变亮.
溶液,再滴入几滴酚酞溶液,接通电源,可观察到小灯泡变亮.
(1)从物质类别看, 属于
属于____________ ;小灯泡变亮的原因是____________ .
(2)向小烧杯中滴加 溶液,观察到以下现象,按要求填写产生对应现象的原因:
溶液,观察到以下现象,按要求填写产生对应现象的原因:
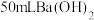 溶液,再滴入几滴酚酞溶液,接通电源,可观察到小灯泡变亮.
溶液,再滴入几滴酚酞溶液,接通电源,可观察到小灯泡变亮.
(1)从物质类别看,
 属于
属于(2)向小烧杯中滴加
 溶液,观察到以下现象,按要求填写产生对应现象的原因:
溶液,观察到以下现象,按要求填写产生对应现象的原因:| 序号 | 现象 | 产生该现象的原因 |
| 1 | 酚酞颜色变浅直至褪去 | 用离子方程式表达:① |
| 2 | 产生白色沉淀 | 用离子方程式表达:② |
| 3 | 小灯泡变暗直至熄灭 | 文字表达:③ |
| 4 | 小灯泡又变亮 | 用电离方程式表达:④ |
您最近一年使用:0次
5 . 实验室需配制 的
的 溶液,请回答下列问题:
溶液,请回答下列问题:
(1)需用托盘天平称取 固体的总质量为
固体的总质量为_______ g。
(2)在此溶液的配制过程中,有以下基本实验步骤,其中只需进行一次的操作是_______ (填序号)。
①称量(用托盘天平) ②溶解 ③转移 ④洗涤 ⑤定容 ⑥摇匀
(3)配制 的
的 溶液用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需要用到的玻璃仪器有
溶液用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需要用到的玻璃仪器有_______ 、_______ 。
(4)配制 的
的 溶液,配制过程中所涉及的下列相关操作正确的是
溶液,配制过程中所涉及的下列相关操作正确的是_______ 。
 的
的 溶液,请回答下列问题:
溶液,请回答下列问题:(1)需用托盘天平称取
 固体的总质量为
固体的总质量为(2)在此溶液的配制过程中,有以下基本实验步骤,其中只需进行一次的操作是
①称量(用托盘天平) ②溶解 ③转移 ④洗涤 ⑤定容 ⑥摇匀
(3)配制
 的
的 溶液用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需要用到的玻璃仪器有
溶液用到的玻璃仪器除量筒、烧杯、玻璃棒外,还需要用到的玻璃仪器有(4)配制
 的
的 溶液,配制过程中所涉及的下列相关操作正确的是
溶液,配制过程中所涉及的下列相关操作正确的是a.  b.
b. 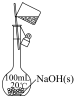 c.
c. 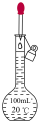 d.
d.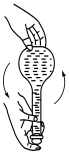
A.用蒸馏水溶解 固体后,立即转入容量瓶中 固体后,立即转入容量瓶中 |
B.称量 固体时,将药品和砝码放反了 固体时,将药品和砝码放反了 |
| C.定容时俯视刻度线 |
| D.定容后发现溶液的凹液面最低点高于刻度线,用胶头滴管将多余的液体吸出 |
您最近一年使用:0次
解题方法
6 . 小明同学用如图所示装置制备氢氧化铁胶体(部分夹持装置已略去)。
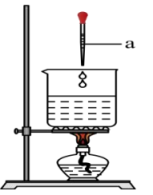
根据所学知识回答下列问题:
(1)仪器a的名称为___________ 。
(2)氢氧化铁胶体的制备:
①烧杯中发生反应的化学方程式为___________ ,反应类型为___________ (填基本反应类型)。
②证明有 胶体生成的方法是
胶体生成的方法是___________ 。(写出具体操作步骤)
③若小明同学制备出的液体呈浑浊状,则可能造成的原因是___________ (任写一种)。
(3)写出下列反应的离子方程式:
①锌和稀盐酸反应制氢气:___________ 。
②大理石和稀盐酸反应制 :
:___________ 。

根据所学知识回答下列问题:
(1)仪器a的名称为
(2)氢氧化铁胶体的制备:
①烧杯中发生反应的化学方程式为
②证明有
 胶体生成的方法是
胶体生成的方法是③若小明同学制备出的液体呈浑浊状,则可能造成的原因是
(3)写出下列反应的离子方程式:
①锌和稀盐酸反应制氢气:
②大理石和稀盐酸反应制
 :
:
您最近一年使用:0次
名校
解题方法
7 . 图是氮循环的一部分:
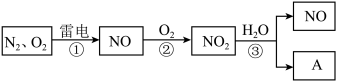
(1)通常状况下,NO2的颜色是_______ 。
(2)反应②的化学方程式是_______ 。
(3)NO2易溶于水,并与水发生化学反应。该反应中,还原剂是_______ 。
(4)化合物A的化学式是_______ 。
(5)治理汽车尾气的一种方法是用催化剂使NO与CO发生反应: 。当生成1molN2时,被氧化的CO为
。当生成1molN2时,被氧化的CO为_______ mol。

(1)通常状况下,NO2的颜色是
(2)反应②的化学方程式是
(3)NO2易溶于水,并与水发生化学反应。该反应中,还原剂是
(4)化合物A的化学式是
(5)治理汽车尾气的一种方法是用催化剂使NO与CO发生反应:
 。当生成1molN2时,被氧化的CO为
。当生成1molN2时,被氧化的CO为
您最近一年使用:0次
8 .  可用于制取
可用于制取 和
和 ,实验室制取纯净、干燥的
,实验室制取纯净、干燥的 的装置如下图。
的装置如下图。
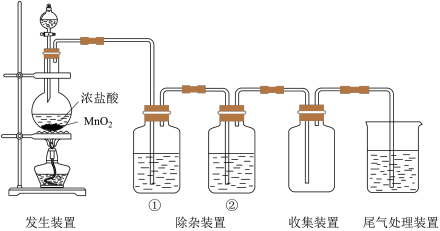
(1)实验室制取 的化学方程式是
的化学方程式是_______ 。
(2)除杂装置①中的试剂是_______ 。
(3)实验室加热 和
和 的固体混合物制取
的固体混合物制取 ,同时生成
,同时生成 ,反应中
,反应中 是催化剂,化学方程式是
是催化剂,化学方程式是_______ 。
 可用于制取
可用于制取 和
和 ,实验室制取纯净、干燥的
,实验室制取纯净、干燥的 的装置如下图。
的装置如下图。
(1)实验室制取
 的化学方程式是
的化学方程式是(2)除杂装置①中的试剂是
(3)实验室加热
 和
和 的固体混合物制取
的固体混合物制取 ,同时生成
,同时生成 ,反应中
,反应中 是催化剂,化学方程式是
是催化剂,化学方程式是
您最近一年使用:0次
解题方法
9 . 填空
(1)断开气态物质中1mol某种共价键生成气态原子需要吸收的能量称为键能(kJ·mol−1)。如表所示是一些共价键的键能。
根据上表的数据,在合成1mol氨_____ (“放出”或“吸收”)的热量为_____ kJ。
(2)在2L容器中投入2molSO2和bmolO2,下图是部分反应物与生成物随时间的变化曲线。
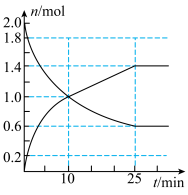
①10min时v(正)_____ v(逆)(填“大于”或“小于”或“等于”);0~10min内,v(SO3)=_____ 。
②平衡时,SO2的转化率为_____ 。
③下列条件能够加快反应速率的是_____ 。
A.升高温度
B.保持压强不变,充入He使容积增大
C.保持体积不变,充入He使压强增大
D.充入一定量的氧气
④下列情况能说明该反应达到化学平衡的是_____ 。
A.v(SO3)=v(SO2)
B.混合气体的密度保持不变
C.t时刻,体系的温度不再发生改变
D.混合气体的总物质的量不再改变
E.SO2、O2、SO3的物质的量之比达到2∶1∶2
(1)断开气态物质中1mol某种共价键生成气态原子需要吸收的能量称为键能(kJ·mol−1)。如表所示是一些共价键的键能。
| 共价键 | H-H | N≡N | N-H |
| 键能(kJ·mol-1) | 436 | 946 | 391 |
(2)在2L容器中投入2molSO2和bmolO2,下图是部分反应物与生成物随时间的变化曲线。

①10min时v(正)
②平衡时,SO2的转化率为
③下列条件能够加快反应速率的是
A.升高温度
B.保持压强不变,充入He使容积增大
C.保持体积不变,充入He使压强增大
D.充入一定量的氧气
④下列情况能说明该反应达到化学平衡的是
A.v(SO3)=v(SO2)
B.混合气体的密度保持不变
C.t时刻,体系的温度不再发生改变
D.混合气体的总物质的量不再改变
E.SO2、O2、SO3的物质的量之比达到2∶1∶2
您最近一年使用:0次
名校
解题方法
10 . 晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用过量的碳还原二氧化硅制得粗硅,同时得到一种可燃性气体;
②粗硅与干燥的HCl气体反应制得 (
(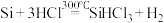 );
);
③ 与过量的
与过量的 在1100℃的温度下反应制得纯硅,已知
在1100℃的温度下反应制得纯硅,已知 能与水剧烈反应,在空气中易自燃。
能与水剧烈反应,在空气中易自燃。
(1)第一步制取粗硅反应的化学方程式为__________ 。
(2)实验室用 与过量的
与过量的 反应制取纯硅装置如图所示(加热和夹持装置略去):
反应制取纯硅装置如图所示(加热和夹持装置略去):

①装置B中的试剂是__________ ,装置C中的烧杯需要加热,目的是__________ 。
②装置D中发生反应的化学方程式是__________ 。
①高温下用过量的碳还原二氧化硅制得粗硅,同时得到一种可燃性气体;
②粗硅与干燥的HCl气体反应制得
 (
(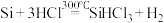 );
);③
 与过量的
与过量的 在1100℃的温度下反应制得纯硅,已知
在1100℃的温度下反应制得纯硅,已知 能与水剧烈反应,在空气中易自燃。
能与水剧烈反应,在空气中易自燃。(1)第一步制取粗硅反应的化学方程式为
(2)实验室用
 与过量的
与过量的 反应制取纯硅装置如图所示(加热和夹持装置略去):
反应制取纯硅装置如图所示(加热和夹持装置略去):
①装置B中的试剂是
②装置D中发生反应的化学方程式是
您最近一年使用:0次



