1 . 已知830℃时,可逆反应CO2(g)+H2(g) CO(g)+H2O(g)ΔH>0的平衡常数K=1。T℃下,在2L恒容密闭容器中,加入0.4mol CO2和0.8molH2,随着反应的进行,测得H2O(g)的物质的量浓度随时间变化如下表所示。
CO(g)+H2O(g)ΔH>0的平衡常数K=1。T℃下,在2L恒容密闭容器中,加入0.4mol CO2和0.8molH2,随着反应的进行,测得H2O(g)的物质的量浓度随时间变化如下表所示。
关于该反应,下列说法正确的是
 CO(g)+H2O(g)ΔH>0的平衡常数K=1。T℃下,在2L恒容密闭容器中,加入0.4mol CO2和0.8molH2,随着反应的进行,测得H2O(g)的物质的量浓度随时间变化如下表所示。
CO(g)+H2O(g)ΔH>0的平衡常数K=1。T℃下,在2L恒容密闭容器中,加入0.4mol CO2和0.8molH2,随着反应的进行,测得H2O(g)的物质的量浓度随时间变化如下表所示。| t/min | 0 | 10 | 20 | 30 | 40 | 70 | 90 |
| c/(mol·L-1) | 0 | 0.04 | 0.07 | 0.09 | 0.10 | 0.12 | 0.12 |
| A.T<830 |
| B.20~40min内,v(H2)=1.5×10-2mol·L-1·min-1 |
| C.平衡后,仅增大压强,CO的体积分数将增大 |
| D.若向容器中充入0.8 mol CO2和1.6molH2,反应达到平衡的时间小于70min |
您最近一年使用:0次
2022-01-15更新
|
146次组卷
|
2卷引用:河北省定州市2021-2022学年高二上学期期末考试化学试题
2 . 某同学将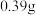 钾投入
钾投入 溶液中待其充分反应。下列叙述错误的是
溶液中待其充分反应。下列叙述错误的是
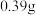 钾投入
钾投入 溶液中待其充分反应。下列叙述错误的是
溶液中待其充分反应。下列叙述错误的是A.反应后的溶液中 的数目约为 的数目约为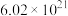 |
| B.反应过程中没有白色沉淀生成 |
C.反应后的溶液中,溶质只有 |
D.生成标准状况下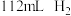 |
您最近一年使用:0次
名校
3 . 马来酸(用H2B表示)是一种二元弱酸,25°C时,某混合溶液中c(H2B) +c(HB-) +c(B2-) = 0.1mol·L-1,测得H2B、HB-、B2-及OH-等离子的pC(pC=-lgc)随溶液pH的变化关系如图所示。下列说法正确的是
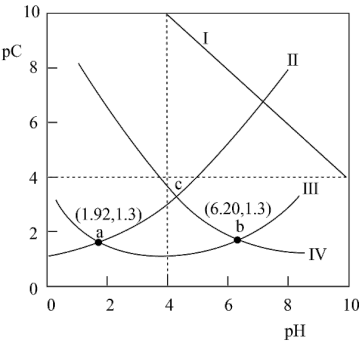

| A.该温度下,马来酸的电离平衡常数Ka1 =10-1.92 |
B.当溶液中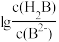 =2时,pH=3.15 =2时,pH=3.15 |
| C.pH=7时,溶液中c(B2-)>c(H2B) >c(HB- ) >c(OH - ) |
D.混合溶液中c(HB-) = 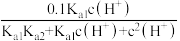 |
您最近一年使用:0次
2022-01-14更新
|
433次组卷
|
3卷引用:山东省潍坊市2021-2022学年高三上学期期末统考化学试题
解题方法
4 . 溴分子易极化,使分子内溴原子分别带部分正电荷和部分负电荷。在一定条件 下CH2=CH-CH=CH2与Br2 发生加成反应会得到两种产物,且两种产物可通过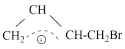 互相转化,反应历程可表示为:
互相转化,反应历程可表示为:
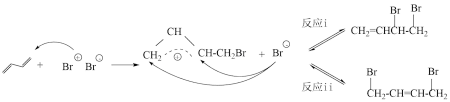
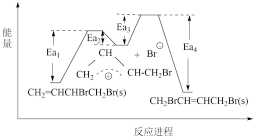
CH2 =CHCHBrCH2Br与CH2BrCH =CHCH2Br相互转化的能量变化如下图所示。已知,同一反应在不同温度下反应速率常数与活化能的关系如下: (其中R为常数)。下列叙述错误的是
(其中R为常数)。下列叙述错误的是
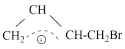 互相转化,反应历程可表示为:
互相转化,反应历程可表示为:
CH2 =CHCHBrCH2Br与CH2BrCH =CHCH2Br相互转化的能量变化如下图所示。已知,同一反应在不同温度下反应速率常数与活化能的关系如下:
 (其中R为常数)。下列叙述错误的是
(其中R为常数)。下列叙述错误的是
| A.相同条件下,反应i的速率比反应ii快 |
| B.升高反应温度,更有利于CH2 = CHCHBrCH2Br的生成 |
| C.反应CH2 =CHCHBrCH2Br(s) →CH2BrCH =CHCH2Br(s)的ΔH=Ea4 +Ea2-Ea1 –Ea3 |
| D.相同条件下,反应达平衡后产物中CH2 BrCH = CHCH2Br含量更大 |
您最近一年使用:0次
解题方法
5 . 如图所示是以TiO2光电极作辅助电极,以Na2S4溶液和NaI溶液为初始电解液组成的二次电池,充电时TiO2光电极受光激发产生电子和空穴,空穴作用下NaI转化为NaI3。下列说法正确的是
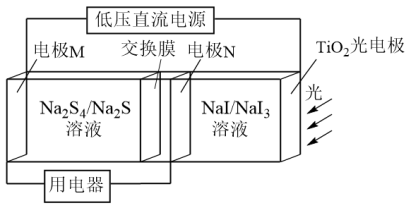

A.放电时M极的电极反应式: 4S2- -6e- =S |
| B.充电时生成1mol NaI3,理论上有2mol Na +转移到M电极室 |
C.放电时TiO2光电极产生的电子转移给I |
| D.充电过程中光能直接转化为电能 |
您最近一年使用:0次
解题方法
6 . 甲醇与SO3生成硫酸氢甲酯的反应为CH3OH(g)+SO3(g)  CH3OSO3H(g)。在无水和有水条件下的部分反应历程如图所示,其“…”表示粒子间的静电作用,下列说法错误的是
CH3OSO3H(g)。在无水和有水条件下的部分反应历程如图所示,其“…”表示粒子间的静电作用,下列说法错误的是
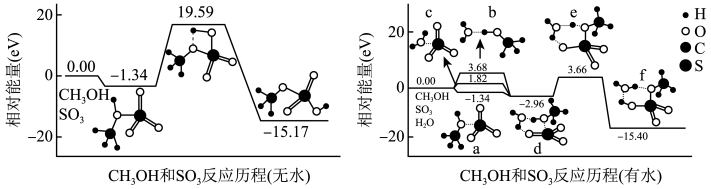
 CH3OSO3H(g)。在无水和有水条件下的部分反应历程如图所示,其“…”表示粒子间的静电作用,下列说法错误的是
CH3OSO3H(g)。在无水和有水条件下的部分反应历程如图所示,其“…”表示粒子间的静电作用,下列说法错误的是
| A.a分子比c分子更稳定 |
| B.水将反应的最高能垒由19.59 eV降为3.66 eV |
| C.有水条件下会降低总反应的焓变 |
| D.d 到f转化的实质为质子转移 |
您最近一年使用:0次
解题方法
7 . 酸性水系锌锰电池在放电时存在电极上MnO2的剥落,会造成电池效率“损失”。最新研究表明,向体系中加入少量KI固体后能使电池持续大电流放电,提高电池的工作效率,原理如图所示,下列说法错误的是


| A.加入KI降低了正极反应的活化能 |
B.I-与剥落的MnO2反应生成的I 能恢复“损失”的能量 能恢复“损失”的能量 |
| C.放电时,正极区溶液的pH减小 |
| D.放电时,消耗1 mol Zn时,正极区电解质溶液增重87 g |
您最近一年使用:0次
解题方法
8 . 下列有关电池的说法中错误的是
| A.原电池放电过程中,负极发生氧化反应 |
| B.原电池工作时电子从负极出发,经外电路流向正极,再从正极经电解液回到负极构成闭合回路 |
C.某燃料电池用熔融碳酸盐作电解质,两极分别通入CO和O2,则通入CO的一极为负极,电极反应式为CO+2e-+CO =2CO2 =2CO2 |
| D.根据自发氧化还原反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑设计的原电池,可以是常温下用铁和铝作电极,用氢氧化钠溶液作电解质溶液 |
您最近一年使用:0次
9 . 下列应用涉及的化学原理正确的是
| 选项 | 应用 | 化学原理 |
| A | 干冰用于人工降雨 | 干冰升华吸热使水蒸气凝结 |
| B | 外接电流的阴极保护法用于钢铁管道防腐 | 阳极材料组成元素的金属性强于铁 |
| C | 小苏打溶液用于中和溅在皮肤上的盐酸 | 小苏打可与盐酸反应且生成的NaCl对皮肤无伤害 |
| D | KSCN溶液用于检验溶液中的 |  与 与 生成红色沉淀 生成红色沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 卤代烃在乙醇中进行溶解反应的机理如图所示(R表示烃基)。下列说法错误的是
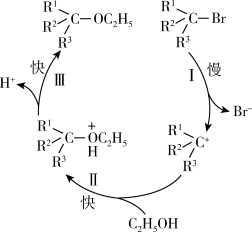
| A.步骤Ⅰ是总反应的决速步骤 |
| B.总反应属于取代反应 |
C. 是总反应的催化剂,能降低反应的活化能 是总反应的催化剂,能降低反应的活化能 |
| D.反应过程中氧原子的成键数目保持不变 |
您最近一年使用:0次
2022-01-09更新
|
275次组卷
|
4卷引用:河北省张家口市2021-2022学年高三上学期期末考试化学试题



