名校
1 . 下列物质在水溶液中的电离方程式书写正确的是
A. | B.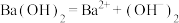 |
C. | D.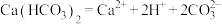 |
您最近一年使用:0次
2 . 用铁泥(主要成分为Fe2O3,还含有少量FeO和Fe)制备纳米Fe3O4的流程如下。下列说法正确的是

| A.步骤②④发生的反应均为氧化还原反应 |
| B.步骤②中发生的反应为2Fe3++Fe = 3Fe2+、Fe+2H+ = Fe2++H2↑ |
| C.步骤④中使用过量的H2O2有利于提高纳米Fe3O4产率 |
| D.纳米Fe3O4能产生丁达尔效应 |
您最近一年使用:0次
3 . 下列化学方程式中,不可以用 表示的是
表示的是
 表示的是
表示的是A. | B.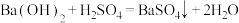 |
C.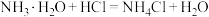 | D.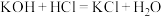 |
您最近一年使用:0次
4 . 下列变化中,需加入还原剂才能进行反应的是
A.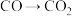 | B.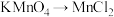 | C. | D.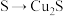 |
您最近一年使用:0次
名校
5 . 将amol钠和amol铝一同投入mg足量水中,所得溶液密度为dg·mL-1,该溶液中溶质的质量分数和物质的量浓度为分别
| A.8200a/(46+m)% | B.11800a/(46+m)% |
| C.1000ad/(46+m)mol/L | D.1000ad/(46+2m)mol/L |
您最近一年使用:0次
6 . 固体化合物X由3种元素组成。某学习小组进行了如下实验:

| A.由现象1得出化合物X含有O元素 | B.X的化学式Na2CuO2 |
| C.固体混合物Y的成分是Cu和NaOH | D.若X与浓盐酸反应产生黄绿色气体,则反应中X作还原剂 |
您最近一年使用:0次
名校
7 . 同温同压下,等质量的SO2与SO3相比较,下列叙述不正确的
| A.含分子个数比为5∶4 | B.含氧原子个数比为5∶6 |
| C.含原子个数为3∶4 | D.含硫元素质量比为4∶5 |
您最近一年使用:0次
8 . 铁在地壳中含量丰富,也是重要的人体微量元素之一。下列有关说法正确的是
| A.铁与水蒸气反应生成氢氧化铁和氢气 |
| B.为了防止缺铁性贫血,麦片中可以添加微量的还原铁粉 |
| C.将饱和FeCl3溶液滴入沸水中,小心加热后制得红褐色Fe(OH)3胶体 |
| D.取新鲜菠菜切开表皮,在内部组织上滴加KSCN溶液,无颜色变化说明菠菜不含铁 |
您最近一年使用:0次
名校
解题方法
9 . 根据下列实验操作和现象所得结论不正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 在小烧杯中滴有少量水,加入20gBa(OH)2·8H2O晶体和10gNH4Cl晶体,用玻璃棒快速搅拌并触摸烧杯外壁,发现烧杯外壁很冷 | Ba(OH)2·8H2O与NH4Cl的反应为吸热反应 |
| B | 将Fe(NO3)2样品溶于稀硫酸后,滴加KSCN溶液,溶液变红 | Fe(NO3)2已变质 |
| C | 用3mL稀盐酸与过量Zn反应,当气泡稀少时,加入1mL浓盐酸,又迅速产生较多气泡 | 盐酸浓度增大,反应速率加快 |
| D | 向5mL0.1mol·L-1FeCl3溶液中滴入0.1 mol·L-1KI溶液5~6滴,加2mLCCl4振荡,静置后取上层清液滴加KSCN溶液,溶液变红 | Fe3+与I-的反应有一定限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为 )恢复了磁性。“钴酞菁”分子结构和性质与人体内的血红素及植物体内的叶绿素非常相似。下列说法中正确的是
)恢复了磁性。“钴酞菁”分子结构和性质与人体内的血红素及植物体内的叶绿素非常相似。下列说法中正确的是
 )恢复了磁性。“钴酞菁”分子结构和性质与人体内的血红素及植物体内的叶绿素非常相似。下列说法中正确的是
)恢复了磁性。“钴酞菁”分子结构和性质与人体内的血红素及植物体内的叶绿素非常相似。下列说法中正确的是| A.其分子直径比氯离子小 | B.在水中形成的分散系属于悬浊液 |
| C.在水中形成的分散系具有丁达尔效应 | D.“钴酞菁”分子能透过滤纸 |
您最近一年使用:0次



