名校
1 . 下列有关能量转化的说法中正确的是
| A.Na与H2O的反应属于放热反应 |
| B.“H—Cl→H+Cl”过程中放出热量 |
| C.干冰升华过程放出热量 |
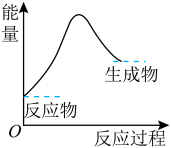
D.反应“C+H2O(g) CO+H2”中的能量变化可以用如图表示 CO+H2”中的能量变化可以用如图表示 |
您最近一年使用:0次
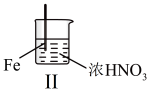
2 . 在通风橱中进行下列实验:
下列说法不正确的是
|
| |
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,很快停止 |
| A.对比Ⅰ、Ⅱ中的现象,说明稀硝酸的氧化性强于浓硝酸 |
| B.Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应 |
| C.过量的铁与稀硝酸反应生成三价铁盐 |
| D.Ⅰ中气体由无色变红棕色的化学方程式为2NO+O2=2NO2 |
您最近一年使用:0次
3 . 世界瓷都-泉州德化盛产陶瓷,下列说法不正确的是
| A.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点 |
| B.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐 |
| C.国产C919用到的氮化硅陶瓷是传统无机非金属材料 |
| D.高品质的瓷器晶莹剔透,属于纯净物 |
您最近一年使用:0次
4 . 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测,质子交换膜只允许 通过,下列说法错误的是
通过,下列说法错误的是
 通过,下列说法错误的是
通过,下列说法错误的是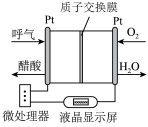
A. 在电池工作时向 在电池工作时向 所在的铂电极移动 所在的铂电极移动 |
B.电子由呼气的铂电极经电解质溶液流向 所在的铂电极 所在的铂电极 |
| C.微处理器通过检测电流大小而计算出被测气体中酒精的含量 |
D.呼气中的酒精分子在 电极被还原为醋酸分子 电极被还原为醋酸分子 |
您最近一年使用:0次
5 . 实验室可用干燥的氯气与亚氯酸钠 固体反应来制备
固体反应来制备 ,装置如图所示,已知
,装置如图所示,已知 常温下为黄绿色气体,熔点
常温下为黄绿色气体,熔点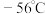 ,沸点
,沸点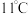 ,极易溶于水且不与水反应,高浓度的
,极易溶于水且不与水反应,高浓度的 受热时易爆炸,下列说法正确的是
受热时易爆炸,下列说法正确的是
 固体反应来制备
固体反应来制备 ,装置如图所示,已知
,装置如图所示,已知 常温下为黄绿色气体,熔点
常温下为黄绿色气体,熔点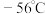 ,沸点
,沸点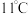 ,极易溶于水且不与水反应,高浓度的
,极易溶于水且不与水反应,高浓度的 受热时易爆炸,下列说法正确的是
受热时易爆炸,下列说法正确的是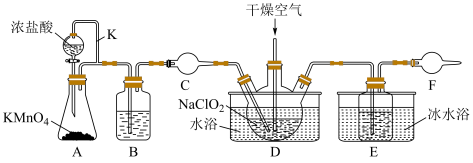
| A.导气管K的作用是平衡气压,保证液体顺利流下 |
| B.C和F中可选用同一种物质 |
C.D中通入一定量的干燥空气,目的主要是将生成的 带入到E中,便于收集. 带入到E中,便于收集. |
D.D中发生的化学反应中氧化剂与还原剂的物质的量之比为 |
您最近一年使用:0次
解题方法
6 . 已知在 、
、 下,
下, 分解生成
分解生成 和
和 的能量变化如图所示.下列说法正确的是
的能量变化如图所示.下列说法正确的是
 、
、 下,
下, 分解生成
分解生成 和
和 的能量变化如图所示.下列说法正确的是
的能量变化如图所示.下列说法正确的是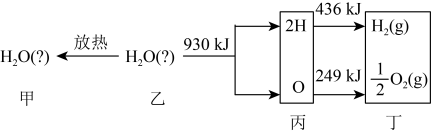
| A.甲为气态水,乙为液态水 |
| B.甲、乙、丙、丁中物质所具有的能量大小关系为丙>丁>乙>甲 |
C.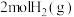 和 和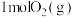 完全反应生成气态水,放出 完全反应生成气态水,放出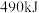 热量 热量 |
D.形成 中的化学键需吸收 中的化学键需吸收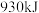 的能量 的能量 |
您最近一年使用:0次
7 . 钠离子电池主要依靠钠离子在正极和负极之间移动来工作,具有安全性能高,充电速度快等优点。一种以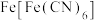 为正极材料的新型可充电钠离子电池的工作原理如图。下列说法错误的是
为正极材料的新型可充电钠离子电池的工作原理如图。下列说法错误的是
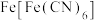 为正极材料的新型可充电钠离子电池的工作原理如图。下列说法错误的是
为正极材料的新型可充电钠离子电池的工作原理如图。下列说法错误的是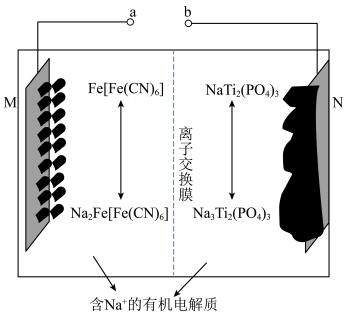
| A.充电时,电极电势:M<N |
B.放电时, 通过离子交换膜从右室移向左室 通过离子交换膜从右室移向左室 |
C.充电时,阳极反应式为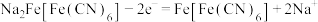 |
D.若初始两电极质量相等,当转移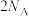 个电子时,两电极质量差为46g 个电子时,两电极质量差为46g |
您最近一年使用:0次
解题方法
8 . X、Y、Z、W是原子序数依次增大的四种短周期元素,最外层电子数之和为17。Y是地壳中含量最多的元素,X、Y形成的某种化合物可表示为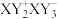 ,Z最外层电子数与K层电子数相等。下列说法错误的是
,Z最外层电子数与K层电子数相等。下列说法错误的是
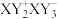 ,Z最外层电子数与K层电子数相等。下列说法错误的是
,Z最外层电子数与K层电子数相等。下列说法错误的是| A.简单离子半径:X>Y>Z | B.X、Y都能与Z形成离子键 |
| C.最简单氢化物的稳定性:W>X | D.Y的最简单氢化物的空间结构是直线形 |
您最近一年使用:0次
9 . W、X、Y、Z均为短周期元素,它们可以形成离子化合物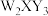 ,W和Y两种元素可以生成
,W和Y两种元素可以生成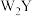 和
和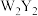 两种化合物,X元素的氢化物和它的某种氧化物反应,可以生成固态单质和水.Z是形成化合物种类最多的元素.下列说法正确的是
两种化合物,X元素的氢化物和它的某种氧化物反应,可以生成固态单质和水.Z是形成化合物种类最多的元素.下列说法正确的是
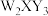 ,W和Y两种元素可以生成
,W和Y两种元素可以生成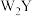 和
和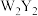 两种化合物,X元素的氢化物和它的某种氧化物反应,可以生成固态单质和水.Z是形成化合物种类最多的元素.下列说法正确的是
两种化合物,X元素的氢化物和它的某种氧化物反应,可以生成固态单质和水.Z是形成化合物种类最多的元素.下列说法正确的是A.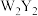 与Z的最高价氧化物反应,生成的产物中存在极性键、非极性键和离子键 与Z的最高价氧化物反应,生成的产物中存在极性键、非极性键和离子键 |
| B.同周期元素中,X的最高价氧化物的水化物酸性最强 |
| C.简单氢化物的稳定性Y大于Z |
D.W、X、Y的原子半径由大到小的顺序是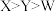 |
您最近一年使用:0次
名校
10 . 铜—锌原电池装置如图所示,电解质溶液为硫酸铜溶液,电池工作一段时间后,下列说法错误的是
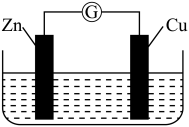
| A.锌电极上的反应为Zn-2e-=Zn2+ |
B.溶液中的 向铜电极移动 向铜电极移动 |
| C.电子从锌电极经过硫酸铜溶液流向铜电极 |
| D.铜电极质量增加 |
您最近一年使用:0次