名校
解题方法
1 . 下列反应均有氢氧化钠生成。回答下列问题:
①Na2O+H2O=2NaOH;
②2Na2O2+2H2O=4NaOH+O2↑;
③2Na+2H2O=2NaOH+H2↑;
④NaH+H2O=NaOH+H2↑。
(1)O2与O3互为__ 。
(2)不属于氧化还原反应的是__ (填方程式序号,下同),同一元素发生氧化还原反应的是__ 。
(3)根据②可推断Na2O2的用途为__ 。
(4)将③改为离子方程式:__ 。
(5)反应④中氧化剂是__ (填化学式,下同),还原产物是__ 。
(6)配平下面这个方程式:__ 。
H2S+ HNO3(浓)= S+ NO2+ H2O
①Na2O+H2O=2NaOH;
②2Na2O2+2H2O=4NaOH+O2↑;
③2Na+2H2O=2NaOH+H2↑;
④NaH+H2O=NaOH+H2↑。
(1)O2与O3互为
(2)不属于氧化还原反应的是
(3)根据②可推断Na2O2的用途为
(4)将③改为离子方程式:
(5)反应④中氧化剂是
(6)配平下面这个方程式:
H2S+ HNO3(浓)= S+ NO2+ H2O
您最近一年使用:0次
名校
解题方法
2 . 有一瓶溶液只含Cl-、CO 、SO
、SO 、Na+、Mg2+、Cu2+六种离子中的某几种,分别取试样于甲、乙、丙三支试管中,进行如下实验:
、Na+、Mg2+、Cu2+六种离子中的某几种,分别取试样于甲、乙、丙三支试管中,进行如下实验:
Ⅰ.甲试管中加入过量的NaOH溶液,有白色沉淀产生;
Ⅱ.乙试管中加BaCl2溶液有沉淀产生;
回答下列问题:
(1)根据(Ⅰ)实验现象可推知,原溶液中一定含有的离子是__ ,请简述判断含该离子的依据:__ (用离子方程式表示),一定不含有的离子是__ 。
(2)根据(Ⅱ)实验现象可推知,原溶液中一定含有的离子是__ 。
(3)由上述实验无法确定的离子是__ 。
 、SO
、SO 、Na+、Mg2+、Cu2+六种离子中的某几种,分别取试样于甲、乙、丙三支试管中,进行如下实验:
、Na+、Mg2+、Cu2+六种离子中的某几种,分别取试样于甲、乙、丙三支试管中,进行如下实验:Ⅰ.甲试管中加入过量的NaOH溶液,有白色沉淀产生;
Ⅱ.乙试管中加BaCl2溶液有沉淀产生;
回答下列问题:
(1)根据(Ⅰ)实验现象可推知,原溶液中一定含有的离子是
(2)根据(Ⅱ)实验现象可推知,原溶液中一定含有的离子是
(3)由上述实验无法确定的离子是
您最近一年使用:0次
名校
3 . 某同学在探究废干电池内的黑色固体回收利用时,进行如图所示实验:

普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。请回答以下问题:
(1)填写标号仪器的名称Ⅰ:__ 。
(2)操作②玻璃棒的作用是__ ;操作②中有一处明显错误请改正__ 。
(3)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为__ (填化学式)。
(4)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为__ (填化学式)。
(5)该同学要对滤液的成分进行检验,以确认是否含有Cl-,下面是他做实验后所写的实验报告,请你写出其空白处的内容:

普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。请回答以下问题:
(1)填写标号仪器的名称Ⅰ:
(2)操作②玻璃棒的作用是
(3)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为
(4)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为
(5)该同学要对滤液的成分进行检验,以确认是否含有Cl-,下面是他做实验后所写的实验报告,请你写出其空白处的内容:
| 实验目的 | 操作 | 实验现象 | 结论 |
| 检验Cl- | 取少许滤液于试管中,加入 | 含有Cl- |
您最近一年使用:0次
名校
解题方法
4 . 下列指定反应的离子方程式正确的是
A.NaHSO4溶液中滴加少量Ba(OH)2溶液:2HSO +Ba2+=Ba(HSO4)2 +Ba2+=Ba(HSO4)2 |
| B.澄清石灰水中通入少量CO2:Ca2++2OH-+CO2=CaCO3↓+H2O |
C.向NaOH溶液中通入过量CO2:2OH-+CO2=CO +H2O +H2O |
| D.向CuSO4溶液加入过量铁粉:3Cu2++2Fe=2Fe3++3Cu |
您最近一年使用:0次
名校
5 . 下列从混合物中分离出其中的一种成分,所采取的分离方法正确的是
| A.对含Ca2+、Mg2+的自来水,可采取沉淀法得到蒸馏水 |
| B.水和酒精的混合物,可用蒸馏的方法,使含水的酒精变为无水酒精 |
| C.要提取碘水中的碘,可用四氯化碳萃取后,分离出下层,再采用蒸馏法得到 |
| D.可用冷却结晶的方法从热的含少量KNO3的NaCl溶液中分离得到纯净的NaCl |
您最近一年使用:0次
名校
解题方法
6 . 将50mL0.1mol•L-1K2SO4溶液加水稀释到100mL,稀释后溶液中K+的物质的量浓度为
| A.0.15mol•L-1 | B.0.05mol•L-1 | C.0.1mol•L-1 | D.0.2mol•L-1 |
您最近一年使用:0次
7 . 已知氧化性:Cl2>Br2>Fe3+>I2,向FeCl2、FeBr2和FeI2的混合液中通入少量Cl2,首先被氧化的是
| A.Cl- | B.Br- | C.Fe2+ | D.I- |
您最近一年使用:0次
8 . 用NA表示阿伏加德罗常数的值。下列判断错误的是
| A.28gN2含有的氮原子数目为2NA |
| B.标准状况下,22.4LCl2含有的原子数目为2NA |
| C.1molNa变为Na+时失去的电子数目为NA |
| D.1 mol∙L−1的K2CO3溶液中含有的K+数目为2NA |
您最近一年使用:0次
名校
9 . 下列反应中,电子转移的方向和数目正确的是
A.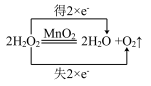 |
B.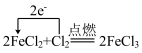 |
C.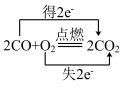 |
D.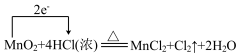 |
您最近一年使用:0次
2021-12-03更新
|
141次组卷
|
4卷引用:内蒙古乌兰浩特第一中学2021-2022学年高一上学期期中考试化学试题
名校
解题方法
10 . 下列说法正确的是
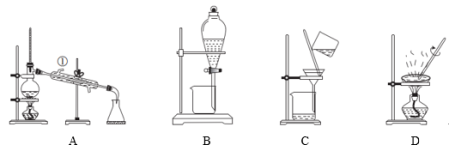

| A.装置A可用于实验室制取蒸馏水,从①处通入冷却水 |
| B.装置B可用于分离苯和水,且苯层由分液漏斗的上口倒出 |
| C.装置C可用于除去固体NaOH中的Ba(OH)2 |
| D.装置D可用于CuSO4溶液蒸发结晶获得CuO |
您最近一年使用:0次



