名校
解题方法
1 . 如图,通过工业联产可有效解决多晶硅(Si)生产中副产物SiCl4.所带来的环境问题。
(1)
反应①的化学方程式为_______ 。
(2)流程中涉及的化学反应属于氧化还原反应的有_______ (填反应序号)。
(3)高温下,反应④的化学方程式为_______ 。
(4)Si和Ge属于同主族元素。下列预测合理的是_______(填选项序号)。
岩脑砂中元素的测定
准确称取xg岩脑砂,与足量的氧化铜混合加热(发生的反应为: ),利用下列装置测定岩脑砂中氮元素和氯元素的质量之比。
),利用下列装置测定岩脑砂中氮元素和氯元素的质量之比。_______ 。
(6)若装置Ⅰ增重yg,利用装置K测得气体体积为VL(已经换算成标准状况),在读取气体体积时,需要a.将气体冷却;b.视线与凹液面最低处相平;c._______ 。
(7)则岩脑砂中
_______ (用代数式表示,不必化简)。若去掉J装置,则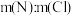 比正确值
比正确值_______ (填“偏高”“偏低”或“无影响”)。
(1)

反应①的化学方程式为
(2)流程中涉及的化学反应属于氧化还原反应的有
(3)高温下,反应④的化学方程式为
(4)Si和Ge属于同主族元素。下列预测合理的是_______(填选项序号)。
| A.Ge与H2化合难于 Si |
| B.GeO2既有氧化性又有还原性 |
| C.酸性H2GeO3>H2SiO3 |
| D.Si和Ge 都可做半导体材料 |
岩脑砂中元素的测定
准确称取xg岩脑砂,与足量的氧化铜混合加热(发生的反应为:
 ),利用下列装置测定岩脑砂中氮元素和氯元素的质量之比。
),利用下列装置测定岩脑砂中氮元素和氯元素的质量之比。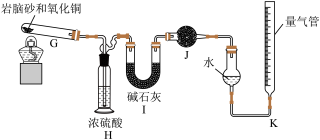
(6)若装置Ⅰ增重yg,利用装置K测得气体体积为VL(已经换算成标准状况),在读取气体体积时,需要a.将气体冷却;b.视线与凹液面最低处相平;c.
(7)则岩脑砂中

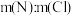 比正确值
比正确值
您最近一年使用:0次
2 . 氮是生物体的重要组成元素,也是维持高等动植物生命活动的必需元素。研究氮的循环和转化对生产和生活有重要的价值。
Ⅰ.某工厂用氨制硝酸和铵盐的流程如图所示。_______ 。实验室固+固制备氨气的化学方程式是_______ 。
(2)同温同压下,理论上设备1与设备2中消耗空气的体积比为___ 。
Ⅱ.氨氮废水的处理是当前科学研究的热点问题。氨氮废水中的氮元素多以 和
和 的形式存在。某工厂处理氨氮废水的流程如图2所示:
的形式存在。某工厂处理氨氮废水的流程如图2所示:_____ 。
(4)过程2的产物均为无毒物质,反应后含氮元素、氯元素的产物化学式分别为_______ 、_______ 。
(5)含余氯废水的主要成分是NaClO以及HClO。X可选用_______(填序号)
(6)为防止环境污染,以下装置(除⑤标明外,其余盛放的液体均为水)可用于吸收多余氨气的是_______ (填序号)。
Ⅰ.某工厂用氨制硝酸和铵盐的流程如图所示。
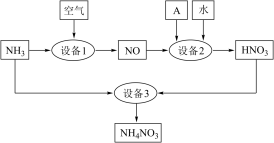
(2)同温同压下,理论上设备1与设备2中消耗空气的体积比为
Ⅱ.氨氮废水的处理是当前科学研究的热点问题。氨氮废水中的氮元素多以
 和
和 的形式存在。某工厂处理氨氮废水的流程如图2所示:
的形式存在。某工厂处理氨氮废水的流程如图2所示:
(4)过程2的产物均为无毒物质,反应后含氮元素、氯元素的产物化学式分别为
(5)含余氯废水的主要成分是NaClO以及HClO。X可选用_______(填序号)
| A.KOH | B. | C. | D.NaCl |
(6)为防止环境污染,以下装置(除⑤标明外,其余盛放的液体均为水)可用于吸收多余氨气的是

您最近一年使用:0次
名校
3 . 过多的NOx排放,往往会产生污染。某研究性小组探究 与炽热的铜粉反应,设计如下
与炽热的铜粉反应,设计如下 能被酸性高锰酸钾溶液氧化成NO
能被酸性高锰酸钾溶液氧化成NO ,此体系中产生的NO
,此体系中产生的NO 浓度较稀。
浓度较稀。
(1)实验开始前,检查装置气密性涉及到以下操作,给出合理的操作顺序:_______ 。
将F中的长导管插入液面以下→_______→_______→_______→_______→_______(操作可重复使用)。
①关闭弹簧夹a,打开弹簧夹b ②观察F中的现象 ③用酒精灯加热A中三颈烧瓶 ④撤走酒精灯
(2)写出A中反应的化学方程式_______ 。装置B的作用是_______ 。
(3)反应一段时间后,装置D中铜粉变黑,写出装置D中发生反应的化学方程式_______ 。
(4)实验过程中,装置E中溶液颜色变浅,则装置E发生的离子方程式为_______ ;
(5)实验前和实验结束时,都需通一段时间的 ,实验结束时目的是
,实验结束时目的是_______ 。
(6)有同学发现装置A溶液呈绿色,而不显蓝色;甲认为是该溶液中硝酸铜质量分数较高所致,而乙认为是该溶液溶解了生成的气体所致。设计方案来判断甲或乙哪种合理,下列方案中不可行 的是_______。
 与炽热的铜粉反应,设计如下
与炽热的铜粉反应,设计如下
 能被酸性高锰酸钾溶液氧化成NO
能被酸性高锰酸钾溶液氧化成NO ,此体系中产生的NO
,此体系中产生的NO 浓度较稀。
浓度较稀。(1)实验开始前,检查装置气密性涉及到以下操作,给出合理的操作顺序:
将F中的长导管插入液面以下→_______→_______→_______→_______→_______(操作可重复使用)。
①关闭弹簧夹a,打开弹簧夹b ②观察F中的现象 ③用酒精灯加热A中三颈烧瓶 ④撤走酒精灯
(2)写出A中反应的化学方程式
(3)反应一段时间后,装置D中铜粉变黑,写出装置D中发生反应的化学方程式
(4)实验过程中,装置E中溶液颜色变浅,则装置E发生的离子方程式为
(5)实验前和实验结束时,都需通一段时间的
 ,实验结束时目的是
,实验结束时目的是(6)有同学发现装置A溶液呈绿色,而不显蓝色;甲认为是该溶液中硝酸铜质量分数较高所致,而乙认为是该溶液溶解了生成的气体所致。设计方案来判断甲或乙哪种合理,下列方案中
| A.加热该绿色溶液,观察颜色变化 |
| B.加水稀释绿色溶液,观察颜色变化 |
| C.向该绿色溶液中通入氮气,观察颜色变化 |
| D.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化某研究性实验小组 |
您最近一年使用:0次
名校
4 . 电视剧中美轮美奂的“仙境”,其中所需的烟雾是在置于温热石棉网上的NH4NO3和Zn粉混合物中滴几滴水后能持续产生白烟,涉及反应: 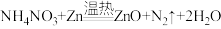 。下列有关说法中错误的是
。下列有关说法中错误的是
| A.上述反应属于氧化还原反应 |
| B.氮气既是氧化产物也是还原反应 |
| C.在标准状况下,11.2LN2中所含电子的物质的量为6mol |
| D.每生成1molZnO共转移5mol电子 |
您最近一年使用:0次
名校
5 . 高锰酸钾生产过程中产生的废锰渣(主要成分为 、
、 和
和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下:
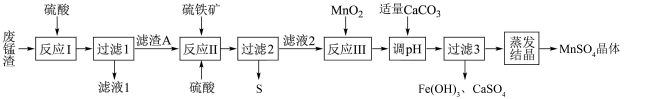
已知:硫铁矿的主要成分为二硫化亚铁( ,杂质不参与反应)。
,杂质不参与反应)。
回答下列问题:
(1)二硫化亚铁中S元素的化合价为_______ 。
(2)①滤渣A的主要成分是_______ (填化学式);
②“反应II”生成 、
、 等物质的离子方程式为
等物质的离子方程式为_______ 。
③“反应III”中还原剂和氧化剂物质的量之比为_______ ;
④“调 ”时,验证
”时,验证 已经沉淀完全的实验操作和现象为
已经沉淀完全的实验操作和现象为_______ 。
 、
、 和
和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下:
已知:硫铁矿的主要成分为二硫化亚铁(
 ,杂质不参与反应)。
,杂质不参与反应)。回答下列问题:
(1)二硫化亚铁中S元素的化合价为
(2)①滤渣A的主要成分是
②“反应II”生成
 、
、 等物质的离子方程式为
等物质的离子方程式为③“反应III”中还原剂和氧化剂物质的量之比为
④“调
 ”时,验证
”时,验证 已经沉淀完全的实验操作和现象为
已经沉淀完全的实验操作和现象为
您最近一年使用:0次
名校
6 . 化工产品中,含氯物质众多,其用途广泛。回答下列问题:
(1)如图为氯及其化合物的“价-类”二维图。缺失的物质B为_______ (填化学式)。

(2)次氯酸钠是一种含氯物质,取含次氯酸钠14.9g/L的“84”消毒液1mL,加水稀释至100mL,则稀释后的溶液中次氯酸钠的物质的量浓度为_______ mol/L。
(3)电石渣[主要成分为Ca(OH)2]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取KClO3的工艺流程如图所示:

已知:Ca(ClO3)2易溶于水。
①“一系列操作”为_______ 、_______ 。
②“转化”发生反应的离子方程式为_______ 。
(1)如图为氯及其化合物的“价-类”二维图。缺失的物质B为

(2)次氯酸钠是一种含氯物质,取含次氯酸钠14.9g/L的“84”消毒液1mL,加水稀释至100mL,则稀释后的溶液中次氯酸钠的物质的量浓度为
(3)电石渣[主要成分为Ca(OH)2]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取KClO3的工艺流程如图所示:

已知:Ca(ClO3)2易溶于水。
①“一系列操作”为
②“转化”发生反应的离子方程式为
您最近一年使用:0次
名校
7 . (I)如表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
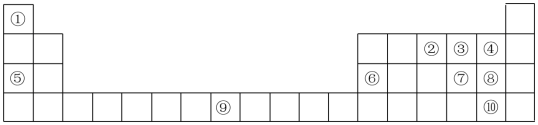
(1)元素②和④的简单氢化物反应生成化合物的电子式为_______ 。
(2)元素⑤和③的单质加热生成产物中含有的化学键类型为_______ 。
(3)元素⑨在周期表中的位置是_______ 。
(II)L、M、N、Q、R、T分别代表上述十种元素之一,其原子半径及主要化合价关系如表:
(4)写出M最高价氧化物对应的水化物与N的最高价含氧酸反应的化学方程式:_______ 。
(5)L、M、Q、R四种元素形成的简单离子半径从大到小的顺序为_______ (用相应的离子符号表示)。

(1)元素②和④的简单氢化物反应生成化合物的电子式为
(2)元素⑤和③的单质加热生成产物中含有的化学键类型为
(3)元素⑨在周期表中的位置是
(II)L、M、N、Q、R、T分别代表上述十种元素之一,其原子半径及主要化合价关系如表:
| 元素代号 | L | M | N | Q | R | T |
| 原子半径/nm | 0.186 | 0.143 | 0.099 | 0.114 | 0.104 | 0.066 |
| 主要化合价 | +1 | +3 | +7、-1 | +7、-1 | +6、-2 | -2 |
(5)L、M、Q、R四种元素形成的简单离子半径从大到小的顺序为
您最近一年使用:0次
名校
解题方法
8 . 铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。黑木耳中含有比较丰富的铁元素,某研究型学习小组同学测定某地黑木耳中铁的含量。
(1)称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。高温灼烧黑木耳,使之完全灰化。将木耳灰用下图流程处理,对滤液中的溶质进行研究。
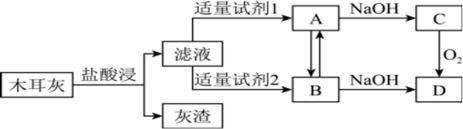
①浸泡液检测不出铁元素的原因是_______ 。
②试剂l应该是_______ 。
(2)A转化为B可加入的试剂有_______ 。
a.酸性高锰酸钾 b.Cl2 c.H2O2溶液
(3)C生成D时的反应现象为_______ 。
(4)已知在酸性条件下Fe2+可被氧气氧化为Fe3+,该反应每转移8mol电子,标准状况下消耗氧气的体积为_______ L。
(1)称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。高温灼烧黑木耳,使之完全灰化。将木耳灰用下图流程处理,对滤液中的溶质进行研究。

①浸泡液检测不出铁元素的原因是
②试剂l应该是
(2)A转化为B可加入的试剂有
a.酸性高锰酸钾 b.Cl2 c.H2O2溶液
(3)C生成D时的反应现象为
(4)已知在酸性条件下Fe2+可被氧气氧化为Fe3+,该反应每转移8mol电子,标准状况下消耗氧气的体积为
您最近一年使用:0次
9 . 下列变化不能直接一步实现的是
A(HCl)→B(Cl2)→C〔Ca(ClO)2〕→D(HClO)→E(CO2)
A(HCl)→B(Cl2)→C〔Ca(ClO)2〕→D(HClO)→E(CO2)
| A.A→B | B.B→C | C.C→D | D.D→E |
您最近一年使用:0次
名校
10 . 中国宇航员已经在太空泡茶了,每个茶装在特制包装袋中,注水后用加热器进行加热就可以喝了,但要插上吸管以防止水珠飘起来,下列说法正确的是
| A.1.8g水中含有原子的物质的量为0.3mol |
| B.宇航员喝茶时注入的H2O的摩尔质量是18g |
| C.在标准状况下,1mol水的体积约是22.4L |
| D.1mol水中含有6.02×1023个H2分子 |
您最近一年使用:0次



