名校
解题方法
1 . 分类法是学习和研究化学的一种重要方法。下列关于 的分类不正确的是
的分类不正确的是
 的分类不正确的是
的分类不正确的是| A.氧化物 | B.钠盐 | C.碳酸盐 | D.正盐 |
您最近一年使用:0次
2 . 下列叙述正确的是
| A.将一块绿豆大小的金属钠加入到CuSO4溶液中,有紫红色的物质析出 |
| B.Cl2有毒,如果出现氯气泄漏,不要向地势低的地方转移 |
| C.钠是银白色金属,熔点低,硬度大 |
| D.在空气中加热时,金属钠剧烈燃烧,生成白色固体 |
您最近一年使用:0次
2023-12-21更新
|
81次组卷
|
2卷引用:内蒙古科尔沁右翼前旗第二中学2023-2024学年高一上学期12月月考化学试题
3 . 下列实验装置不能达到实验目的的是
| ①验证Na和水反应为放热反应 | ②检验Na2O2与H2O反应有O2生成 | ③观察钾元素的焰色 | ④比较Na2CO3、NaHCO3的稳定性 |
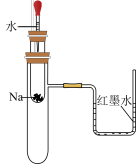 |  | 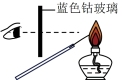 |  |
| A.① | B.② | C.③ | D.④ |
您最近一年使用:0次
2023-12-21更新
|
255次组卷
|
2卷引用:内蒙古科尔沁右翼前旗第二中学2023-2024学年高一上学期12月月考化学试题
4 . 设 为阿伏加德罗常数的值,下列有关说法正确的是
为阿伏加德罗常数的值,下列有关说法正确的是
 为阿伏加德罗常数的值,下列有关说法正确的是
为阿伏加德罗常数的值,下列有关说法正确的是A.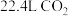 与CO的混合气体中含碳原子数目为 与CO的混合气体中含碳原子数目为 |
B.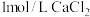 溶液中含离子总数为 溶液中含离子总数为 |
C.标准状况下, 所含有的 所含有的 分子数目为 分子数目为 |
D.2.3g Na与足量氧反应生成 和 和 混合物时电子转移数目为 混合物时电子转移数目为 |
您最近一年使用:0次
2023-12-21更新
|
155次组卷
|
2卷引用:内蒙古科尔沁右翼前旗第二中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
5 . 利用 氧化绿色的
氧化绿色的 浓强碱溶液制备
浓强碱溶液制备 的装置如下图所示(加热、夹持装置略):
的装置如下图所示(加热、夹持装置略):______________________________ 。
(2)如果d中用足量的NaOH溶液吸收多余氯气,写出相应的离子方程式:______________________________ 。
(3)一段时间后,当仪器C中溶液由绿色完全转变为紫红色即停止通氯气。熄灭A处酒精灯,再____________________ ,待冷却后拆除装置。
(4)某同学在实验中发现,若用稀盐酸代替浓盐酸与 混合加热没有氯气生成,欲探究该条件下不能生成氯气的原因,该同学提出下列假设:
混合加热没有氯气生成,欲探究该条件下不能生成氯气的原因,该同学提出下列假设:
假设1: 的浓度不够大;
的浓度不够大;
假设2:____________________ ;
假设3: 和
和 的浓度均不够大。
的浓度均不够大。
设计实验方案,进行实验。在下表中写出实验步骤以及预期现象和结论。(限选实验试剂:蒸馏水、浓 、NaCl固体、
、NaCl固体、 固体、稀盐酸、
固体、稀盐酸、 溶液、淀粉-KI溶液)
溶液、淀粉-KI溶液)
 氧化绿色的
氧化绿色的 浓强碱溶液制备
浓强碱溶液制备 的装置如下图所示(加热、夹持装置略):
的装置如下图所示(加热、夹持装置略):
(2)如果d中用足量的NaOH溶液吸收多余氯气,写出相应的离子方程式:
(3)一段时间后,当仪器C中溶液由绿色完全转变为紫红色即停止通氯气。熄灭A处酒精灯,再
(4)某同学在实验中发现,若用稀盐酸代替浓盐酸与
 混合加热没有氯气生成,欲探究该条件下不能生成氯气的原因,该同学提出下列假设:
混合加热没有氯气生成,欲探究该条件下不能生成氯气的原因,该同学提出下列假设:假设1:
 的浓度不够大;
的浓度不够大;假设2:
假设3:
 和
和 的浓度均不够大。
的浓度均不够大。设计实验方案,进行实验。在下表中写出实验步骤以及预期现象和结论。(限选实验试剂:蒸馏水、浓
 、NaCl固体、
、NaCl固体、 固体、稀盐酸、
固体、稀盐酸、 溶液、淀粉-KI溶液)
溶液、淀粉-KI溶液)实验步骤 | 预期现象与结论 |
步骤1:取少量 稀盐酸于试管A中,加入少量 稀盐酸于试管A中,加入少量 ,滴加几滴浓硫酸,充分振荡,塞紧带导管的胶塞,导管插入淀粉-KI溶液中,加热 ,滴加几滴浓硫酸,充分振荡,塞紧带导管的胶塞,导管插入淀粉-KI溶液中,加热 | ①若淀粉-KI溶液变蓝,则假设1成立 ②若淀粉-KI溶液不变蓝,则假设2或假设3成立 |
步骤2:取少量 稀盐酸于试管B中,加入少量 稀盐酸于试管B中,加入少量 ,加入少量NaCl固体,充分振荡,塞紧带导管的胶塞,导管插入淀粉-KI溶液中,加热 ,加入少量NaCl固体,充分振荡,塞紧带导管的胶塞,导管插入淀粉-KI溶液中,加热 | ①若淀粉-KI溶液变盐,则 ②若淀粉-KI溶液不变蓝,结合步骤1中的结论②,则 |
您最近一年使用:0次
2023-12-20更新
|
45次组卷
|
2卷引用:内蒙古自治区乌兰浩特第一中学2023-2024学年高一上学期第二次月考化学试题
解答题-实验探究题
|
适中(0.65)
|
名校
6 . “84消毒液”能有效杀灭甲型H1N1病毒,某同学购买了一瓶“84”消毒液,该消毒液通常稀释到100倍(体积比)使用,查阅相关资料和消毒液包装说明得到如图信息:
(1)该“84”消毒液NaClO物质的量浓度约为__________  (保留1位小数)。
(保留1位小数)。
(2)某同学欲配制上述浓度的“84”消毒液480ml。请你帮他将下列过程补充完整:
①计算并用托盘大平称量NaClO固体__________ g;
②将称量好的NaClO固体放在烧杯中,加适量蒸馏水,用玻璃棒搅拌,使NaClO全部溶解:
③将烧杯中的溶液沿着玻璃棒注入容量瓶中;
④用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,将洗涤液也都注入容量瓶中,轻轻摇动容量瓶,使溶液混合均匀;
⑤将蒸馏水注入容量瓶中,当液面距离容量瓶颈部的刻度线1~2cm时,改用__________ 滴加蒸馏水至凹液面与刻度线相切,盖好瓶塞,反复上下颠倒,摇匀;
⑥将配好的溶液倒入试剂瓶中,并贴好标签。
(3)在配制过程中,下列操作中能使所配溶液的浓度偏高的有__________ (填序号)。
①用托盘天平称量时物品和砝码放反(托盘天平的最小砝码为1g)
②烧杯中固体溶解后未冷却直接转移定容
③转移前,容量瓶中含有少量蒸馏水
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤定容时,俯视刻度线
(4)“84”消毒液与稀硫酸混合使用可增强消毒能力,请用化学方程式解释其原因:______________________________ 。某消毒小组人员用 的浓硫酸配制
的浓硫酸配制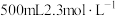 的稀硫酸用于增强“84”消毒液的消毒能力,需取用浓硫酸的体积为
的稀硫酸用于增强“84”消毒液的消毒能力,需取用浓硫酸的体积为__________ mL。
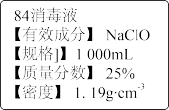
(1)该“84”消毒液NaClO物质的量浓度约为
 (保留1位小数)。
(保留1位小数)。(2)某同学欲配制上述浓度的“84”消毒液480ml。请你帮他将下列过程补充完整:
①计算并用托盘大平称量NaClO固体
②将称量好的NaClO固体放在烧杯中,加适量蒸馏水,用玻璃棒搅拌,使NaClO全部溶解:
③将烧杯中的溶液沿着玻璃棒注入容量瓶中;
④用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,将洗涤液也都注入容量瓶中,轻轻摇动容量瓶,使溶液混合均匀;
⑤将蒸馏水注入容量瓶中,当液面距离容量瓶颈部的刻度线1~2cm时,改用
⑥将配好的溶液倒入试剂瓶中,并贴好标签。
(3)在配制过程中,下列操作中能使所配溶液的浓度偏高的有
①用托盘天平称量时物品和砝码放反(托盘天平的最小砝码为1g)
②烧杯中固体溶解后未冷却直接转移定容
③转移前,容量瓶中含有少量蒸馏水
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤定容时,俯视刻度线
(4)“84”消毒液与稀硫酸混合使用可增强消毒能力,请用化学方程式解释其原因:
 的浓硫酸配制
的浓硫酸配制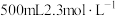 的稀硫酸用于增强“84”消毒液的消毒能力,需取用浓硫酸的体积为
的稀硫酸用于增强“84”消毒液的消毒能力,需取用浓硫酸的体积为
您最近一年使用:0次
名校
7 . 亚硝酸钠( )是一种用途广泛的工业盐,有像食盐一样的外观和咸味,它可将正常的血红蛋白变为高铁血红蛋白,使血红蛋白中的铁元素由二价变为三价,失去携氧能力,美蓝是亚硝酸盐中毒的有效解毒剂。由于
)是一种用途广泛的工业盐,有像食盐一样的外观和咸味,它可将正常的血红蛋白变为高铁血红蛋白,使血红蛋白中的铁元素由二价变为三价,失去携氧能力,美蓝是亚硝酸盐中毒的有效解毒剂。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。回答以下问题:
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。回答以下问题:
(1) 也可作为食品防腐剂,但由于亚硝酸钠具有一定的毒性,因此食品中用量和残留量均有严格规定,可用酸性
也可作为食品防腐剂,但由于亚硝酸钠具有一定的毒性,因此食品中用量和残留量均有严格规定,可用酸性 测定
测定 样品纯度,反应原理如下:
样品纯度,反应原理如下:________
__________ __________
__________ __________=__________
__________=__________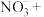 __________
__________ __________
__________ ,请将离子方程式抄写在答题卡上并完成配平。
,请将离子方程式抄写在答题卡上并完成配平。
(2)从物质分类角度来看, 是
是__________ (填字母代号)。
a.酸 b.正盐 c.酸式盐
d.碱 e.电解质 f.非电解质
(3)下列关于中毒与解毒原理中说法正确的是__________(填序号)。
(4)误食 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列__________(填序号)反应中
表现出的性质与下列__________(填序号)反应中 表现出的性质相同。
表现出的性质相同。
(5)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式:______________________________ 。
 )是一种用途广泛的工业盐,有像食盐一样的外观和咸味,它可将正常的血红蛋白变为高铁血红蛋白,使血红蛋白中的铁元素由二价变为三价,失去携氧能力,美蓝是亚硝酸盐中毒的有效解毒剂。由于
)是一种用途广泛的工业盐,有像食盐一样的外观和咸味,它可将正常的血红蛋白变为高铁血红蛋白,使血红蛋白中的铁元素由二价变为三价,失去携氧能力,美蓝是亚硝酸盐中毒的有效解毒剂。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。回答以下问题:
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。回答以下问题:(1)
 也可作为食品防腐剂,但由于亚硝酸钠具有一定的毒性,因此食品中用量和残留量均有严格规定,可用酸性
也可作为食品防腐剂,但由于亚硝酸钠具有一定的毒性,因此食品中用量和残留量均有严格规定,可用酸性 测定
测定 样品纯度,反应原理如下:
样品纯度,反应原理如下:__________
 __________
__________ __________=__________
__________=__________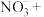 __________
__________ __________
__________ ,请将离子方程式抄写在答题卡上并完成配平。
,请将离子方程式抄写在答题卡上并完成配平。(2)从物质分类角度来看,
 是
是a.酸 b.正盐 c.酸式盐
d.碱 e.电解质 f.非电解质
(3)下列关于中毒与解毒原理中说法正确的是__________(填序号)。
| A.解毒剂美蓝应该具有氧化性 | B.中毒时亚硝酸盐发生氧化反应 |
| C.解毒时高铁血红蛋白被还原 | D.中毒过程中血红蛋白显氧化性 |
 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列__________(填序号)反应中
表现出的性质与下列__________(填序号)反应中 表现出的性质相同。
表现出的性质相同。A. |
B. |
C.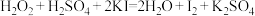 |
D. |
您最近一年使用:0次
名校
8 . 下列离子方程式正确的是
A.用醋酸除去水垢: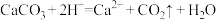 |
B.向 溶液中加过量的 溶液中加过量的 溶液: 溶液: |
C.向饱和 溶液中通入过量 溶液中通入过量 : :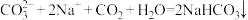 |
D. 溶液与少量的 溶液与少量的 溶液混合: 溶液混合: |
您最近一年使用:0次
2023-12-20更新
|
122次组卷
|
2卷引用:内蒙古自治区乌兰浩特第一中学2023-2024学年高一上学期第二次月考化学试题
名校
9 . 在给定条件的水溶液中能大量共存的离子组是
A.使酚酞变红色的溶液: 、 、 、 、 、 、 |
B.加入 固体的溶液中: 固体的溶液中: 、 、 、 、 、 、 |
C.使紫色石蕊溶液呈红色的溶液: 、 、 、 、 、 、 |
D.含有大量 的溶液: 的溶液: 、 、 、 、 、 、 |
您最近一年使用:0次
2023-12-20更新
|
87次组卷
|
2卷引用:内蒙古自治区乌兰浩特第一中学2023-2024学年高一上学期第二次月考化学试题
名校
解题方法
10 . 下列反应不属于四种基本反应类型,但属于氧化还原反应的是
A.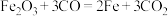 | B. |
C. | D.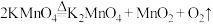 |
您最近一年使用:0次
2023-12-18更新
|
78次组卷
|
7卷引用:内蒙古乌兰浩特市第四中学2022-2023学年高一上学期第一次月考化学试题
内蒙古乌兰浩特市第四中学2022-2023学年高一上学期第一次月考化学试题内蒙古自治区兴安盟乌兰浩特第一中学2023-2024学年高一上学期期中考试化学试题黑龙江省哈尔滨市德强高级中学2022-2023学年高一上学期10月月考化学试题(已下线)专题03 氧化还原反应【考题猜想】(10大题型)-2023-2024学年高一化学上学期期中考点大串讲(人教版2019必修第一册)云南省楚雄东兴中学2023-2024学年高一上学期10月月考化学试题四川省泸州市泸县第四中学2023-2024学年高一下学期开学化学试题福建省永安市第三中学高中校2023-2024学年高一上学期第二次月考化学试题



