名校
解题方法
1 . “打赢蓝天保卫战”,意味着对大气污染防治比过去要求更高。二氧化硫——空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的结合,原理如图所示。下列说法正确的是
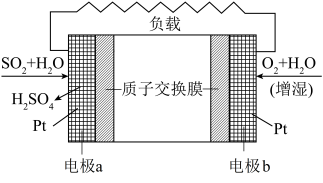

| A.该电池放电时质子从电极b移向电极a |
B.相同条件下,放电过程中消耗的, 和 和 的体积比为2∶1 的体积比为2∶1 |
C.电极a附近发生的电极反应为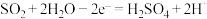 |
D.电极b附近发生的电极反应为 |
您最近一年使用:0次
2023-11-16更新
|
1380次组卷
|
28卷引用:内蒙古阿拉善盟2022-2023学年高一下学期期末考试化学试题
内蒙古阿拉善盟2022-2023学年高一下学期期末考试化学试题山东省济宁市2018届高三第一次模拟考试理综化学试题【全国百强校】甘肃省天水市第一中学2018届高三第三次模拟考试理综化学试题【全国百强校】青海省西宁市第四高级中学2019届高三上学期第二次(10月)模拟考试理科综合化学试题【全国百强校】江西省景德镇市第一中学2018-2019学年高二上学期期中考试化学试题(已下线)专题6.2 原电池 化学电源(讲)——2020年高考化学一轮复习讲练测四川省凉山彝族自治州2019-2020学年高一下学期期末考试化学试题(已下线)第20讲 原电池 化学电源(精讲)——2021年高考化学一轮复习讲练测安徽省郎溪中学、泾县中学2020-2021学年高一下学期3月联考化学试题安徽省合肥市第一中学2020-2021学年高一下学期期中考试化学试题(已下线)课时30 新型原电池装置-2022年高考化学一轮复习小题多维练(全国通用)陕西省绥德中学2020-2021学年高二下学期6月质量检测化学试题四川省南充市白塔中学2020-2021学年高一下学期第二次月考(6月)化学试题吉林省吉林市普通中学2022-2023学年高三第一次调研测试化学试题吉林省吉林市普通中学2022-2023学年高三上学期10月调研化学试题浙江省北斗联盟2022-2023学年高二上学期期中联考化学试题陕西省延安市第一中学2021-2022学年高一下学期期末考试化学试题吉林省延边第二中学2022-2023学年高三上学期10月月考化学试题山西省怀仁市第一中学校云东校区2021-2022学年高二上学期第四次月考理综化学试题福建省莆田第二十四中学2021-2022学年高二下学期开学摸底考试化学(2卷)试题天津市河东区 2022-2023 学年高二上学期期末质量检测化学试题江苏省扬州中学2022-2023学年高二下学期开学摸底考试化学试题(已下线)第六章 化学反应与能量 第35讲 原电池 化学电源天津市实验中学2023-2024学年高三上学期第二次阶段检测化学试题辽宁省辽东南协作校2023-2024学年高二上学期12月月考化学(A卷)试题(已下线)寒假作业08 原电池-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)吉林省梅河口市第五中学2023-2024学年高二上学期12月月考化学试题四川省泸州市泸县第四中学2023-2024学年高二上学期1月期末化学试题
解题方法
2 . 已知烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A能发生下图所示的转化关系。

回答下列问题:
(1)A→B的反应类型是___________ ;
(2)写出B→C的反应方程式___________ ;
(3)F的同分异构体结构简式为___________ ;
(4)已知G是A的同系物,相对分子质量比A大14,请写出由G生成聚合物的反应方程式___________ ;
(5)某实验小组按如图装置制备E,

①写出B和D反应生成E的化学方程式___________ ;
②反应前左试管中加入化学药品的顺序为___________ ;
③在右试管中通常加入___________ 溶液。

回答下列问题:
(1)A→B的反应类型是
(2)写出B→C的反应方程式
(3)F的同分异构体结构简式为
(4)已知G是A的同系物,相对分子质量比A大14,请写出由G生成聚合物的反应方程式
(5)某实验小组按如图装置制备E,

①写出B和D反应生成E的化学方程式
②反应前左试管中加入化学药品的顺序为
③在右试管中通常加入
您最近一年使用:0次
解题方法
3 . 研究碳、氮的氧化物的性质对化工生产和环境保护有重要意义。
(1)现代社会的一切活动都离不开能量,化学反应在发生物质变化的同时伴随能量的变化。下图为1molN2(g)和1molO2(g)充分反应生成2molNO(g)的能量变化图。若断裂1molNO(g)分子中的化学键,需要吸收___________ 能量。该反应中反应物所具有的总能量___________ (填“高于”“低于”或“等于”生成物所具有的总能量。

(2)由下图的能量转化关系可知生成16g CH3OH(l)需要___________ (填“吸收”或“放出”)___________ kJ能量。

(3)CO2催化加氢合成新能源甲醇,既实现了碳资源充分利用,又可有效减少CO2排放。在体积为2L的密闭容器中,充入2molCO2和6molH2,一定条件下发生反应: ,测得CO2(g)和CH3OH(g)的浓度随时间变化如下图所示。
,测得CO2(g)和CH3OH(g)的浓度随时间变化如下图所示。

①在4min到9min时间段,v(H2)=___________ mol·L-1·min-1
②能说明上述反应达到平衡状态的是___________ ;
A.恒温、恒容时,容器内混合气体的密度不再变化
B.反应中CO2与CH3OH的物质的量浓度相等时(即图中交叉点)
C.有2个C=O键断裂的同时,有3个H-H键生成
D.当v正(CO2)=3v逆(H2)
③平衡时H2的物质的量为___________ 。
(4)燃料电池是一种高效、环境友好的供电装置,如有图为CH3OH燃料电池的工作原理示意图,a、b均为情性电极。

①b极的电极反应为:___________ ;
②若此燃料电池电路中转移2mol电子,则消耗的O2在标准状况下的体积为___________ 。
(1)现代社会的一切活动都离不开能量,化学反应在发生物质变化的同时伴随能量的变化。下图为1molN2(g)和1molO2(g)充分反应生成2molNO(g)的能量变化图。若断裂1molNO(g)分子中的化学键,需要吸收

(2)由下图的能量转化关系可知生成16g CH3OH(l)需要

(3)CO2催化加氢合成新能源甲醇,既实现了碳资源充分利用,又可有效减少CO2排放。在体积为2L的密闭容器中,充入2molCO2和6molH2,一定条件下发生反应:
 ,测得CO2(g)和CH3OH(g)的浓度随时间变化如下图所示。
,测得CO2(g)和CH3OH(g)的浓度随时间变化如下图所示。
①在4min到9min时间段,v(H2)=
②能说明上述反应达到平衡状态的是
A.恒温、恒容时,容器内混合气体的密度不再变化
B.反应中CO2与CH3OH的物质的量浓度相等时(即图中交叉点)
C.有2个C=O键断裂的同时,有3个H-H键生成
D.当v正(CO2)=3v逆(H2)
③平衡时H2的物质的量为
(4)燃料电池是一种高效、环境友好的供电装置,如有图为CH3OH燃料电池的工作原理示意图,a、b均为情性电极。

①b极的电极反应为:
②若此燃料电池电路中转移2mol电子,则消耗的O2在标准状况下的体积为
您最近一年使用:0次
4 . 公元前9世纪,二氧化硫就被用于消毒和漂白。实验室可用下列装置(部分夹持仪器略去)制取SO2并验证其性质。

(1)检查装置A、B气密性的操作为:先关闭装置A中分液漏斗活塞和装置B中止水夹K,往长颈漏斗中注水至水柱高于广口瓶液面,若观察到___________ ,则气密性良好;
(2)装置A中反应的化学方程式为___________ ;
(3)实验时,通气一段时间后,C试管中出现大量淡黄色浑浊现象,证明二氧化硫具有___________ (填“还原性”“氧化性”或“漂白性);
(4)实验结束时,关闭止水夹K,装置B所起的作用是___________ ;
(5)取少量试管D中的溶液,加入BaCl2溶液,产生白色沉淀。SO2通入试管D中反应的离子方程式为___________ ;
(6)用如图装置验证 酸性比
酸性比 强。
强。

请从下列试剂中选择合适试剂以完成实验(要求:试剂不重复,填代号):
a.品红溶液 b.酸性KMnO4溶液 c.饱和NaHCO3 d.饱和NaHSO3溶液
X为___________ ,Y为___________ ,Z为___________ 。

(1)检查装置A、B气密性的操作为:先关闭装置A中分液漏斗活塞和装置B中止水夹K,往长颈漏斗中注水至水柱高于广口瓶液面,若观察到
(2)装置A中反应的化学方程式为
(3)实验时,通气一段时间后,C试管中出现大量淡黄色浑浊现象,证明二氧化硫具有
(4)实验结束时,关闭止水夹K,装置B所起的作用是
(5)取少量试管D中的溶液,加入BaCl2溶液,产生白色沉淀。SO2通入试管D中反应的离子方程式为
(6)用如图装置验证
 酸性比
酸性比 强。
强。
请从下列试剂中选择合适试剂以完成实验(要求:试剂不重复,填代号):
a.品红溶液 b.酸性KMnO4溶液 c.饱和NaHCO3 d.饱和NaHSO3溶液
X为
您最近一年使用:0次
解题方法
5 . 已知A、B、C、D、E、F、G是原子序数依次增大的短周期主族元素,已知A的某种原子核内没有中子,A和D,C和F分别为同一主族元素,B原子的最外层电子数比次外层多3,E的最高价氧化物对应的水化物既可以和强酸反应也可以和强碱溶液反应。
(1)C、E分别形成的简单离子中,半径较大的是___________ (填离子符号)
(2)F和G的最高价氧化物对应的水化物酸性较强的是___________ (填化学式)
(3)由A、D、F形成的化合物中化学键的类型为___________ ;
(4)由A、B形成18e-化合物的结构式为___________ ;
(5)用电子式表示C与D形成的原子个数比为1:2的化合物的形成过程___________ ;
(6)D、E的最高价氧化物对应的水化物相互反应的化学方程式为___________ ;
(7)由B、G形成的化合物分子中,B和G原子的最外层均达到8电子稳定结构,该化合物遇水可反应生成一种具有漂白性的化合物,写出反应的化学方程式:___________ 。
(1)C、E分别形成的简单离子中,半径较大的是
(2)F和G的最高价氧化物对应的水化物酸性较强的是
(3)由A、D、F形成的化合物中化学键的类型为
(4)由A、B形成18e-化合物的结构式为
(5)用电子式表示C与D形成的原子个数比为1:2的化合物的形成过程
(6)D、E的最高价氧化物对应的水化物相互反应的化学方程式为
(7)由B、G形成的化合物分子中,B和G原子的最外层均达到8电子稳定结构,该化合物遇水可反应生成一种具有漂白性的化合物,写出反应的化学方程式:
您最近一年使用:0次
6 . 在恒容绝热密闭容器中投入24g焦炭粉、充入 气体发生反应:
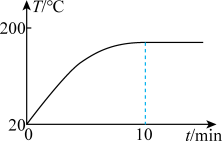
气体发生反应: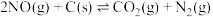 ,测得容器内气体温度与时间关系如图所示。下列推断正确的是
,测得容器内气体温度与时间关系如图所示。下列推断正确的是
 气体发生反应:
气体发生反应: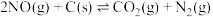 ,测得容器内气体温度与时间关系如图所示。下列推断正确的是
,测得容器内气体温度与时间关系如图所示。下列推断正确的是
| A.混合气体的压强始终保持不变 |
| B.该反应的逆反应是放热反应 |
| C.增大焦炭粉质量,反应速率加快 |
D.10min时,单位时间内消耗1mol 同时消耗2moI 同时消耗2moI |
您最近一年使用:0次
7 . 我国科学家开发新型催化剂(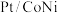 )实现室温下
)实现室温下 和
和 反应生成
反应生成 。向2L恒容密闭容器中充入2.0mol
。向2L恒容密闭容器中充入2.0mol 和1.0mol
和1.0mol ,加入该催化剂,室温下发生反应
,加入该催化剂,室温下发生反应 ,测得
,测得 的物质的量随时间变化如表所示。下列说法正确的是
的物质的量随时间变化如表所示。下列说法正确的是
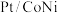 )实现室温下
)实现室温下 和
和 反应生成
反应生成 。向2L恒容密闭容器中充入2.0mol
。向2L恒容密闭容器中充入2.0mol 和1.0mol
和1.0mol ,加入该催化剂,室温下发生反应
,加入该催化剂,室温下发生反应 ,测得
,测得 的物质的量随时间变化如表所示。下列说法正确的是
的物质的量随时间变化如表所示。下列说法正确的是| t/min | 0 | 5 | 10 | 15 | 20 | 25 |
| n/mol | 2.0 | 1.3 | 0.9 | 0.6 | 0.5 | 0.5 |
| A.容器中的元素均位于短周期 | B.5~10min内,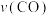 最大 最大 |
C.平衡时 的浓度为1.5mol/L 的浓度为1.5mol/L | D.CO的平衡转化率为75% |
您最近一年使用:0次
8 .  代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是
 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是A.1mol蔗糖完全水解生成的葡萄糖分子数为 |
B.工业上,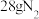 和4mol 和4mol 在高温高压催化剂作用下生成的 在高温高压催化剂作用下生成的 分子数为 分子数为 |
C.标准状况下,11.2L氯仿(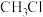 )中含有的极性键数目为 )中含有的极性键数目为 |
D.1molFe溶于过量稀硝酸溶液中,转移电子数为 |
您最近一年使用:0次
9 . 通过下列实验步骤及现象,得出的结论错误的是
| 选项 | 实验步骤及现象 | 实验结论 |
| A | 向某溶液中加入NaOH浓溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝 | 该溶液中一定含有 |
| B | 向某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含 |
| C | 将灼热后表面变黑的螺旋状铜丝伸入约50℃的乙醇中,铜丝能保持红热一段时间 | 乙醇催化氧化反应是放热反应 |
| D | 在0.01mol乙醇中加入过量的金属钠充分反应,收集到标准状况下气体112mL | 乙醇分子中有1个氢原子与氧原子相连,其余与碳原子相连 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 高强度运动会导致肌肉乳酸堆积,产生酸痛感。已知乳酸的结构简式如图所示,关于该有机物的说法错误的是


| A.含有羧基、烃基两种官能团 |
| B.该有机物能与碳酸氢钠反应放出CO2 |
| C.该有机物分子只含极性键和非极性键 |
| D.该有机物能发生酯化反应 |
您最近一年使用:0次



