1 . 氮氧化物会导致光化学烟雾和酸雨,在1Fe³⁺的催化作用下,NH₃可将 NO还原为无污染的气体,反应历程如图,下列说法不正确的是

| A.基态Fe²⁺的价层电子排布式为3d⁶ |
| B.电负性: N>O>H>Fe |
| C.该过程中存在极性键和非极性键的断裂和形成 |
D.图中的总反应可表示为 |
您最近一年使用:0次
解题方法
2 . 《自然》报道了我国科学家利用催化剂通过化学链合成氨。回答下列问题:
(1)NH3可用于制备NaN3、NH₄NO₃,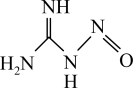 (亚硝基胍)等含氮化合物,基态N的核外电子排布为
(亚硝基胍)等含氮化合物,基态N的核外电子排布为___________ ; NH₄NO₃中 NH 中中心原子的杂化轨道类型为
中中心原子的杂化轨道类型为___________ NO 的空间结构为
的空间结构为___________ ; 亚硝基胍分子中σ键与π键的数目比为___________ 。
(2)N、P位于同一主族,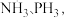 分子结构如图所示:
分子结构如图所示:___________ ,
②NH₃比PH₃的沸点高, 其主要原因是___________ 。
③磷化镓的晶胞结构如下图所示,A点坐标为(0,0,0),B点坐标为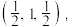 则C点坐标为
则C点坐标为___________ ;
(1)NH3可用于制备NaN3、NH₄NO₃,
 (亚硝基胍)等含氮化合物,基态N的核外电子排布为
(亚硝基胍)等含氮化合物,基态N的核外电子排布为 中中心原子的杂化轨道类型为
中中心原子的杂化轨道类型为 的空间结构为
的空间结构为(2)N、P位于同一主族,
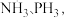 分子结构如图所示:
分子结构如图所示:
②NH₃比PH₃的沸点高, 其主要原因是
③磷化镓的晶胞结构如下图所示,A点坐标为(0,0,0),B点坐标为
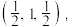 则C点坐标为
则C点坐标为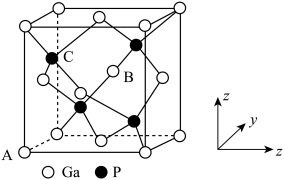
您最近一年使用:0次
解题方法
3 . 硅和碳及其化合物多是新型无机非金属材料。
(1)金刚石属于___________ 晶体,C₆₀属于___________ 晶体,它们都是碳元素的___________ 。
(2)石墨烯是只由一层碳原子所构成的平面薄膜,富勒烯以C₆₀为代表,结构如下图。
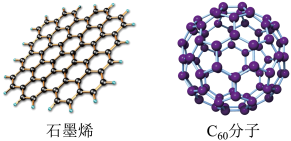
从石墨中剥离得到石墨烯需克服的作用是___________ ;在石墨烯中,每个六元环占有___________ 个C原子。
(3)碳化硅(化学式:SiC)与晶体硅(化学式:Si)和金刚石(化学式:C)相比较,三者熔点从高到低的顺序(用化学式和“>”表示):___________ 。
(4)氮化硅是一种高温陶瓷材料,已知氮化硅的晶体结构中,原子间都以单键相连,且N原子和N原子,Si原子与 Si原子不直接相连,同时每个原子都满足8电子稳定结构,请写出氮化硅的化学式:___________ 。
(5)已知化学键的键能数据如下表:
已知反应热:△H=反应物的总键能之和-生成物的总键能之和。则反应 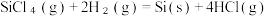 )的△H=
)的△H=___________ kJ/mol。
(1)金刚石属于
(2)石墨烯是只由一层碳原子所构成的平面薄膜,富勒烯以C₆₀为代表,结构如下图。

从石墨中剥离得到石墨烯需克服的作用是
(3)碳化硅(化学式:SiC)与晶体硅(化学式:Si)和金刚石(化学式:C)相比较,三者熔点从高到低的顺序(用化学式和“>”表示):
(4)氮化硅是一种高温陶瓷材料,已知氮化硅的晶体结构中,原子间都以单键相连,且N原子和N原子,Si原子与 Si原子不直接相连,同时每个原子都满足8电子稳定结构,请写出氮化硅的化学式:
(5)已知化学键的键能数据如下表:
| 化学键 | Si-Cl | H-H | H-Cl | Si-Si |
| 键能 kJ/mol | 360 | 436 | 431 | 176 |
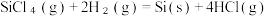 )的△H=
)的△H=
您最近一年使用:0次
解题方法
4 . 研究元素周期表右上角区域元素,有利于研发新型绿色农药,如 等。
等。
 和
和 的混合气体经光解作用可生成一种新分子
的混合气体经光解作用可生成一种新分子
①
 中S
中S 键。
键。②下列分子中属于非极性分子的是
a. b.
b. c.
c. d.
d.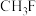 e.
e.
 、
、 中沸点较高的是
中沸点较高的是(3)下列物质变化,只与范德华力有关的是
A.干冰熔化 B.乙酸汽化 C.乙醇与HCHO混溶
D. 溶于水 E.碘溶于四氯化碳
溶于水 E.碘溶于四氯化碳
 。推测酸性:
。推测酸性:
 。
。(5)最近我国某科研团队用磷化钴纳米片催化合成氧化偶氯、偶氯、胺类芳香化合物,反应原理为
 。
。P与N属于同主族元素,但是 不能稳定存在的原因
不能稳定存在的原因
您最近一年使用:0次
5 . 某多孔储氢材料前驱体结构如图,M、W、X、Y、Z五种短周期元素原子序数依次增大,基态Z原子的电子填充了3个能级,其中有2个未成对电子。下列叙述正确的是
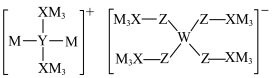
A. 的沸点低于 的沸点低于 的沸点,因为 的沸点,因为 的相对质量较小 的相对质量较小 |
| B.Y的氧化物对应的水化物一定是强酸 |
| C.第一电离能:Z>Y>X>W |
| D.简单氢化物的沸点:Z>Y>X |
您最近一年使用:0次
解题方法
6 . 偶氨苯作为光开关,可对外部刺激作出响应。其结构简式如图所示。下列分析错误的是
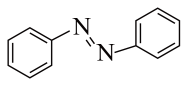
| A.根据“相似相溶”原理判断该物质可能与苯互溶 |
| B.分子中所有原子可能处于同一平面上 |
| C.1mol偶氮苯含2mol极性共价键 |
D.分子中C和N原子均采用 杂化方式 杂化方式 |
您最近一年使用:0次
解题方法
7 . X、Y、Z、M、Q、R皆为前20号元素,其原子半径与化合价的关系如图所示。下列说法错误的是
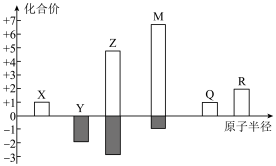
| A.QX只存在离子键 | B.Z的氢化物可形成非极性键 |
| C.简单离子半径:Q>M>R | D.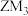 各原子最外层均达到8电子稳定结构 各原子最外层均达到8电子稳定结构 |
您最近一年使用:0次
解题方法
8 . 咪唑( )是生产抗真菌药物的主要原料之一,下列说法错误的是
)是生产抗真菌药物的主要原料之一,下列说法错误的是
| A.咪唑分子为极性分子 | B.分子中C-N键的极性小于N-H键的极性 |
C.分子中 键与 键与 键个数比为9∶2 键个数比为9∶2 | D.咪唑中两个N原子均为 杂化 杂化 |
您最近一年使用:0次
9 . 不同元素的原子在分子内吸引电子的能力大小可用一定数值 来表示,
来表示, 值越大,其原子吸引电子的能力越强,在所形成的分子中为带负电荷的一方。下表是某些元素的
值越大,其原子吸引电子的能力越强,在所形成的分子中为带负电荷的一方。下表是某些元素的 值:
值:
(1)通过分析 值的变化规律,确定N、Mg的
值的变化规律,确定N、Mg的 值范围:
值范围:
___________ < (Mg)<
(Mg)<___________ ;___________ < (N)<
(N)<___________ 。
(2)如果 值为电负性的数值,试推断
值为电负性的数值,试推断 中化学键的类型为
中化学键的类型为___________ 。(填“离子键”、“共价键”)
(3)预测元素周期表中 值最小的元素是
值最小的元素是___________ (放射性元素除外)
(4)某有机化合物的结构为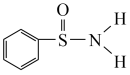 ,其中S-N键中,你认为共用电子对偏向
,其中S-N键中,你认为共用电子对偏向___________ (填元素符号)。
(5)推测 值与原子半径的关系为
值与原子半径的关系为___________ 。
 来表示,
来表示, 值越大,其原子吸引电子的能力越强,在所形成的分子中为带负电荷的一方。下表是某些元素的
值越大,其原子吸引电子的能力越强,在所形成的分子中为带负电荷的一方。下表是某些元素的 值:
值:| 元素符号 | Li | Be | B | C | O | F |
 值 值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 |
| 元素符号 | Na | Al | Si | P | S | Cl |
 值 值 | 0.93 | 1.60 | 1.90 | 2.19 | 2.55 | 3.16 |
(1)通过分析
 值的变化规律,确定N、Mg的
值的变化规律,确定N、Mg的 值范围:
值范围: (Mg)<
(Mg)< (N)<
(N)<(2)如果
 值为电负性的数值,试推断
值为电负性的数值,试推断 中化学键的类型为
中化学键的类型为(3)预测元素周期表中
 值最小的元素是
值最小的元素是(4)某有机化合物的结构为
 ,其中S-N键中,你认为共用电子对偏向
,其中S-N键中,你认为共用电子对偏向(5)推测
 值与原子半径的关系为
值与原子半径的关系为
您最近一年使用:0次
解题方法
10 . 磷化硼(BP)是一种超硬耐磨涂层材料,其结构与金刚石类似,晶胞结构如图所示,设晶胞参数为 apm,下列说法不正确的是


| A.基态磷原子的核外电子运动状态有 15种 |
B.P与B原子的最近距离为 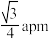 |
| C.与P原子最近的等距离的P原子有 12个 |
D.该晶体的密度为 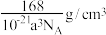 |
您最近一年使用:0次



