名校
1 . 下列有关电解质溶液说法正确的是
| A.用同浓度的NaOH溶液分别中和等体积等pH的盐酸和醋酸溶液,盐酸消耗的NaOH溶液体积多 |
B.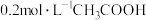 溶液与 溶液与 溶液等体积混合后存在: 溶液等体积混合后存在: |
C.常温下,已知 的 的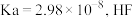 的 的 ,则等浓度等体积的 ,则等浓度等体积的 和 和 溶液,前者所含离子总数比后者小 溶液,前者所含离子总数比后者小 |
D.粗铜精炼中,电解质溶液中 浓度始终不变 浓度始终不变 |
您最近一年使用:0次
名校
2 . 研究物质结构对学习化学有重要意义。下列选项正确的是
①酸性: ,是因为
,是因为 的电负性大于
的电负性大于 的电负性,使
的电负性,使 的羧基中O-H的极性更大
的羧基中O-H的极性更大
②金刚石、 晶体的熔点依次降低
晶体的熔点依次降低
③同周期,与 元素未成对电子数相等的元素有3种
元素未成对电子数相等的元素有3种
④ 与
与 分子极性相同,是因为二者都是由非极性键构成的分子
分子极性相同,是因为二者都是由非极性键构成的分子
⑤沸点:对羟基苯甲醛>邻羟基苯甲醛
⑥元素 位于周期表第四周期ⅣA族,核外电子排布式为
位于周期表第四周期ⅣA族,核外电子排布式为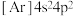 ,属于
,属于 区
区
⑦配合物 中配位原子是
中配位原子是
⑧在 中的溶解度:
中的溶解度: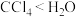
①酸性:
 ,是因为
,是因为 的电负性大于
的电负性大于 的电负性,使
的电负性,使 的羧基中O-H的极性更大
的羧基中O-H的极性更大②金刚石、
 晶体的熔点依次降低
晶体的熔点依次降低③同周期,与
 元素未成对电子数相等的元素有3种
元素未成对电子数相等的元素有3种④
 与
与 分子极性相同,是因为二者都是由非极性键构成的分子
分子极性相同,是因为二者都是由非极性键构成的分子⑤沸点:对羟基苯甲醛>邻羟基苯甲醛
⑥元素
 位于周期表第四周期ⅣA族,核外电子排布式为
位于周期表第四周期ⅣA族,核外电子排布式为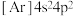 ,属于
,属于 区
区⑦配合物
 中配位原子是
中配位原子是
⑧在
 中的溶解度:
中的溶解度: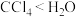
| A.①⑤⑦ | B.③④⑥ | C.②⑥⑦ | D.①④⑧ |
您最近一年使用:0次
3 . 室温下,向Mg(NO3)2溶液、HF溶液、CH3CH2COOH溶液中分别滴加NaOH溶液,测得溶液中pH与pX[pX=-lgX,X代表 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是
已知:
 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是已知:

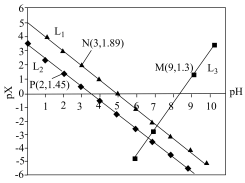
A. 代表的是pH与 代表的是pH与 的关系 的关系 |
B. 的 的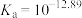 |
C.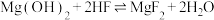 的 的 |
| D.含相同浓度NaF、HF的混合溶液的pH>7 |
您最近一年使用:0次
2024-04-01更新
|
587次组卷
|
6卷引用:内蒙古自治区赤峰第四中学2023-2024学年高三下学期开学考试理综试题-高中化学
4 . 室温下,向Na2CO3和NaHCO3的混合溶液中逐滴加入BaCl2溶液,溶液中-1gc(Ba2+)与 的关系如图所示(已知:
的关系如图所示(已知: 、
、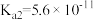 ;
; )。下列说法正确的是
)。下列说法正确的是
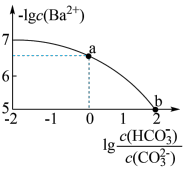
 的关系如图所示(已知:
的关系如图所示(已知: 、
、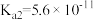 ;
; )。下列说法正确的是
)。下列说法正确的是
| A.a对应溶液pH=6.5 |
B.b对应溶液的c(HCO )=0.05mol/L )=0.05mol/L |
C.a→b的过程中,溶液中 一直增大 一直增大 |
D.a对应的溶液中一定存在: |
您最近一年使用:0次
2023-09-01更新
|
1183次组卷
|
3卷引用:内蒙古赤峰二中2023-2024学年高三上学期10月月考化学试题
内蒙古赤峰二中2023-2024学年高三上学期10月月考化学试题辽宁省鞍山市2023-2024学年高三上学期第一次质量监测化学试题(已下线)考点4 沉淀溶解平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
5 . 铝镁合金是飞机制造、化工生产等行业的重要材料。某研究性学习小组为测定某铝镁合金(不含其他元素)中铝的质量分数,设计了下列两种不同实验方案进行探究。填写下列空白:
[方案一]将铝镁合金与足量NaOH溶液反应,测定剩余固体质量。
(1)实验中发生反应的离子方程式是___ 。
[实验步骤]
(2)称取8.1g铝镁合金粉末样品,溶于体积为V、物质的量浓度为4.0mol·L-1NaOH溶液中,充分反应。则NaOH溶液的体积V≥___ mL。
(3)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得铝的质量分数将___ (填“偏高”、“偏低”或“无影响”)。
[方案二]将铝镁合金与足量稀硫酸溶液反应,测定生成气体的体积。
[实验步骤]
(4)同学们拟选用下列实验装置完成实验:
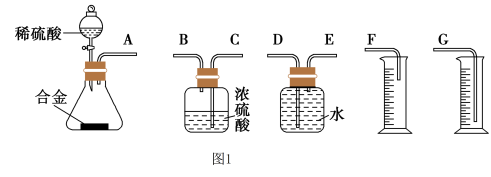
你认为最简易的装置其连接顺序是A接( ),( )接( ),( )接( )(填接口字母,注意:可不填满)___ 。
(5)仔细分析上述实验装置后,同学们认为会引起较大误差。于是他们设计了如图2所示的实验装置。与图2装置相比,用图1连接的装置进行实验时,若不考虑导管中液体体积的影响,测定铝镁合金中铝的质量分数将___ (填“偏大”、“偏小”或“无影响”).
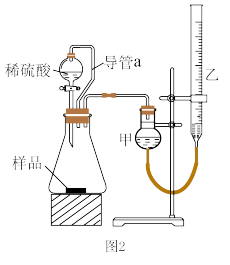
某同学提出该实验装置不够完善,应在甲和锥形瓶之间添加一个装有碱石灰的干燥装置。你的意见是___ (填“需要”或“不需要”)
(6)用图2装置进行实验时:为了较准确测量氢气的体积,在读反应前后量气管乙中液面的读数求其差值的过程中,应注意___(填字母编号)。
(7)图2装置进行实验,合金的质量为7.8g,测得氢气体积为8.96L(标准状况),则合金中铝的质量分数为___ (保留两位有效数字)。
[方案一]将铝镁合金与足量NaOH溶液反应,测定剩余固体质量。
(1)实验中发生反应的离子方程式是
[实验步骤]
(2)称取8.1g铝镁合金粉末样品,溶于体积为V、物质的量浓度为4.0mol·L-1NaOH溶液中,充分反应。则NaOH溶液的体积V≥
(3)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得铝的质量分数将
[方案二]将铝镁合金与足量稀硫酸溶液反应,测定生成气体的体积。
[实验步骤]
(4)同学们拟选用下列实验装置完成实验:

你认为最简易的装置其连接顺序是A接( ),( )接( ),( )接( )(填接口字母,注意:可不填满)
(5)仔细分析上述实验装置后,同学们认为会引起较大误差。于是他们设计了如图2所示的实验装置。与图2装置相比,用图1连接的装置进行实验时,若不考虑导管中液体体积的影响,测定铝镁合金中铝的质量分数将

某同学提出该实验装置不够完善,应在甲和锥形瓶之间添加一个装有碱石灰的干燥装置。你的意见是
(6)用图2装置进行实验时:为了较准确测量氢气的体积,在读反应前后量气管乙中液面的读数求其差值的过程中,应注意___(填字母编号)。
| A.冷却至室温 |
| B.等待片刻,待乙管中液面不再上升时立即读数 |
| C.读数时应移动右侧量气管,使甲乙两端液面相平 |
| D.视线与凹液面最低处相平 |
您最近一年使用:0次
名校
解题方法
6 . 某烃的结构简式为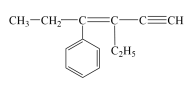 ,若分子中共线碳原子数为a,可能共面的碳原子数最多为b,含四面体结构的碳原子数为c,则a、b、c分别是( )
,若分子中共线碳原子数为a,可能共面的碳原子数最多为b,含四面体结构的碳原子数为c,则a、b、c分别是( )
 ,若分子中共线碳原子数为a,可能共面的碳原子数最多为b,含四面体结构的碳原子数为c,则a、b、c分别是( )
,若分子中共线碳原子数为a,可能共面的碳原子数最多为b,含四面体结构的碳原子数为c,则a、b、c分别是( )| A.3、4、5 | B.3、10、4 |
| C.3、14、4 | D.4、10、4 |
您最近一年使用:0次
2020-05-14更新
|
6338次组卷
|
40卷引用:2016-2017学年内蒙古赤峰二中高二上月考二化学卷
2016-2017学年内蒙古赤峰二中高二上月考二化学卷【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高二上学期第二次月考化学试题【全国百强校】陕西省西安市长安区第一中学2017-2018学年高一下学期期末考试(理)化学试题广西壮族自治区贵港市覃塘高级中学2018-2019学年高二上学期9月月考化学试题【全国百强校】江西省南昌市第十中学2018-2019学年高二下学期3月月考化学试题(已下线)2019年6月8日 《每日一题》选修5-周末培优内蒙古呼和浩特开来中学2018-2019学年高二5月期中考试化学试题云南省丘北二中2018-2019学年高二下学期期末考试化学试题河北省鸡泽县第一中学2019-2020学年高二10月月考化学试题江西省宜春市宜丰中学2019-2020学年高二上学期第三次月考化学试题有机物分子中原子共线共面问题和芳香烃的同分异构专题-【百强校】河南省洛阳市第一高级中学高三化学复习练习云南省陆良县联办高级中学2019-2020学年高二上学期期末考试化学试题广西壮族自治区崇左市大新县大新中学2019-2020学年高二上学期期末考试化学试题广西壮族自治区崇左市宁明中学2019-2020学年高二上学期期末考试化学试题吉林省白城市第四中学2019-2020学年高二下学期网上阶段检测化学试题山西省长治市2019-2020学年高二下学期第一次在线月考化学试题广西隆林县第二中学2019-2020学年高二上学期期末考试化学试题福建省莆田市荔城区第二十四中学2019-2020学年高二下学期期中化学试题河北省张家口市涿鹿县涿鹿中学2019-2020学年高二下学期3月月考化学试题甘肃省张掖市临泽县第一中学2019-2020学年高二下学期期中考试化学试题高二选择性必修3(人教版2019)第二章 烃 专题2 有机化合物共线 共面问题的判断江西省新余市2020-2021学年高一下学期期末质量检测化学试题河北省唐山市曹妃甸第一中学2020-2021学年高一下学期6月月考化学试题(已下线)专题讲座(十) 有机物分子中原子共线、共面的判断(精练)-2022年高考化学一轮复习讲练测黑龙江省哈尔滨工业大学附属中学校2021-2022学年高二上学期期末考试化学试题(已下线)第11讲 烃的燃烧、共面问题(word讲义)-【帮课堂】2021-2022学年高二化学同步精品讲义(人教2019选择性必修3)辽宁省建平县实验中学2021-2022学年高二下学期第三次月考化学试题黑龙江省哈尔滨市德强高中2021-2022学年高二下学期期中考试化学试题上海市宝山区2022届高三模拟考试化学试题山东省青岛市2022届高三下学期五月模拟考试化学试题辽宁省部分中学2019-2020高一下学期期末考试化学试题安徽省芜湖市第一中学2022-2023学年高二上学期12月份教学质量检测化学试题河南省安阳市第一中学2023届高三第四次全真模拟化学试题(已下线)烃——课时7烃的燃烧与共面第二章 烃(A卷·知识通关练)-2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修3)山西省晋城市第一中学校2022-2023学年高二下学期5月月考化学试题湖北省武汉外国语学校2022-2023学年高一下学期期末考试化学试题湖南省邵阳市第二中学2023-2024学年高二上学期基础知识竞赛化学试题7.2.2 烃、有机高分子材料 随堂练习天津市崇化中学2023-2024学年高二下学期期中阶段质量监测化学试卷
7 . 某温度下,分别向20mL浓度均为xmol/L的NaCl和Na2CrO4溶液中滴加0.1mol/LAgNO3溶液,滴加过程中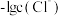 和
和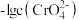 与AgNO3溶液的体积关系如图所示。下列说法不正确的是
与AgNO3溶液的体积关系如图所示。下列说法不正确的是

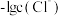 和
和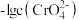 与AgNO3溶液的体积关系如图所示。下列说法不正确的是
与AgNO3溶液的体积关系如图所示。下列说法不正确的是
| A.x =0.1 | B.曲线I代表NaCl溶液 |
| C.Ksp(Ag2CrO4)约为4×10-12 | D.y=9 |
您最近一年使用:0次
2020-04-25更新
|
2121次组卷
|
7卷引用:内蒙古赤峰二中2021-2022学年高二上学期期末考试化学试题
2013·全国·一模
8 . 甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如表所示:
(1)反应②是_______ (填“吸热”或“放热”)反应。
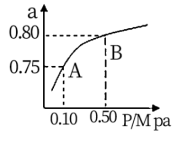
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系,如图所示。则平衡状态由A变到B时,平衡常数K(A) K(B)(填“>”、“<”或“=”)。据反应①与②可推导出K1、K2与K3之间的关系,则K3=_______ (用K1、K2表示)。
(3)在3 L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。

当曲线Ⅰ变为曲线Ⅱ时,改变的条件是_______ 。
当曲线Ⅰ变为曲线Ⅲ时,改变的条件是_______ 。
(4)甲醇燃料电池有着广泛的用途,同时Al-AgO电池是应用广泛的鱼 雷电池,其原理如图所示。该电池的负极反应式是_______

(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)= c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数为_______ 。
| 化学反应 | 平衡常数 | 温度℃ | |
| 500 | 800 | ||
| ①2H2(g)+CO(g)⇌CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)⇌ H2O (g)+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)⇌CH3OH(g)+H2O (g) | K3 | ||
(1)反应②是
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系,如图所示。则平衡状态由A变到B时,平衡常数K(A) K(B)(填“>”、“<”或“=”)。据反应①与②可推导出K1、K2与K3之间的关系,则K3=

(3)在3 L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。

当曲线Ⅰ变为曲线Ⅱ时,改变的条件是
当曲线Ⅰ变为曲线Ⅲ时,改变的条件是
(4)甲醇燃料电池有着广泛的用途,同时Al-AgO电池是应用广泛的鱼 雷电池,其原理如图所示。该电池的负极反应式是

(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)= c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数为
您最近一年使用:0次
解题方法
9 . 尿素是蛋白质代谢的产物,也是重要的化学肥料。工业合成尿素反应如下:
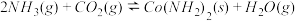
(1)在一个真空恒容密闭容器中充入CO2和NH3发生上述反应合成尿素,恒定温度下混合气体中的氨气含量如图所示。
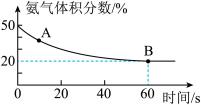
①A点的正反应速率v正(CO2)_______ B点的逆反应速率v逆(CO2)(填“>”、“<”或“=”);
氨气的平衡转化率为________________________ 。
②关于上述反应的平衡状态下列说法正确的是________________
(2)合成尿素的反应在进行时分为如下两步:
第一步:2NH3(l)+CO2(g) H2NCOONH4(l) (氨基甲酸铵) △H1
H2NCOONH4(l) (氨基甲酸铵) △H1
第二步:H2NCOONH4(l) H2O(l)+H2NCONH2(l) △H2
H2O(l)+H2NCONH2(l) △H2
某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如下图Ⅰ所示:

①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第_______ 步反应决定,总反应进行到 _______ min时到达平衡。
②反应进行到10 min时测得CO2的物质的量如图所示,则用CO2表示的第一步反应的速率v(CO2)=_________ 。
③第二步反应的平衡常数K随温度的变化如上右图Ⅱ所示,则△H2________ 0(填“>”“<”或“=”)
④第一步反应的△S________ 0(填“>”、“<”或,“=”),在________ (填“较高”或“较低”)温度下有利于该反应自发进行。
(3)氨基甲酸铵极易水解成碳酸铵,酸性条件水解更彻底。将氨基甲酸铵粉末逐渐加入1L0.1mol/L的盐酸溶液中直到pH=7(室温下,忽略溶液体积变化),共用去0.052mol氨基甲酸铵,此时溶液中几乎不含碳元素。此时溶液中c(NH4+)=_____________________ ;NH4+水解平衡常数值为______________ 。
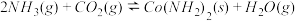
(1)在一个真空恒容密闭容器中充入CO2和NH3发生上述反应合成尿素,恒定温度下混合气体中的氨气含量如图所示。

①A点的正反应速率v正(CO2)
氨气的平衡转化率为
②关于上述反应的平衡状态下列说法正确的是
| A.分离出少量的尿素,反应物的转化率将增大 |
| B.平衡时再充入一定量NH3 (g),CO2的转化率增大 |
| C.NH3的转化率始终等于CO2的转化率 |
| D.加入有效的催化剂能够提高尿素的产率 |
第一步:2NH3(l)+CO2(g)
 H2NCOONH4(l) (氨基甲酸铵) △H1
H2NCOONH4(l) (氨基甲酸铵) △H1第二步:H2NCOONH4(l)
 H2O(l)+H2NCONH2(l) △H2
H2O(l)+H2NCONH2(l) △H2某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如下图Ⅰ所示:

①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第
②反应进行到10 min时测得CO2的物质的量如图所示,则用CO2表示的第一步反应的速率v(CO2)=
③第二步反应的平衡常数K随温度的变化如上右图Ⅱ所示,则△H2
④第一步反应的△S
(3)氨基甲酸铵极易水解成碳酸铵,酸性条件水解更彻底。将氨基甲酸铵粉末逐渐加入1L0.1mol/L的盐酸溶液中直到pH=7(室温下,忽略溶液体积变化),共用去0.052mol氨基甲酸铵,此时溶液中几乎不含碳元素。此时溶液中c(NH4+)=
您最近一年使用:0次
10 . (Ⅰ.利用含锰废水(主要含Mn2+、SO 、H+、Fe2+、Al3+、Cu2+)可制备高性能磁性材料碳酸锰(MnCO3)。其中一种工艺流程如下:
、H+、Fe2+、Al3+、Cu2+)可制备高性能磁性材料碳酸锰(MnCO3)。其中一种工艺流程如下:

已知某些物质完全沉淀的pH如下表:
回答下列问题:
(1)过程②中,所得滤渣W的主要成分是_________________ 。
(2)过程③中,发生反应的离子方程式是_________________ 。
(3)过程④中,若生成的气体J可使澄清石灰水变浑浊,则生成MnCO3的反应的离子方程
式是___________________________ 。
(4)由MnCO3可制得重要的催化剂MnO2:2MnCO3+O2=2MnO2+2CO2。现在空气中加热460.0 g MnCO3,得到332.0 g产品,若产品中杂质只有MnO,则该产品中MnO2的质量分数是_________ (用百分数表示,小数点后保留1位小数)。
Ⅱ.常温下,浓度均为0.1 mol·L-1的下列六种溶液的pH如下表:
(1)上述盐溶液中的阴离子,结合H+能力最强的是_________ 。
(2)根据表中数据判断,浓度均为0.01 mol·L-1的下列物质的溶液中,酸性最强的是_________ (填序号)。
A.HCN
B.HClO
C.C6H5OH
D.CH3COOH
E.H2CO3
(3)根据上表数据,请你判断下列反应不能成立的是_________ (填序号)。
A.HCN+Na2CO3=NaHCO3+NaCN
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
D.CH3COONa+HClO=NaClO+CH3COOH
 、H+、Fe2+、Al3+、Cu2+)可制备高性能磁性材料碳酸锰(MnCO3)。其中一种工艺流程如下:
、H+、Fe2+、Al3+、Cu2+)可制备高性能磁性材料碳酸锰(MnCO3)。其中一种工艺流程如下:
已知某些物质完全沉淀的pH如下表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 | Mn(OH)2 | CuS | MnS | MnCO3 |
| 沉淀完全时的pH | 3.2 | 5.4 | 6.4 | 9.8[ | ≥0 | ≥7 | ≥7 |
(1)过程②中,所得滤渣W的主要成分是
(2)过程③中,发生反应的离子方程式是
(3)过程④中,若生成的气体J可使澄清石灰水变浑浊,则生成MnCO3的反应的离子方程
式是
(4)由MnCO3可制得重要的催化剂MnO2:2MnCO3+O2=2MnO2+2CO2。现在空气中加热460.0 g MnCO3,得到332.0 g产品,若产品中杂质只有MnO,则该产品中MnO2的质量分数是
Ⅱ.常温下,浓度均为0.1 mol·L-1的下列六种溶液的pH如下表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
(2)根据表中数据判断,浓度均为0.01 mol·L-1的下列物质的溶液中,酸性最强的是
A.HCN
B.HClO
C.C6H5OH
D.CH3COOH
E.H2CO3
(3)根据上表数据,请你判断下列反应不能成立的是
A.HCN+Na2CO3=NaHCO3+NaCN
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
D.CH3COONa+HClO=NaClO+CH3COOH
您最近一年使用:0次



