名校
1 . 硫脲 在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备
在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备 ,然后
,然后 再与CaCN2合成
再与CaCN2合成 ,实验装置(夹持及加热装置略)如图所示。
,实验装置(夹持及加热装置略)如图所示。 易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。
易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。
回答下列问题:
(1)实验前先检查装置气密性,操作为:①在E中加水至浸没导管末端,……;②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;③一段时间后,E处导管末端形成一段水柱,且高度不变。将操作①补充完整_______ 。
(2)检查气密性后加入药品,装置A中的试剂最佳组合是_______ (填字母),打开K2。
A.FeS固体+浓硫酸 B.FeS固体+稀硝酸 C.FeS固体+稀盐酸
装置B中盛装的试剂为_______ 。待A中反应结束后关闭K2,打开K1通N2一段时间,目的是_______ 。
(3)撤走搅拌器,打开K3,水浴加热D处三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度在80℃的原因是_______ ,D处合成硫脲的化学方程式为_______ 。
(4)将装置D中液体过滤后,结晶得到粗产品。测定粗产品中硫脲纯度:称取mg产品,加水溶解配成500mL溶液,量取25mL于锥形瓶中,滴加一定量的稀硫酸使溶液显酸性,用cmol⋅L-1KMnO4标准溶液滴定,滴定至终点时消耗KMnO4标准溶液VmL。
①硫脲 中硫元素的化合价为
中硫元素的化合价为_______ 价。
②滴定时,硫脲转化为CO2、N2、 的离子方程式为
的离子方程式为_______ 。
③样品中硫脲的质量分数为_______ (用含“m,c、V”的式子表示)。
 在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备
在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备 ,然后
,然后 再与CaCN2合成
再与CaCN2合成 ,实验装置(夹持及加热装置略)如图所示。
,实验装置(夹持及加热装置略)如图所示。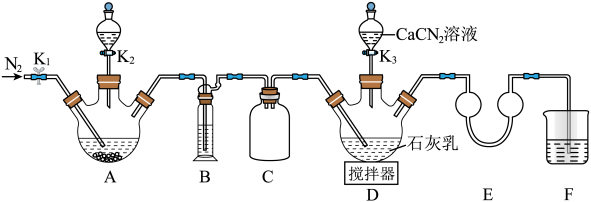
 易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。
易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。回答下列问题:
(1)实验前先检查装置气密性,操作为:①在E中加水至浸没导管末端,……;②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;③一段时间后,E处导管末端形成一段水柱,且高度不变。将操作①补充完整
(2)检查气密性后加入药品,装置A中的试剂最佳组合是
A.FeS固体+浓硫酸 B.FeS固体+稀硝酸 C.FeS固体+稀盐酸
装置B中盛装的试剂为
(3)撤走搅拌器,打开K3,水浴加热D处三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度在80℃的原因是
(4)将装置D中液体过滤后,结晶得到粗产品。测定粗产品中硫脲纯度:称取mg产品,加水溶解配成500mL溶液,量取25mL于锥形瓶中,滴加一定量的稀硫酸使溶液显酸性,用cmol⋅L-1KMnO4标准溶液滴定,滴定至终点时消耗KMnO4标准溶液VmL。
①硫脲
 中硫元素的化合价为
中硫元素的化合价为②滴定时,硫脲转化为CO2、N2、
 的离子方程式为
的离子方程式为③样品中硫脲的质量分数为
您最近一年使用:0次
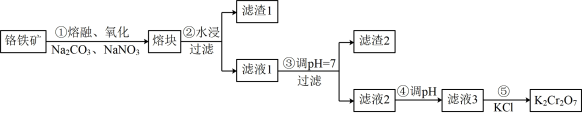
2 . 铬铁矿的主要成分为FeO▪Cr2O3, 制备K2Cr2O7流程如图所示:
(1)基态Cr原子价电子轨道分布图为__________ ,铬位于元素周期表中__________ 区。
(2)配合物[Cr(NH3)4(H2O)2]Cl中提供电子对形成配位键的原子是__________ ,中心离子的配位数为_________ 。
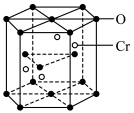
(3)铬的一种氧化物晶胞结构如图所示,若六棱柱的底面边长为lnm,高为hnm,NA代表同伏加德罗常数的值,则该晶体的密度p=__________ g/cm3。 形式存在。则该步主要反应的方程为
形式存在。则该步主要反应的方程为__________ ,该步骤不能使用陶瓷容器,原因是__________ 。
(5)步骤④调滤液2的pH使之变__________ (填“大”或“小”)。原因是__________ (用离子方程式表示)。
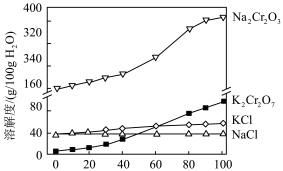
(6)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,分离得到K2Cr2O7固体的方法是__________ ,冷却到__________ (填标号)得到的K2Cr2O7固体产品最多。
(7)已知Ksp(Ag2CrO4 )=1.0×10-12、Ksp(AgCl)=2.0×10-10, 若用10LNaCl溶液溶解0.1mol的Ag2CrO4固体,则NaCl溶液的最初浓度不得低于__________ mol/L。
(1)基态Cr原子价电子轨道分布图为
(2)配合物[Cr(NH3)4(H2O)2]Cl中提供电子对形成配位键的原子是
(3)铬的一种氧化物晶胞结构如图所示,若六棱柱的底面边长为lnm,高为hnm,NA代表同伏加德罗常数的值,则该晶体的密度p=
 形式存在。则该步主要反应的方程为
形式存在。则该步主要反应的方程为(5)步骤④调滤液2的pH使之变
(6)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,分离得到K2Cr2O7固体的方法是
(7)已知Ksp(Ag2CrO4 )=1.0×10-12、Ksp(AgCl)=2.0×10-10, 若用10LNaCl溶液溶解0.1mol的Ag2CrO4固体,则NaCl溶液的最初浓度不得低于
您最近一年使用:0次
名校
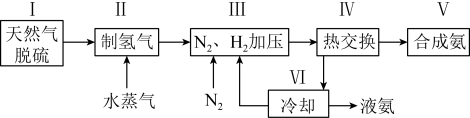
3 . 合成氨是人类科学技术上的一项重大突破,一种工业合成氨的简式流程图如下:
(1)步骤 可以使用湿法脱硫。科研人员把铁的配合物
可以使用湿法脱硫。科研人员把铁的配合物 (L为配体)溶于弱碱性的海水中,制成吸收液,将气体
(L为配体)溶于弱碱性的海水中,制成吸收液,将气体 转化为单质硫。该工艺包含两个阶段:①
转化为单质硫。该工艺包含两个阶段:① 的吸收氧化;②
的吸收氧化;② 的再生。反应原理如下:
的再生。反应原理如下:
①
 (
( )
)
②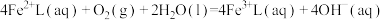
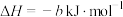 (
( )
)
该工艺的总反应热化学方程式为___________ 。
(2)用氨水也可以吸收 ,产物为
,产物为 。常温下0.1mol/L的
。常温下0.1mol/L的 溶液pH
溶液pH___________ (选填“>”、“<”或“=”)7,其中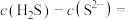
___________ (用溶液中其他粒子浓度计算式表示)。( ,
, ,
, ,
,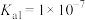 ,
,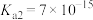 )
)
(3)步骤 中制氢气的原理如下:
中制氢气的原理如下:
①
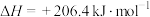
②
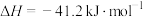
反应①能自发进行的条件是___________ (选填“高温”、“低温”或“任何温度”)。若在恒容绝热容器中加入2mol CO和1mol  只进行反应②,可以判定反应达到平衡的是
只进行反应②,可以判定反应达到平衡的是___________ 。
a.相同时间段内CO消耗的物质的量与 生成的物质的量相同
生成的物质的量相同
b.气体平均摩尔质量保持不变
c.CO与 转化率一样
转化率一样
d.CO分压保持不变
e.体系总压保持不变
(4)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是___________ (填序号)。简述本流程中提高合成氨原料总转化率的方法:___________ 。
(5)利用电化学法也可以合成氨。如图是用低温固体质子导体作为电解质,用 做阴极催化剂电解氢气和氮气合成氨的原理示意图。
做阴极催化剂电解氢气和氮气合成氨的原理示意图。 电极反应产生氨气的电极反应式为
电极反应产生氨气的电极反应式为___________ 。若 电极一侧通入纯氮气0.5mol,阴极出气口获得的气体总量增加0.3mol,经检测转移电子1mol,则在阴极出气口获得的气体中,氨气的体积分数为
电极一侧通入纯氮气0.5mol,阴极出气口获得的气体总量增加0.3mol,经检测转移电子1mol,则在阴极出气口获得的气体中,氨气的体积分数为___________ 。
(1)步骤
 可以使用湿法脱硫。科研人员把铁的配合物
可以使用湿法脱硫。科研人员把铁的配合物 (L为配体)溶于弱碱性的海水中,制成吸收液,将气体
(L为配体)溶于弱碱性的海水中,制成吸收液,将气体 转化为单质硫。该工艺包含两个阶段:①
转化为单质硫。该工艺包含两个阶段:① 的吸收氧化;②
的吸收氧化;② 的再生。反应原理如下:
的再生。反应原理如下:①

 (
( )
)②
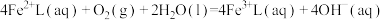
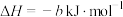 (
( )
)该工艺的总反应热化学方程式为
(2)用氨水也可以吸收
 ,产物为
,产物为 。常温下0.1mol/L的
。常温下0.1mol/L的 溶液pH
溶液pH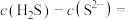
 ,
, ,
, ,
,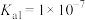 ,
,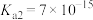 )
)(3)步骤
 中制氢气的原理如下:
中制氢气的原理如下:①

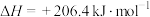
②

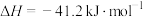
反应①能自发进行的条件是
 只进行反应②,可以判定反应达到平衡的是
只进行反应②,可以判定反应达到平衡的是a.相同时间段内CO消耗的物质的量与
 生成的物质的量相同
生成的物质的量相同b.气体平均摩尔质量保持不变
c.CO与
 转化率一样
转化率一样d.CO分压保持不变
e.体系总压保持不变
(4)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是
(5)利用电化学法也可以合成氨。如图是用低温固体质子导体作为电解质,用
 做阴极催化剂电解氢气和氮气合成氨的原理示意图。
做阴极催化剂电解氢气和氮气合成氨的原理示意图。 电极反应产生氨气的电极反应式为
电极反应产生氨气的电极反应式为 电极一侧通入纯氮气0.5mol,阴极出气口获得的气体总量增加0.3mol,经检测转移电子1mol,则在阴极出气口获得的气体中,氨气的体积分数为
电极一侧通入纯氮气0.5mol,阴极出气口获得的气体总量增加0.3mol,经检测转移电子1mol,则在阴极出气口获得的气体中,氨气的体积分数为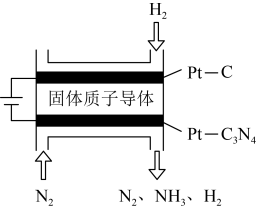
您最近一年使用:0次
名校
4 . 某学习小组欲利用 平衡体系探究影响平衡的因素,将
平衡体系探究影响平衡的因素,将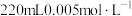
 溶液和
溶液和 溶液混合,得血红色溶液X,进行下列实验:
溶液混合,得血红色溶液X,进行下列实验:
实验Ⅰ.改变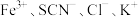 等离子浓度对平衡的影响
等离子浓度对平衡的影响
(1)取2mL溶液X,加入5滴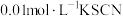 溶液,溶液红色
溶液,溶液红色_______ (填“变深”、“变浅”或“不变”,下同):取2mL溶液X,插入经砂纸打磨过的铁丝,溶液红色_______ 。
(2)取2mL溶液X,加入5滴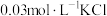 溶液,观察到溶液红色变浅,产生该现象的原因可能是
溶液,观察到溶液红色变浅,产生该现象的原因可能是_______ 或者不直接参与平衡体系的 或
或 对平衡产生了影响。
对平衡产生了影响。
实验Ⅱ.探究KCl对平衡体系的影响,为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。 平衡有影响,且KCl浓度越大,影响
平衡有影响,且KCl浓度越大,影响_______ ,二是_______ 。
(4)针对产生上述影响的可能原因,学习小组同学提出以下猜想:
猜想①: 产生的影响。
产生的影响。
猜想②: 产生的影响。
产生的影响。
猜想③:_______ 。
实验Ⅲ.探究盐对 和
和 平衡体系产生的影响
平衡体系产生的影响
资料信息:
a.溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
b.在 溶液中存在反应
溶液中存在反应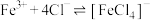 。
。
(5)根据上述信息,学习小组同学各取2mL溶液X,分别加入5滴①去离子水、②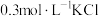 溶液、溶液、③
溶液、溶液、③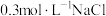 溶液、④
溶液、④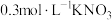 溶液、⑤
溶液、⑤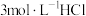 溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
溶液进行实验,测得各溶液的透射率随时间的变化如图所示。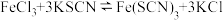 平衡体系的实验组是
平衡体系的实验组是____ ,盐效应影响较大的阳离子是_______ 。
A.实验①②③ B.实验①②④ C.实验①③④
(6)解释出现实验⑤现象的原因:_______ 。
 平衡体系探究影响平衡的因素,将
平衡体系探究影响平衡的因素,将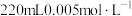
 溶液和
溶液和 溶液混合,得血红色溶液X,进行下列实验:
溶液混合,得血红色溶液X,进行下列实验:实验Ⅰ.改变
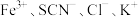 等离子浓度对平衡的影响
等离子浓度对平衡的影响(1)取2mL溶液X,加入5滴
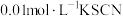 溶液,溶液红色
溶液,溶液红色(2)取2mL溶液X,加入5滴
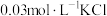 溶液,观察到溶液红色变浅,产生该现象的原因可能是
溶液,观察到溶液红色变浅,产生该现象的原因可能是 或
或 对平衡产生了影响。
对平衡产生了影响。实验Ⅱ.探究KCl对平衡体系的影响,为了确定KCl是否对平衡产生影响,学习小组同学进行如下探究:各取2mL溶液X放入3支比色皿中,分别滴加5滴不同浓度的KCl溶液,并测定各溶液的透射率随时间的变化(已知溶液颜色越深,透射率越小),结果如图所示。
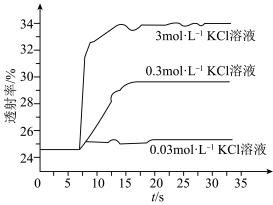
 平衡有影响,且KCl浓度越大,影响
平衡有影响,且KCl浓度越大,影响(4)针对产生上述影响的可能原因,学习小组同学提出以下猜想:
猜想①:
 产生的影响。
产生的影响。猜想②:
 产生的影响。
产生的影响。猜想③:
实验Ⅲ.探究盐对
 和
和 平衡体系产生的影响
平衡体系产生的影响资料信息:
a.溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。
b.在
 溶液中存在反应
溶液中存在反应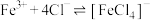 。
。(5)根据上述信息,学习小组同学各取2mL溶液X,分别加入5滴①去离子水、②
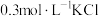 溶液、溶液、③
溶液、溶液、③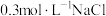 溶液、④
溶液、④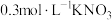 溶液、⑤
溶液、⑤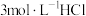 溶液进行实验,测得各溶液的透射率随时间的变化如图所示。
溶液进行实验,测得各溶液的透射率随时间的变化如图所示。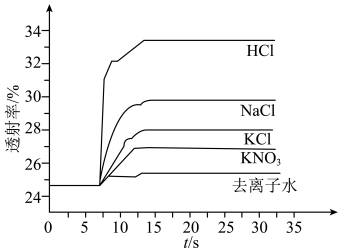
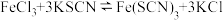 平衡体系的实验组是
平衡体系的实验组是A.实验①②③ B.实验①②④ C.实验①③④
(6)解释出现实验⑤现象的原因:
您最近一年使用:0次
名校
5 . 化合物J是一种EED抑制剂的中间体,其合成路线如下:
(1)C中含氧官能团的名称为__________ 。
(2)E的结构简式为__________ 。
(3)检验F中含碳碳双键的试剂为__________ 。
(4)C→D的反应类型为__________ 。
(5)已知A→B为取代反应,该反应的化学方程式为____________________ 。
(6)与B具有相同官能团且属于芳香族化合物的同分异构体共有__________ 种(不考虑立体异构)。
(7)根据题干信息,补全虚线框内剩余片段,使其合成路线完整__________ 。
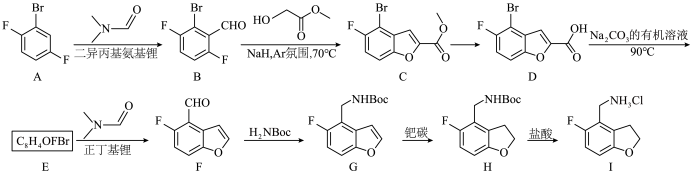
已知:—Boc代表 。
。
(1)C中含氧官能团的名称为
(2)E的结构简式为
(3)检验F中含碳碳双键的试剂为
(4)C→D的反应类型为
(5)已知A→B为取代反应,该反应的化学方程式为
(6)与B具有相同官能团且属于芳香族化合物的同分异构体共有
(7)根据题干信息,补全虚线框内剩余片段,使其合成路线完整

您最近一年使用:0次
2024-04-07更新
|
320次组卷
|
2卷引用:天津市耀华中学2024届高三下学期第一次模拟考试化学试卷
6 . 室温下,向Mg(NO3)2溶液、HF溶液、CH3CH2COOH溶液中分别滴加NaOH溶液,测得溶液中pH与pX[pX=-lgX,X代表 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是
已知:
 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是已知:

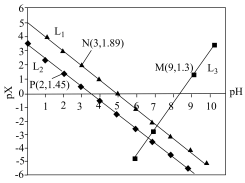
A. 代表的是pH与 代表的是pH与 的关系 的关系 |
B. 的 的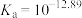 |
C.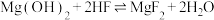 的 的 |
| D.含相同浓度NaF、HF的混合溶液的pH>7 |
您最近一年使用:0次
2024-04-01更新
|
564次组卷
|
6卷引用:天津市耀华中学2024届高三下学期第二次模拟化学试题
名校
7 . 将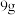 铜和铁的混合物投入
铜和铁的混合物投入 稀硝酸中,充分反应后得到标准状况下
稀硝酸中,充分反应后得到标准状况下 ,剩余
,剩余 金属;继续加入
金属;继续加入 等浓度的稀硝酸,金属完全溶解,又得到标准状况下
等浓度的稀硝酸,金属完全溶解,又得到标准状况下 。若向反应后的溶液中加入
。若向反应后的溶液中加入 溶液,溶液不变红,则下列说法不正确的是
溶液,溶液不变红,则下列说法不正确的是
A.原混合物中铜和铁各 |
B.稀硝酸的物质的量浓度为 |
C.第一次剩余的 金属为铜 金属为铜 |
D.向反应后的溶液中再加入该稀硝酸 ,又得到标准状况下的 ,又得到标准状况下的 |
您最近一年使用:0次
名校
8 . 室温下, 体系中各含碳微粒的物质的量分数与
体系中各含碳微粒的物质的量分数与 的关系如图1所示.在
的关系如图1所示.在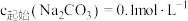 的体系中,研究
的体系中,研究 在不同
在不同 时的可能产物,
时的可能产物,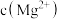 与
与 的关系如图2所示,曲线Ⅰ的离子浓度关系符合
的关系如图2所示,曲线Ⅰ的离子浓度关系符合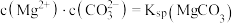 ,曲线Ⅱ的离子浓度关系符合
,曲线Ⅱ的离子浓度关系符合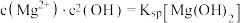 。
。
 体系中各含碳微粒的物质的量分数与
体系中各含碳微粒的物质的量分数与 的关系如图1所示.在
的关系如图1所示.在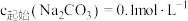 的体系中,研究
的体系中,研究 在不同
在不同 时的可能产物,
时的可能产物,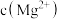 与
与 的关系如图2所示,曲线Ⅰ的离子浓度关系符合
的关系如图2所示,曲线Ⅰ的离子浓度关系符合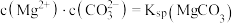 ,曲线Ⅱ的离子浓度关系符合
,曲线Ⅱ的离子浓度关系符合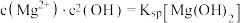 。
。 
A.由 点可求得 点可求得 |
B. 的体系中: 的体系中: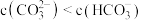 |
C. 点的体系中,发生反应 点的体系中,发生反应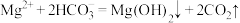 |
D. 点的体系中, 点的体系中,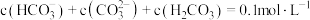 |
您最近一年使用:0次
2024-03-01更新
|
856次组卷
|
2卷引用:天津市耀华中学2024届高三下学期第一次模拟考试化学试卷
名校
解题方法
9 . 科学家合成了一种高温超导材料,其晶胞结构如图所示,该立方晶胞参数为 。设
。设 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是
 。设
。设 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是
A.晶体的最简化学式为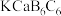 |
B.晶体中与 最近且距离相等的 最近且距离相等的 有4个 有4个 |
| C.晶胞中B和C原子构成的多面体有14个面 |
D.晶体的密度为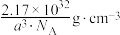 |
您最近一年使用:0次
2023-12-05更新
|
1168次组卷
|
4卷引用:2024届天津市宁河区芦台第一中学高三下学期第三次模拟化学试题
2024届天津市宁河区芦台第一中学高三下学期第三次模拟化学试题吉林省长春市2024届高三上学期质量监测(一)化学试题(已下线)专题04 物质结构与性质 元素推断-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)专题04 物质结构与性质-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
10 . 25℃时,某混合溶液中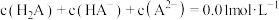 由水电离出的
由水电离出的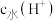 的对数
的对数 与
与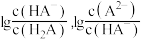 的关系如图所示。下列说法不正确的是
的关系如图所示。下列说法不正确的是

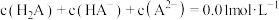 由水电离出的
由水电离出的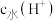 的对数
的对数 与
与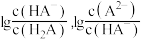 的关系如图所示。下列说法不正确的是
的关系如图所示。下列说法不正确的是
A.曲线 表示 表示 与 与 的变化关系 的变化关系 |
B.X点时存在 |
C.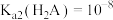 |
D. 点时溶液的 点时溶液的 |
您最近一年使用:0次
2023-11-20更新
|
514次组卷
|
2卷引用:天津市和平区天津市耀华中学2023-2024学年高三上学期第三次月考化学试卷



