名校
解题方法
1 . 如图,通过工业联产可有效解决多晶硅(Si)生产中副产物SiCl4.所带来的环境问题。
(1)
反应①的化学方程式为_______ 。
(2)流程中涉及的化学反应属于氧化还原反应的有_______ (填反应序号)。
(3)高温下,反应④的化学方程式为_______ 。
(4)Si和Ge属于同主族元素。下列预测合理的是_______(填选项序号)。
岩脑砂中元素的测定
准确称取xg岩脑砂,与足量的氧化铜混合加热(发生的反应为: ),利用下列装置测定岩脑砂中氮元素和氯元素的质量之比。
),利用下列装置测定岩脑砂中氮元素和氯元素的质量之比。_______ 。
(6)若装置Ⅰ增重yg,利用装置K测得气体体积为VL(已经换算成标准状况),在读取气体体积时,需要a.将气体冷却;b.视线与凹液面最低处相平;c._______ 。
(7)则岩脑砂中
_______ (用代数式表示,不必化简)。若去掉J装置,则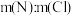 比正确值
比正确值_______ (填“偏高”“偏低”或“无影响”)。
(1)

反应①的化学方程式为
(2)流程中涉及的化学反应属于氧化还原反应的有
(3)高温下,反应④的化学方程式为
(4)Si和Ge属于同主族元素。下列预测合理的是_______(填选项序号)。
| A.Ge与H2化合难于 Si |
| B.GeO2既有氧化性又有还原性 |
| C.酸性H2GeO3>H2SiO3 |
| D.Si和Ge 都可做半导体材料 |
岩脑砂中元素的测定
准确称取xg岩脑砂,与足量的氧化铜混合加热(发生的反应为:
 ),利用下列装置测定岩脑砂中氮元素和氯元素的质量之比。
),利用下列装置测定岩脑砂中氮元素和氯元素的质量之比。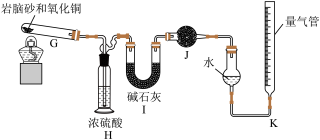
(6)若装置Ⅰ增重yg,利用装置K测得气体体积为VL(已经换算成标准状况),在读取气体体积时,需要a.将气体冷却;b.视线与凹液面最低处相平;c.
(7)则岩脑砂中

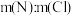 比正确值
比正确值
您最近一年使用:0次
2 . 氮是生物体的重要组成元素,也是维持高等动植物生命活动的必需元素。研究氮的循环和转化对生产和生活有重要的价值。
Ⅰ.某工厂用氨制硝酸和铵盐的流程如图所示。_______ 。实验室固+固制备氨气的化学方程式是_______ 。
(2)同温同压下,理论上设备1与设备2中消耗空气的体积比为___ 。
Ⅱ.氨氮废水的处理是当前科学研究的热点问题。氨氮废水中的氮元素多以 和
和 的形式存在。某工厂处理氨氮废水的流程如图2所示:
的形式存在。某工厂处理氨氮废水的流程如图2所示:_____ 。
(4)过程2的产物均为无毒物质,反应后含氮元素、氯元素的产物化学式分别为_______ 、_______ 。
(5)含余氯废水的主要成分是NaClO以及HClO。X可选用_______(填序号)
(6)为防止环境污染,以下装置(除⑤标明外,其余盛放的液体均为水)可用于吸收多余氨气的是_______ (填序号)。
Ⅰ.某工厂用氨制硝酸和铵盐的流程如图所示。
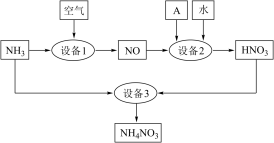
(2)同温同压下,理论上设备1与设备2中消耗空气的体积比为
Ⅱ.氨氮废水的处理是当前科学研究的热点问题。氨氮废水中的氮元素多以
 和
和 的形式存在。某工厂处理氨氮废水的流程如图2所示:
的形式存在。某工厂处理氨氮废水的流程如图2所示:
(4)过程2的产物均为无毒物质,反应后含氮元素、氯元素的产物化学式分别为
(5)含余氯废水的主要成分是NaClO以及HClO。X可选用_______(填序号)
| A.KOH | B. | C. | D.NaCl |
(6)为防止环境污染,以下装置(除⑤标明外,其余盛放的液体均为水)可用于吸收多余氨气的是

您最近一年使用:0次
名校
3 . 过多的NOx排放,往往会产生污染。某研究性小组探究 与炽热的铜粉反应,设计如下
与炽热的铜粉反应,设计如下 能被酸性高锰酸钾溶液氧化成NO
能被酸性高锰酸钾溶液氧化成NO ,此体系中产生的NO
,此体系中产生的NO 浓度较稀。
浓度较稀。
(1)实验开始前,检查装置气密性涉及到以下操作,给出合理的操作顺序:_______ 。
将F中的长导管插入液面以下→_______→_______→_______→_______→_______(操作可重复使用)。
①关闭弹簧夹a,打开弹簧夹b ②观察F中的现象 ③用酒精灯加热A中三颈烧瓶 ④撤走酒精灯
(2)写出A中反应的化学方程式_______ 。装置B的作用是_______ 。
(3)反应一段时间后,装置D中铜粉变黑,写出装置D中发生反应的化学方程式_______ 。
(4)实验过程中,装置E中溶液颜色变浅,则装置E发生的离子方程式为_______ ;
(5)实验前和实验结束时,都需通一段时间的 ,实验结束时目的是
,实验结束时目的是_______ 。
(6)有同学发现装置A溶液呈绿色,而不显蓝色;甲认为是该溶液中硝酸铜质量分数较高所致,而乙认为是该溶液溶解了生成的气体所致。设计方案来判断甲或乙哪种合理,下列方案中不可行 的是_______。
 与炽热的铜粉反应,设计如下
与炽热的铜粉反应,设计如下
 能被酸性高锰酸钾溶液氧化成NO
能被酸性高锰酸钾溶液氧化成NO ,此体系中产生的NO
,此体系中产生的NO 浓度较稀。
浓度较稀。(1)实验开始前,检查装置气密性涉及到以下操作,给出合理的操作顺序:
将F中的长导管插入液面以下→_______→_______→_______→_______→_______(操作可重复使用)。
①关闭弹簧夹a,打开弹簧夹b ②观察F中的现象 ③用酒精灯加热A中三颈烧瓶 ④撤走酒精灯
(2)写出A中反应的化学方程式
(3)反应一段时间后,装置D中铜粉变黑,写出装置D中发生反应的化学方程式
(4)实验过程中,装置E中溶液颜色变浅,则装置E发生的离子方程式为
(5)实验前和实验结束时,都需通一段时间的
 ,实验结束时目的是
,实验结束时目的是(6)有同学发现装置A溶液呈绿色,而不显蓝色;甲认为是该溶液中硝酸铜质量分数较高所致,而乙认为是该溶液溶解了生成的气体所致。设计方案来判断甲或乙哪种合理,下列方案中
| A.加热该绿色溶液,观察颜色变化 |
| B.加水稀释绿色溶液,观察颜色变化 |
| C.向该绿色溶液中通入氮气,观察颜色变化 |
| D.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化某研究性实验小组 |
您最近一年使用:0次
名校
4 . 高锰酸钾生产过程中产生的废锰渣(主要成分为 、
、 和
和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下:
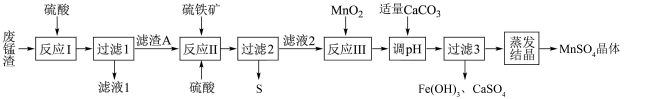
已知:硫铁矿的主要成分为二硫化亚铁( ,杂质不参与反应)。
,杂质不参与反应)。
回答下列问题:
(1)二硫化亚铁中S元素的化合价为_______ 。
(2)①滤渣A的主要成分是_______ (填化学式);
②“反应II”生成 、
、 等物质的离子方程式为
等物质的离子方程式为_______ 。
③“反应III”中还原剂和氧化剂物质的量之比为_______ ;
④“调 ”时,验证
”时,验证 已经沉淀完全的实验操作和现象为
已经沉淀完全的实验操作和现象为_______ 。
 、
、 和
和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下:
已知:硫铁矿的主要成分为二硫化亚铁(
 ,杂质不参与反应)。
,杂质不参与反应)。回答下列问题:
(1)二硫化亚铁中S元素的化合价为
(2)①滤渣A的主要成分是
②“反应II”生成
 、
、 等物质的离子方程式为
等物质的离子方程式为③“反应III”中还原剂和氧化剂物质的量之比为
④“调
 ”时,验证
”时,验证 已经沉淀完全的实验操作和现象为
已经沉淀完全的实验操作和现象为
您最近一年使用:0次
名校
5 . (I)如表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
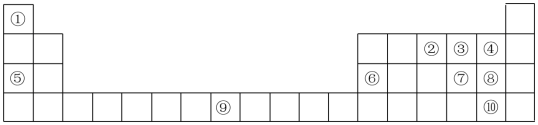
(1)元素②和④的简单氢化物反应生成化合物的电子式为_______ 。
(2)元素⑤和③的单质加热生成产物中含有的化学键类型为_______ 。
(3)元素⑨在周期表中的位置是_______ 。
(II)L、M、N、Q、R、T分别代表上述十种元素之一,其原子半径及主要化合价关系如表:
(4)写出M最高价氧化物对应的水化物与N的最高价含氧酸反应的化学方程式:_______ 。
(5)L、M、Q、R四种元素形成的简单离子半径从大到小的顺序为_______ (用相应的离子符号表示)。

(1)元素②和④的简单氢化物反应生成化合物的电子式为
(2)元素⑤和③的单质加热生成产物中含有的化学键类型为
(3)元素⑨在周期表中的位置是
(II)L、M、N、Q、R、T分别代表上述十种元素之一,其原子半径及主要化合价关系如表:
| 元素代号 | L | M | N | Q | R | T |
| 原子半径/nm | 0.186 | 0.143 | 0.099 | 0.114 | 0.104 | 0.066 |
| 主要化合价 | +1 | +3 | +7、-1 | +7、-1 | +6、-2 | -2 |
(5)L、M、Q、R四种元素形成的简单离子半径从大到小的顺序为
您最近一年使用:0次
名校
解题方法
6 . 铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。黑木耳中含有比较丰富的铁元素,某研究型学习小组同学测定某地黑木耳中铁的含量。
(1)称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。高温灼烧黑木耳,使之完全灰化。将木耳灰用下图流程处理,对滤液中的溶质进行研究。
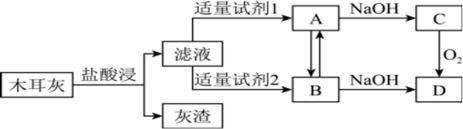
①浸泡液检测不出铁元素的原因是_______ 。
②试剂l应该是_______ 。
(2)A转化为B可加入的试剂有_______ 。
a.酸性高锰酸钾 b.Cl2 c.H2O2溶液
(3)C生成D时的反应现象为_______ 。
(4)已知在酸性条件下Fe2+可被氧气氧化为Fe3+,该反应每转移8mol电子,标准状况下消耗氧气的体积为_______ L。
(1)称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。高温灼烧黑木耳,使之完全灰化。将木耳灰用下图流程处理,对滤液中的溶质进行研究。

①浸泡液检测不出铁元素的原因是
②试剂l应该是
(2)A转化为B可加入的试剂有
a.酸性高锰酸钾 b.Cl2 c.H2O2溶液
(3)C生成D时的反应现象为
(4)已知在酸性条件下Fe2+可被氧气氧化为Fe3+,该反应每转移8mol电子,标准状况下消耗氧气的体积为
您最近一年使用:0次
名校
解题方法
7 . 如图为制取无水氯化铁粉末的装置,已知氯化铁粉末很容易吸水生成含结晶水的化合物。
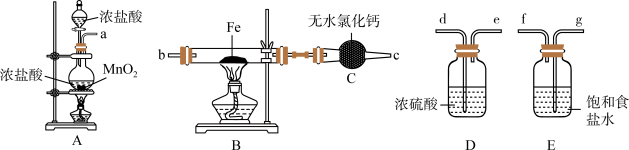
回答下列问题:
(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序):___________ 。
(2)装置A中发生反应的离子方程式为___________ 。
(3)装置E的作用是___________ 。
(4)这套实验装置的缺陷是没有尾气处理装置,应增加一个装有 溶液的烧杯吸收尾气,发生反应的化学方程式为
溶液的烧杯吸收尾气,发生反应的化学方程式为___________ 。
(5)利用制取的无水氯化铁固体配制少量 饱和溶液并制备
饱和溶液并制备 胶体。
胶体。
①溶解制取的无水氯化铁固体时,发现溶液偏浅绿色,取少量溶液于试管中,滴加几滴酸性高锰酸钾溶液,发现高锰酸钾颜色褪去,发生反应的离子方程式为___________ ;溶解所得溶液中含有 的原因可能是
的原因可能是___________ 。
②向沸水中滴加少量 饱和溶液,继续煮沸,至
饱和溶液,继续煮沸,至___________ (填实验现象)时停止,得到 胶体。
胶体。

回答下列问题:
(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序):
(2)装置A中发生反应的离子方程式为
(3)装置E的作用是
(4)这套实验装置的缺陷是没有尾气处理装置,应增加一个装有
 溶液的烧杯吸收尾气,发生反应的化学方程式为
溶液的烧杯吸收尾气,发生反应的化学方程式为(5)利用制取的无水氯化铁固体配制少量
 饱和溶液并制备
饱和溶液并制备 胶体。
胶体。①溶解制取的无水氯化铁固体时,发现溶液偏浅绿色,取少量溶液于试管中,滴加几滴酸性高锰酸钾溶液,发现高锰酸钾颜色褪去,发生反应的离子方程式为
 的原因可能是
的原因可能是②向沸水中滴加少量
 饱和溶液,继续煮沸,至
饱和溶液,继续煮沸,至 胶体。
胶体。
您最近一年使用:0次
2024-03-02更新
|
88次组卷
|
2卷引用:内蒙古自治区乌兰浩特第一中学2023-2024学年高一上学期期末考试化学试题
名校
8 . A、B、C、D、E、F是原子序数依次增大的元素,其相关信息如下。
回答下列问题:
(1)元素A和E形成的化合物的电子式为___________ ,该化合物含有的化学键类型是___________ 。
(2)元素B在元素周期表中的位置为___________ ,其原子结构示意图为___________ 。
(3)元素D形成的单质在元素C形成的单质中燃烧的化学方程式为___________ ;元素D形成的单质久置于空气中最终得到的化合物的化学式为___________ 。
(4)下列事实,能证明元素E的非金属性强于S(硫)的非金属性的是___________(填字母)。
| 元素 | 特征 | 元素 | 特征 |
| A | 该元素的某种原子不含中子 | B | 简单氢化物的分子结构模型为 |
| C | 在人体中含量最多 | D | 该元素形成的化合物灼烧时火焰呈现黄色 |
| E | 该元素形成的单质常温下是黄绿色的有毒气体 | F | 由该元素形成的合金是目前我国用途最广的合金 |
(1)元素A和E形成的化合物的电子式为
(2)元素B在元素周期表中的位置为
(3)元素D形成的单质在元素C形成的单质中燃烧的化学方程式为
(4)下列事实,能证明元素E的非金属性强于S(硫)的非金属性的是___________(填字母)。
A.酸性: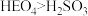 | B. 通入 通入 溶液能产生黄色沉淀 溶液能产生黄色沉淀 |
C.氢化物稳定性: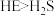 | D.常温下,E的单质为气态,S的单质为固态 |
您最近一年使用:0次
9 . 高锰酸钾生产过程中产生的废锰渣(主要成分为 、KOH和
、KOH和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下:

已知:硫铁矿的主要成分为二硫化亚铁( ,杂质不参与反应)。
,杂质不参与反应)。
回答下列问题:
(1)二硫化亚铁中S元素的化合价为___________ 。
(2)滤渣A的主要成分是___________ (填化学式);“反应Ⅱ”生成 、
、 等物质的离子方程式为
等物质的离子方程式为___________ 。
(3)“反应Ⅲ”中还原剂和氧化剂物质的量之比为___________ ;加入 作为氧化剂的优点是
作为氧化剂的优点是___________ 。
(4)“调pH”时,验证 已经沉淀完全的实验操作和现象为
已经沉淀完全的实验操作和现象为____________________ 。
(5)“蒸发结晶”时,应在___________ 时停止加热。
 、KOH和
、KOH和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下:
已知:硫铁矿的主要成分为二硫化亚铁(
 ,杂质不参与反应)。
,杂质不参与反应)。回答下列问题:
(1)二硫化亚铁中S元素的化合价为
(2)滤渣A的主要成分是
 、
、 等物质的离子方程式为
等物质的离子方程式为(3)“反应Ⅲ”中还原剂和氧化剂物质的量之比为
 作为氧化剂的优点是
作为氧化剂的优点是(4)“调pH”时,验证
 已经沉淀完全的实验操作和现象为
已经沉淀完全的实验操作和现象为(5)“蒸发结晶”时,应在
您最近一年使用:0次
2024-01-08更新
|
214次组卷
|
3卷引用:内蒙古自治区乌兰浩特第一中学2023-2024学年高一上学期期末考试化学试题
名校
10 . 自古至今,铁及其化合物在人类生产生活中的使用发挥了巨大的作用。
(1)古代中国四大发明之一的司南是由天然磁石制成的,其主要成分是__________ (填化学式)。
(2)工业上,可利用硫酸亚铁溶液和氧气在催化剂条件下制作铁黄(FeOOH),一种不溶于水的黄色固体,写出该反应的离子方程式:______________________________ 。
(3)从某工业废渣wg(主要含二氧化硅、氧化铁、氧化镁)中提取氧化铁的工艺流程如图(部分操作和条件略):

已知:二氧化硅不溶于硫酸。
①滤渣的主要成分为__________ (填化学式)。
②写出步骤Ⅴ的化学方程式:______________________________ 。
③请写出验证硫酸亚铁溶液中是否存在 的实验方法:
的实验方法:______________________________ 。
④若提取过程中铁元素的损耗忽略不计,最终获得ng的氧化铁。则废渣中铁元素的质量分数为__________ 。
(1)古代中国四大发明之一的司南是由天然磁石制成的,其主要成分是
(2)工业上,可利用硫酸亚铁溶液和氧气在催化剂条件下制作铁黄(FeOOH),一种不溶于水的黄色固体,写出该反应的离子方程式:
(3)从某工业废渣wg(主要含二氧化硅、氧化铁、氧化镁)中提取氧化铁的工艺流程如图(部分操作和条件略):

已知:二氧化硅不溶于硫酸。
①滤渣的主要成分为
②写出步骤Ⅴ的化学方程式:
③请写出验证硫酸亚铁溶液中是否存在
 的实验方法:
的实验方法:④若提取过程中铁元素的损耗忽略不计,最终获得ng的氧化铁。则废渣中铁元素的质量分数为
您最近一年使用:0次



