解题方法
1 . 绿矾(FeSO4·xH2O)是自然界存在的一种矿石,翠绿如宝石,很早就引起人们的重视;绿矾焙烧是一种生产硫酸的古老方法。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,若产生___________ 现象,说明该样品已变质。
(2)为测定绿矾中结晶水含量,将石英玻璃管A(带两端开关K1和K2)称重,质量为150.0g,将样品装入石英玻璃管中,再次将装置A称重,质量为177.7g。按如图所示连接好装置进行实验,A中发生的反应为:FeSO4·xH2O FeSO4+xH2O↑。
FeSO4+xH2O↑。
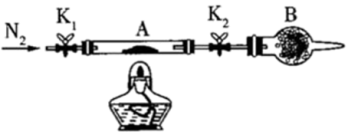
①仪器B的名称是___________ 。
②下列实验操作步骤,正确的顺序为da___________ e;重复上述操作步骤,直至装置A恒重,质量为165.2g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2 d.打开K1和K2,缓缓通入N2 e.称量装置A f.冷却到室温
③根据实验记录,计算绿矾化学式中结晶水数目x=___________ (结果保留到小数点后一位)。
(3)为探究硫酸亚铁高温分解的产物,将(2)中已恒重的装置A接入如图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。
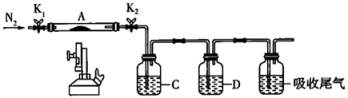
①加热前通入N2的作用是___________ 。
②C中盛有BaCl2溶液,观察到C中有白色沉淀生成,则该沉淀是___________ (填化学式)。
③D中所盛的试剂为品红溶液,观察到溶液褪色。根据上述实验现象,写出硫酸亚铁高温分解的化学反应方程式:___________ 。
(4)绿矾的纯度可通过KMnO4滴定法测定。现称取2.780g绿矾样品,配制成250mL溶液,用硫酸酸化的0.0100mol·L-1的KMnO4溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
①此滴定实验达到终点的现象是___________ 。
②上表中第一次实验记录数据明显大于后两次,其原因可能是___________ (填字母)。
A.第一次滴定前酸式滴定管尖嘴有气泡,滴定结束无气泡
B.第一次滴定用的锥形瓶用待测液润洗过
C.第一次滴定结束时,俯视读取酸性高锰酸钾溶液的体积
D.后两次滴定所用酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,若产生
(2)为测定绿矾中结晶水含量,将石英玻璃管A(带两端开关K1和K2)称重,质量为150.0g,将样品装入石英玻璃管中,再次将装置A称重,质量为177.7g。按如图所示连接好装置进行实验,A中发生的反应为:FeSO4·xH2O
 FeSO4+xH2O↑。
FeSO4+xH2O↑。
①仪器B的名称是
②下列实验操作步骤,正确的顺序为da
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2 d.打开K1和K2,缓缓通入N2 e.称量装置A f.冷却到室温
③根据实验记录,计算绿矾化学式中结晶水数目x=
(3)为探究硫酸亚铁高温分解的产物,将(2)中已恒重的装置A接入如图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

①加热前通入N2的作用是
②C中盛有BaCl2溶液,观察到C中有白色沉淀生成,则该沉淀是
③D中所盛的试剂为品红溶液,观察到溶液褪色。根据上述实验现象,写出硫酸亚铁高温分解的化学反应方程式:
(4)绿矾的纯度可通过KMnO4滴定法测定。现称取2.780g绿矾样品,配制成250mL溶液,用硫酸酸化的0.0100mol·L-1的KMnO4溶液滴定。每次所取待测液体积均为25.00mL,实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 24.52 | 24.02 | 23.98 |
②上表中第一次实验记录数据明显大于后两次,其原因可能是
A.第一次滴定前酸式滴定管尖嘴有气泡,滴定结束无气泡
B.第一次滴定用的锥形瓶用待测液润洗过
C.第一次滴定结束时,俯视读取酸性高锰酸钾溶液的体积
D.后两次滴定所用酸性高锰酸钾标准液保存时间过长,有部分变质,浓度降低
您最近一年使用:0次
名校
解题方法
2 . 下列实验方案能达到实验目的的是
| 实验目的 | 实验方案 | |
| A | 检验 ,晶体是否已氧化变质 ,晶体是否已氧化变质 | 将 样品溶于稀硝酸后,滴加 样品溶于稀硝酸后,滴加 溶液,观察是否有沉淀生成 溶液,观察是否有沉淀生成 |
| B | 证明 ,沉淀可以转化为 ,沉淀可以转化为 沉淀 沉淀 | 向2mL1mol/LNaOH溶液中先加入3滴1mol/L 溶液,再加入3滴1mol/L 溶液,再加入3滴1mol/L 溶液 溶液 |
| C | 制备氢氧化铁胶体 | 向沸水中滴加氯化铁稀溶液,继续煮沸至溶液呈红褐色 |
| D | 证明HA酸性比HB弱 | 等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体,HA放出的氢气多 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 为测定某亚硫酸钠(Na2SO3)样品的纯度,甲同学称取5.0g固体用如下装置进行实验。回答以下问题:
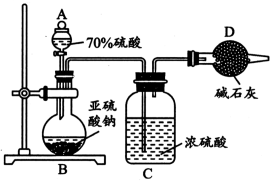
(1)仪器A的名称为_______ 。
(2)B中烧瓶内发生反应的离子方程式为_______ 。
(3)亚硫酸钠易氧化变质,变质后的样品中除亚硫酸钠外还将含有____ (填化学式)。证明Na2SO3样品已部分变质的方法是____ 。
(4)反应结束后,测得D处干燥管增重2.4g,可知该样品中亚硫酸钠的纯度为_______ 。若缺少装置C,实验测得的样品的纯度_______ (填“偏高”或“偏低”或“无影响”)。
(5)乙认为甲的实验方案存在明显缺陷,为使结果更准确,应采取的做法是_______ 。

(1)仪器A的名称为
(2)B中烧瓶内发生反应的离子方程式为
(3)亚硫酸钠易氧化变质,变质后的样品中除亚硫酸钠外还将含有
(4)反应结束后,测得D处干燥管增重2.4g,可知该样品中亚硫酸钠的纯度为
(5)乙认为甲的实验方案存在明显缺陷,为使结果更准确,应采取的做法是
您最近一年使用:0次
4 . 某同学用硫铁矿焙烧后的烧渣(主要成分为Fe2O3、SiO2、Al2O3。不考虑其它杂质)制取绿矾(FeSO4· 7H2O),设计了如下流程(部分物质已略去)。
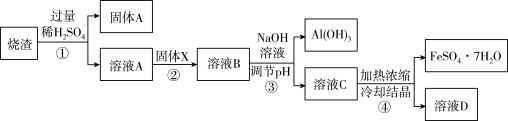
回答下列问题:
(1)硫铁矿的主要成分是FeS2,其中铁元素化合价为_______ ,焙烧产物之一的Fe2O3,俗称________ 。
(2)固体A的主要成分是_______ ,固体X为_________ 。
(3)写出①中Al2O3发生反应的离子方程式:__________ 。
(4)从溶液C到绿矾的过程中,须控制反应条件防止变质,检验其变质所用的化学试剂是________ ,步骤③所得Al(OH)3沉淀含有杂质,应如何洗涤?__________ 。

回答下列问题:
(1)硫铁矿的主要成分是FeS2,其中铁元素化合价为
(2)固体A的主要成分是
(3)写出①中Al2O3发生反应的离子方程式:
(4)从溶液C到绿矾的过程中,须控制反应条件防止变质,检验其变质所用的化学试剂是
您最近一年使用:0次
2020-08-20更新
|
186次组卷
|
3卷引用:广西钦州市浦北县浦北中学2020-2021学年高二3月月考化学试题
5 . Na2CO3、NaHCO3是生活中常见的盐,某实验小组通过以下实验探究这两种物质的性质。
(1)称取两种固体各1g分别放入两支试管中,再各加入5mL水,充分振荡,并恢复至室温。发现Na2CO3完全溶解,而NaHCO3有剩余。由此得出结论:在相同温度下,_______ 。
(2)某学生设计如图所示装置进行NaHCO3的分解实验,并证实产物中有CO2产生。
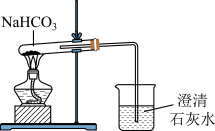
①试管中发生的化学反应方程式为_______ 。
②指出该学生设计的装置图的错误之处,并改正(文字说明即可)_______ 。
(3)测定Na2CO3样品(含氯化钠杂质)中Na2CO3的质量分数:
①称取mg样品放入烧杯内加水溶解。
②加入过量的氯化钙溶液充分反应,反应的化学方程式为_______ 。
③过滤、洗涤、干燥,称量沉淀的质量为ng。则样品中Na2CO3的质量分数为_______ 。
(1)称取两种固体各1g分别放入两支试管中,再各加入5mL水,充分振荡,并恢复至室温。发现Na2CO3完全溶解,而NaHCO3有剩余。由此得出结论:在相同温度下,
(2)某学生设计如图所示装置进行NaHCO3的分解实验,并证实产物中有CO2产生。

①试管中发生的化学反应方程式为
②指出该学生设计的装置图的错误之处,并改正(文字说明即可)
(3)测定Na2CO3样品(含氯化钠杂质)中Na2CO3的质量分数:
①称取mg样品放入烧杯内加水溶解。
②加入过量的氯化钙溶液充分反应,反应的化学方程式为
③过滤、洗涤、干燥,称量沉淀的质量为ng。则样品中Na2CO3的质量分数为
您最近一年使用:0次
名校
6 . 电炉加热时用纯O2氧化管内样品,根据产物的质量确定有机物的组成。用燃烧法确定有机物分子式常用装置如图1所示。

(1)产生的O2按从左到右的流向,所选装置各导管的正确连接顺序是_ (每个装置只能使用一次);
(2)C装置中浓硫酸的作用是__________________________ ;
(3)D装置中发生的化学方程式为______________________ ;
(4)燃烧管中CuO的作用是__________ ,装置F中碱石灰的作用是_____ ;
(5)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.92 g样品,经充分反应后,A管质量增加1.76 g,B管质量增加1.08 g,则该样品的实验式为_________ ;
(6)用质谱仪测定其相对分子质量,得到如图2所示的质谱图,则该有机物的相对分子质量为__ ;

(7)能否根据A的实验式确定A的分子式?____ (填“能”或“不能”),若能,则A的分子式是____ (若不能,则此空不填)。
(8)该物质的1H核磁共振氢谱图如图3所示,则其结构简式为_______________ 。


(1)产生的O2按从左到右的流向,所选装置各导管的正确连接顺序是
(2)C装置中浓硫酸的作用是
(3)D装置中发生的化学方程式为
(4)燃烧管中CuO的作用是
(5)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.92 g样品,经充分反应后,A管质量增加1.76 g,B管质量增加1.08 g,则该样品的实验式为
(6)用质谱仪测定其相对分子质量,得到如图2所示的质谱图,则该有机物的相对分子质量为

(7)能否根据A的实验式确定A的分子式?
(8)该物质的1H核磁共振氢谱图如图3所示,则其结构简式为

您最近一年使用:0次
7 . 某校实验小组的同学利用如图所示实验装置探究氨与氧化铜的反应(图中夹持、固定装置部分均略去)。
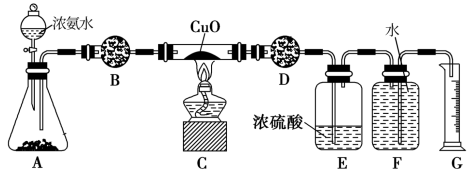
(1)A中盛放浓氨水的仪器的名称是___________ ,锥形瓶中的固体药品为一种纯净物,它是___________ 。
(2)B中固体试剂的作用为___________ 。
(3)打开分液漏斗活塞,加入试剂,点燃C处的酒精灯,一段时间后,观察到C中氧化铜全部转化成光亮的红色固体,经检验该红色固体为一种单质,F中集气瓶内收集到一种无色气态单质。写出装置C中反应的化学方程式:___________ 。
(4)E中浓硫酸的作用是___________ 。
(5)已知Cu2O也是红色的。表中数据为另一小组实验前后C装置的质量,通过计算可知反应后的产物中___________ (填“有”“无”或“无法确定”)Cu2O。

(1)A中盛放浓氨水的仪器的名称是
(2)B中固体试剂的作用为
(3)打开分液漏斗活塞,加入试剂,点燃C处的酒精灯,一段时间后,观察到C中氧化铜全部转化成光亮的红色固体,经检验该红色固体为一种单质,F中集气瓶内收集到一种无色气态单质。写出装置C中反应的化学方程式:
(4)E中浓硫酸的作用是
(5)已知Cu2O也是红色的。表中数据为另一小组实验前后C装置的质量,通过计算可知反应后的产物中
| 空玻璃管 | 实验前(样品+玻璃管) | 实验后(样品+玻璃管) |
| 59.60g | 65.60g | 64.64g |
您最近一年使用:0次
8 . 下图装置是用燃烧法来确定有机物组成的常用装置,这种方法是在电炉加热时用纯氧气氧化硬质玻璃管内样品,根据氧化产物的质量确定有机物的组成(在装置中C里的氧化铜是确保有机物中的碳元素完全转化为二氧化碳)。请回答有关问题:
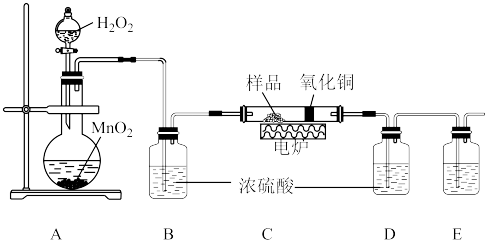
(1)写出A装置中发生反应的化学方程式___________ 。再写出用A装置制取另一种常见气体的化学方程式___________ 。
(2)若去掉B装置会对___________ 元素的测定结果有影响,会使测定结果___________ (填“偏大”或“偏小”)。
(3)E装置中所盛放物质最好是___________ (选填:①石灰水;②NaOH溶液;③水)。
(4)若准确称取1.12克样品(样品只含C、H、O三种元素中的两种或三种)。经充分燃烧,D装置增重1.44克,E装置增重3.52克,则该有机物样品中所含的元素为___________ 。

(1)写出A装置中发生反应的化学方程式
(2)若去掉B装置会对
(3)E装置中所盛放物质最好是
(4)若准确称取1.12克样品(样品只含C、H、O三种元素中的两种或三种)。经充分燃烧,D装置增重1.44克,E装置增重3.52克,则该有机物样品中所含的元素为
您最近一年使用:0次
解题方法
9 . 某学习小组用如下实验装置测定某生铁(铁碳合金)样品中的碳元素含量及浓硫酸的还原产物。

(1)仪器A的名称是_______ 。
(2)装置B中品红溶液的作用是_______ ;装置C中酸性高锰酸钾溶液的作用是_______ 。
(3)取生铁样品15g,与足量浓硫酸完全反应后无固体剩余。假设产生的 全部进入装置E中,称得装置E增重2.2g,则该生铁样品中的碳元素含量为
全部进入装置E中,称得装置E增重2.2g,则该生铁样品中的碳元素含量为 _______ ;甲同学认为装置F多余,若撤去装置F,则测得样品中的碳元素含量_______ (填“偏高”、“偏低”或“无影响”)。

(1)仪器A的名称是
(2)装置B中品红溶液的作用是
(3)取生铁样品15g,与足量浓硫酸完全反应后无固体剩余。假设产生的
 全部进入装置E中,称得装置E增重2.2g,则该生铁样品中的碳元素含量为
全部进入装置E中,称得装置E增重2.2g,则该生铁样品中的碳元素含量为
您最近一年使用:0次
名校
10 . 某探究小组用碘量法来测定样品中N2H4·H2O的含量。取样品5.000 g,加水配成250 mL无色溶液,已知溶液呈碱性,取25.00 mL溶液,用滴定管盛装0.2000 mol/L的I2标准液进行滴定。滴定反应中氧化产物和还原产物分别为N2和I-。
(1)用_____________ 填“酸式”或“碱式”)滴定管盛装I2标准液,在取液、盛装、滴定过程中还需要的玻璃仪器有_____________________________________ 。
(2)滴定过程中,需要加入_____ 作为指示剂,滴定终点的判断方法___________ 。
(3)滴定前后液面如图所示,所用I2标准液的体积为________________ mL。
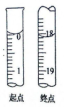
(4)样品中水合肼(N2H4·H2O)的质量分数为_____________________ ,若滴定过程中,盛放I2标准液的滴定管刚开始有气泡,滴定后无气泡,则测得样品中水合肼(N2H4·H2O)的质量分数____________ 填“偏大”、“偏小”或“无影响”)。
(1)用
(2)滴定过程中,需要加入
(3)滴定前后液面如图所示,所用I2标准液的体积为

(4)样品中水合肼(N2H4·H2O)的质量分数为
您最近一年使用:0次
2018-12-13更新
|
204次组卷
|
2卷引用:广西玉林高级中学南校区2021-2022学年高二上学期期中考试理综化学试题



