名校
解题方法
1 . 下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| 选项 | 实验 | 现象 | 结论 |
| A | 将过量铁粉加入稀硝酸中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将Fe氧化为Fe3+ |
| B | 将铜粉加入1.0mol/LFe2(SO4)3溶液中 | 溶液由黄色变为蓝绿(青)色 | 金属铁比铜活泼 |
| C | 向久置的FeCl2溶液中加入酸性KMnO4溶液 | KMnO4溶液紫色褪去 | FeCl2溶液没有完全被氧化 |
| D | 将少量Na2SO3样品溶于足量稀盐酸中,静置,取上层溶液于试管中,滴加BaCl2溶液 | 产生白色沉淀 | 该Na2SO3样品已经变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-06-19更新
|
361次组卷
|
4卷引用:黑龙江省哈尔滨市第九中学2020-2021学年高二下学期6月月考化学试题
黑龙江省哈尔滨市第九中学2020-2021学年高二下学期6月月考化学试题(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)湖南省衡阳师范学院祁东附属中学2021-2022学年高三上学期12月月考化学试题
名校
2 . 据古籍记载,焙烧绿矾( )矿石能制备铁红,同时制得硫酸。某研究性学习小组对绿矾的焙烧反应进行探究,装置如下图所示。
)矿石能制备铁红,同时制得硫酸。某研究性学习小组对绿矾的焙烧反应进行探究,装置如下图所示。

回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加 溶液,无明显现象。再向试管中加入适量
溶液,无明显现象。再向试管中加入适量___________ (填写试剂名称),振荡,溶液变为红色。由此可知该样品___________ (填“已”或“未”)变质。
(2)写出绿矾充分焙烧的过程中只生成一种酸性气体的化学方程式___________ 。
(3)装置 中冷水的作用是
中冷水的作用是___________ 。
(4)为防止倒吸,停止实验时应进行的操作是___________ 。
(5)用 滴定法测定绿矾的纯度。称取
滴定法测定绿矾的纯度。称取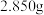 绿矾样品,配制成
绿矾样品,配制成 溶液,量取
溶液,量取 待测液于锥形瓶中,用
待测液于锥形瓶中,用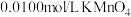 酸性溶液滴定,反应消耗
酸性溶液滴定,反应消耗 酸性溶液体积的平均值为
酸性溶液体积的平均值为 。
。
①配制绿矾样品溶液时需要用到的玻璃仪器是:烧杯、玻璃棒、量筒、___________ 。
②该实验滴定终点时溶液的颜色变为___________ 。
③该绿矾样品中 的质量分数为
的质量分数为___________ (计算结果保留3位有效数字)。
 )矿石能制备铁红,同时制得硫酸。某研究性学习小组对绿矾的焙烧反应进行探究,装置如下图所示。
)矿石能制备铁红,同时制得硫酸。某研究性学习小组对绿矾的焙烧反应进行探究,装置如下图所示。
回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加
 溶液,无明显现象。再向试管中加入适量
溶液,无明显现象。再向试管中加入适量(2)写出绿矾充分焙烧的过程中只生成一种酸性气体的化学方程式
(3)装置
 中冷水的作用是
中冷水的作用是(4)为防止倒吸,停止实验时应进行的操作是
(5)用
 滴定法测定绿矾的纯度。称取
滴定法测定绿矾的纯度。称取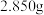 绿矾样品,配制成
绿矾样品,配制成 溶液,量取
溶液,量取 待测液于锥形瓶中,用
待测液于锥形瓶中,用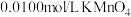 酸性溶液滴定,反应消耗
酸性溶液滴定,反应消耗 酸性溶液体积的平均值为
酸性溶液体积的平均值为 。
。①配制绿矾样品溶液时需要用到的玻璃仪器是:烧杯、玻璃棒、量筒、
②该实验滴定终点时溶液的颜色变为
③该绿矾样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
2021-04-24更新
|
548次组卷
|
5卷引用:黑龙江省大庆铁人中学2021届高三第四次模拟考试化学试题
解题方法
3 . 从下列事实所列出的相应结论正确的是
| 序号 | 实验事实 | 结论 |
| ① | SO2使酸性高锰酸钾溶液褪色 | 可证明SO2有漂白性 |
| ② | 用磨口玻璃瓶保存NaOH溶液,硝酸用棕色试剂瓶保存在阴暗处 | 都发生了氧化还原反应 |
| ③ | 取少量Na2SO3样品加入Ba(NO3)2溶液后,产生白色沉淀滴加稀盐酸,沉淀不溶解, | 证明Na2SO3已氧化变质 |
| ④ | 某溶液加入稀盐酸产生能使澄清石灰水变浑浊的无色无味气体,该溶液滴加CaCl2溶液,有白色沉淀生成 | 确定该溶液存在CO32- |
| ⑤ | 某无色溶液中加入浓氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该溶液一定有NH4+ |
| A.①② | B.③④⑤ | C.②④ | D.④⑤ |
您最近一年使用:0次
2020-01-20更新
|
42次组卷
|
3卷引用:黑龙江绥化市第七中学校2020-2021学年高一下学期第二次月考化学试题
4 . 下列化学实验事实及解释都正确的是
| A.向Na2SO3溶液中加入硝酸酸化的Ba(NO3)2溶液,有白色沉淀出现,说明Na2SO3溶液已经变质 |
| B.向某溶液中加入盐酸产生无色气体,该气体能使澄清石灰水变浑浊,说明该溶液中一定有CO32- |
| C.向某溶液中加入BaCl2溶液,产生白色沉淀,加稀硝酸后,白色沉淀不溶解,说明该溶液中一定含有SO42- |
| D.取少量久置的Na2SO3样品溶于水,加足量盐酸有气体产生,然后加BaCl2溶液,产生白色沉淀,说明Na2SO3样品已部分变质 |
您最近一年使用:0次
2018-12-09更新
|
164次组卷
|
2卷引用:黑龙江省鹤岗市第一中学2020-2021学年高二下学期期末考试化学试题
5 . 下列依据相关实验得出的结论正确的是
| A.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 |
| B.将Fe(NO3)2样品溶于稀盐酸中,然后滴加KSCN溶液,溶液变红,说明Fe(NO3)2样品已氧化变质 |
| C.在食盐试样中加入盐酸和KI溶液,加入淀粉溶液后变蓝,说明食盐试样中可能含有KIO3 |
| D.加入AgNO3溶液后生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有Cl-存在 |
您最近一年使用:0次
2016-12-09更新
|
128次组卷
|
3卷引用:黑龙江省哈尔滨市第七十三中学校2020-2021学年高二下学期期中考试化学试题
名校
6 . 三氯化铬(CrCl3)是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取CrCl3的反应为Cr2O3(s)+3CCl4(g) 2CrCl3(s)+3COCl2(g),其实验装置如下图所示:
2CrCl3(s)+3COCl2(g),其实验装置如下图所示:
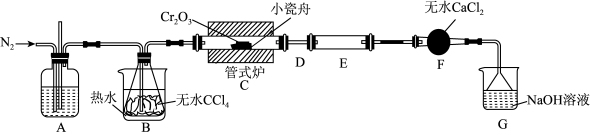
已知:①COC12(俗称光气)有毒,遇水发生水解:COCl2+H2O=CO2+2HCl;
②碱性条件下,H2O2可将Cr3+氧化为 (黄色);酸性条件下,H2O2将
(黄色);酸性条件下,H2O2将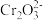 (橙色)还原为Cr3+(绿色)。
(橙色)还原为Cr3+(绿色)。
(1)A装置用于干燥N2和观察其流速,A中的试剂是___________ ;无水CaCl2的作用是___________ ;反应结束后要继续通入一段时间氮气,主要目的是___________ 。
(2)装置E用来收集产物。实验过程中若D处因发生凝华出现堵塞,A装置中可观察到的现象是___________ ;可通过___________ (填操作)使实验继续进行。
(3)尾气与装置G中过量的NaOH溶液发生反应的离子方程式是___________ 。
(4)测定产品中CrCl,质量分数的实验步骤如下:
I.取m g CrCl3产品,在强碱性条件下,加入过量30%H2O2溶液,小火加热使CrCl3完全转化为 ,再继续加热一段时间。
,再继续加热一段时间。
II.冷却后加适量的蒸馏水,再滴入适量的稀硫酸和浓磷酸(浓磷酸作用是分子指示剂提前变色),使 转化为
转化为 。
。
III.在溶液中加入适量浓H2SO4混合均匀,滴入3滴试亚铁灵做指示剂,用新配制的c mol·L-1(NH4)2Fe(SO4)2标准溶液滴定,溶液由黄色经蓝绿色至红褐色即为终点,消耗(NH4)2Fe(SO4)2标准溶液V mL(滴定中 被Fe2+还原为Cr3+)。
被Fe2+还原为Cr3+)。
①产品中CrCl3质量分数表达式为___________ 。
②下列操作将导致产品中CrCl3质量分数测定值偏高的是___________ (填字母标号)。
A.步骤I中未继续加热一段时间
B.步骤III中(NH4)2Fe(SO4)2溶液部分变质
C.步骤II用盐酸替代硫酸
D.步骤III中读数时,滴定前俯视,滴定后平视
 2CrCl3(s)+3COCl2(g),其实验装置如下图所示:
2CrCl3(s)+3COCl2(g),其实验装置如下图所示:
已知:①COC12(俗称光气)有毒,遇水发生水解:COCl2+H2O=CO2+2HCl;
②碱性条件下,H2O2可将Cr3+氧化为
 (黄色);酸性条件下,H2O2将
(黄色);酸性条件下,H2O2将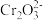 (橙色)还原为Cr3+(绿色)。
(橙色)还原为Cr3+(绿色)。(1)A装置用于干燥N2和观察其流速,A中的试剂是
(2)装置E用来收集产物。实验过程中若D处因发生凝华出现堵塞,A装置中可观察到的现象是
(3)尾气与装置G中过量的NaOH溶液发生反应的离子方程式是
(4)测定产品中CrCl,质量分数的实验步骤如下:
I.取m g CrCl3产品,在强碱性条件下,加入过量30%H2O2溶液,小火加热使CrCl3完全转化为
 ,再继续加热一段时间。
,再继续加热一段时间。II.冷却后加适量的蒸馏水,再滴入适量的稀硫酸和浓磷酸(浓磷酸作用是分子指示剂提前变色),使
 转化为
转化为 。
。III.在溶液中加入适量浓H2SO4混合均匀,滴入3滴试亚铁灵做指示剂,用新配制的c mol·L-1(NH4)2Fe(SO4)2标准溶液滴定,溶液由黄色经蓝绿色至红褐色即为终点,消耗(NH4)2Fe(SO4)2标准溶液V mL(滴定中
 被Fe2+还原为Cr3+)。
被Fe2+还原为Cr3+)。①产品中CrCl3质量分数表达式为
②下列操作将导致产品中CrCl3质量分数测定值偏高的是
A.步骤I中未继续加热一段时间
B.步骤III中(NH4)2Fe(SO4)2溶液部分变质
C.步骤II用盐酸替代硫酸
D.步骤III中读数时,滴定前俯视,滴定后平视
您最近一年使用:0次
2021-10-19更新
|
675次组卷
|
3卷引用:黑龙江省哈尔滨师范大学附属中学2021-2022学年高三上学期期中考试化学试题
名校
解题方法
7 . 有机物H(C9H8O4)是洁面化妆品的中间体,以A为原料合成有机物H的路线如图:
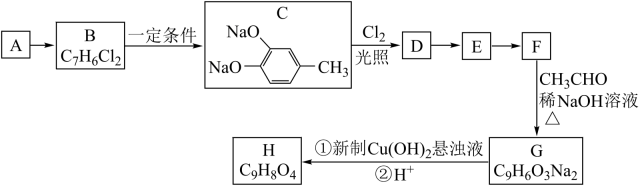
已知:①A是相对分子量为92的芳香烃;
②D是C的一氯取代物;
③RCHO+R1CH2CHO RCH=CR1CHO+H2O(R、R1为烃基或氢原子)。
RCH=CR1CHO+H2O(R、R1为烃基或氢原子)。
回答下列问题:
(1)B的化学名称为___ (用系统命名法)。
(2)由D生成E所用的试剂和反应条件为___ 。
(3)由E生成F的反应类型为___ ,F的结构简式为___ 。
(4)G与新制Cu(OH)2悬浊液反应的化学方程式为___ 。
(5)H长期暴露在空气中容易变质的主要原因是___ 。
(6)X是F酸化后的产物,T是X的芳香族同分异构体,且T能与NaHCO3反应生成CO2,则符合条件的T的结构有___ 种(不包括立体异构),写出其中核磁共振氢谱有6组峰的T的结构简式__ 。
(7)参照上述流程,设计以乙醇为原料制备CH3CH=CHCOOH的合成路线:__ 。(其它无机试剂任选)。

已知:①A是相对分子量为92的芳香烃;
②D是C的一氯取代物;
③RCHO+R1CH2CHO
 RCH=CR1CHO+H2O(R、R1为烃基或氢原子)。
RCH=CR1CHO+H2O(R、R1为烃基或氢原子)。回答下列问题:
(1)B的化学名称为
(2)由D生成E所用的试剂和反应条件为
(3)由E生成F的反应类型为
(4)G与新制Cu(OH)2悬浊液反应的化学方程式为
(5)H长期暴露在空气中容易变质的主要原因是
(6)X是F酸化后的产物,T是X的芳香族同分异构体,且T能与NaHCO3反应生成CO2,则符合条件的T的结构有
(7)参照上述流程,设计以乙醇为原料制备CH3CH=CHCOOH的合成路线:
您最近一年使用:0次
2021-05-05更新
|
642次组卷
|
2卷引用:黑龙江省哈尔滨市第九中学2021届高三第二次模拟考试理科综合化学试题
名校
8 . 下列实验操作、实验现象和实验结论均正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 将少量浓硝酸分多次加入Cu和稀硫酸的混合物中 | 产生红棕色气体 | 硝酸的还原产物为NO2 |
| B | 将少量Fe(NO3)2试样加水溶解后,滴加稀硫酸酸化,再滴加KSCN溶液 | 溶液变成血红色 | Fe(NO3)2试样无法确定是否变质 |
| C | 2滴0.1mol·L-1 MgCl2溶液中滴加2ml 1mol·L-1 NaOH溶液,再滴加2滴0.1 mol·L-1 FeCl3溶液 | 先生成白色沉淀,后生成红褐色沉淀 | Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| D | 将溴乙烷和NaOH乙醇溶液混合加热,产生的气体通入酸性KMnO4溶液 | 酸性KMnO4溶液褪色 | 产生了乙烯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-06-29更新
|
213次组卷
|
3卷引用:黑龙江省哈尔滨市第六中学2020-2021学年高二6月月考化学试题
名校
解题方法
9 . 氧化亚铜(Cu2O)主要用于制造船底防污漆。已知CuO经高温灼烧生成Cu2O,Cu2O与H+发生反应为Cu2O+2H+=Cu+Cu2++H2O。现将经高温灼烧后的CuO样品投入足量稀硫酸中得到混合溶液,有关说法不正确的是
| A.如果溶液中出现蓝色,说明CuO已分解 |
| B.样品与酸反应中Cu2O既为氧化剂又是还原剂 |
| C.高温条件下,稳定性:Cu2O>CuO |
| D.Cu2O+2H+=Cu+Cu2++H2O,该反应中Cu为还原产物 |
您最近一年使用:0次
10 . 酸性KMnO4溶液、H2O2溶液在生活、卫生医疗中常用作消毒剂,其中H2O2还可用于漂白,是化学实验室里必备的重要氧化试剂。高锰酸钾造成的污渍可用还原性的草酸(H2C2O4)去除。FeNO33溶液也是重要的氧化试剂,下面是对这三种氧化试剂性质的探究。
(1)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,写出该反应的离子方程式:_______ ,氧化产物与还原产物的物质的量之比为_______ 。
(2)取300mL0.2molL-1的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则转移电子的物质的量是_______
(3)测定KMnO4样品的纯度可用标准Na2S2O3溶液进行滴定,取0.474克KMnO4样品溶解酸化后,用0.100molL1的标准Na2S2O3溶液进行滴定,标准Na2S2O3溶液应盛装在_________________ (填“酸式”或“碱式”)滴定管中。实验中,滴定至终点时消耗标准Na2S2O3溶液12.00mL,则该样品中KMnO4的物质的量是_______ (有关离子方程式为8 +5
+5 +14H=8Mn2++10
+14H=8Mn2++10 +7H2O)
+7H2O)
(4)在溶FeNO33液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的原因是_______ ,又变为棕黄色的离子方程式是_______ 。
(1)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,写出该反应的离子方程式:
(2)取300mL0.2molL-1的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则转移电子的物质的量是
(3)测定KMnO4样品的纯度可用标准Na2S2O3溶液进行滴定,取0.474克KMnO4样品溶解酸化后,用0.100molL1的标准Na2S2O3溶液进行滴定,标准Na2S2O3溶液应盛装在
 +5
+5 +14H=8Mn2++10
+14H=8Mn2++10 +7H2O)
+7H2O)(4)在溶FeNO33液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的原因是
您最近一年使用:0次



