名校
1 . 室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 取久置的 粉末,向其中滴加过量的盐酸,产生无色气体 粉末,向其中滴加过量的盐酸,产生无色气体 |  粉末没有变质 粉末没有变质 |
| B | 将 样品溶于稀硫酸后,滴加KSCN溶液,溶液变红 样品溶于稀硫酸后,滴加KSCN溶液,溶液变红 |  样品已变质 样品已变质 |
| C | 将 气体通入棕黄色 气体通入棕黄色 溶液,溶液变为浅绿色 溶液,溶液变为浅绿色 |  具有还原性 具有还原性 |
| D | 把 和气体X一起通入到 和气体X一起通入到 溶液中,有白色沉淀产生 溶液中,有白色沉淀产生 | X气体具有强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-09更新
|
355次组卷
|
2卷引用:黑龙江省哈尔滨市第三中学校2023-2024学年 高一下学期第一次验收考试化学试题
名校
2 . 下列实验的实验操作、现象及所得到的结论均正确的是
选项 | 实验操作 | 现象和结论 |
A | 取少量硫代硫酸钠样品溶于水,先加入过量稀盐酸,再滴加 溶液 溶液 | 有沉淀生成,则硫代硫酸钠已变质生成了硫酸钠 |
B | 向 溶液中加入醋酸,将产生的气体通入苯酚钠水溶液中 溶液中加入醋酸,将产生的气体通入苯酚钠水溶液中 | 观察到苯酚钠溶液变浑浊,则碳酸的酸性强于苯酚 |
C | 常温下,测定 溶液酸碱性 溶液酸碱性 | 若溶液呈碱性,则 为弱酸 为弱酸 |
D | 相同温度下,向含有NaCl、NaBr的混合溶液中逐滴加入 溶液 溶液 | 先出现淡黄色沉淀,则 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-29更新
|
479次组卷
|
2卷引用:黑龙江省哈尔滨市第三中学校2023-2024学年高三一模化学试题
名校
解题方法
3 . 氯化亚铜(CuCl)广泛用于冶金、电镀、医药等行业。已知CuCl难溶于水和乙醇,在潮湿空气中易变质。学习小组开展了与CuCl相关的系列实验。回答下列问题:
Ⅰ.利用废铜屑制备 ,实验装置如图所示。
,实验装置如图所示。_______ 。
(2)三颈烧瓶中制备 的化学方程式为
的化学方程式为____ ,将浓盐酸加入三颈烧瓶的操作为:____ ,再将分液漏斗下面的活塞打开。
Ⅱ.制备氯化亚铜,制备流程如图所示:
(3)反应①中氧化剂与还原剂的物质的量之比为_______ ,操作②为_______ 。
(4)析出的CuCl粗产品不用盐酸而用水、乙醇分别洗涤的目的依次是_____ 、_______ 。
(5)测定产品中CuCl的质量分数。准确称取制备的CuCl产品0.40g,加入足量的氯化铁溶液,待样品全部溶解后,加入适量稀硫酸,用 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液24.00mL,反应中
溶液24.00mL,反应中 被还原为
被还原为 ,产品中CuCl的质量分数为
,产品中CuCl的质量分数为_____ (保留四位有效数字)。
Ⅰ.利用废铜屑制备
 ,实验装置如图所示。
,实验装置如图所示。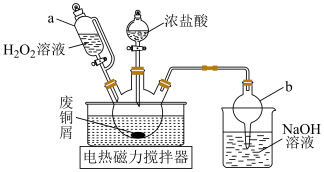
(2)三颈烧瓶中制备
 的化学方程式为
的化学方程式为Ⅱ.制备氯化亚铜,制备流程如图所示:


(3)反应①中氧化剂与还原剂的物质的量之比为
(4)析出的CuCl粗产品不用盐酸而用水、乙醇分别洗涤的目的依次是
(5)测定产品中CuCl的质量分数。准确称取制备的CuCl产品0.40g,加入足量的氯化铁溶液,待样品全部溶解后,加入适量稀硫酸,用
 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液24.00mL,反应中
溶液24.00mL,反应中 被还原为
被还原为 ,产品中CuCl的质量分数为
,产品中CuCl的质量分数为
您最近一年使用:0次
4 . 下列有关实验、现象及结论等叙述正确的个数有
①向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀,X具有强氧化性
②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有Fe2+
④向饱和NaHCO3溶液中滴加硼酸,无气泡产生,酸性:硼酸<碳酸
⑤取少量Fe(NO3)2样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
⑥除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶
①向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀,X具有强氧化性
②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有Fe2+
④向饱和NaHCO3溶液中滴加硼酸,无气泡产生,酸性:硼酸<碳酸
⑤取少量Fe(NO3)2样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
⑥除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
2024-04-19更新
|
299次组卷
|
2卷引用:黑龙江省大庆铁人中学2023-2024学年高一下学期开学考试化学试题
名校
5 . 下列实验操作、现象和所得到的结论均正确的是
| 选项 | 实验内容 | 实验结论 |
| A | 将Fe(NO3)2样品溶于稀HNO3溶液中,加入KSCN溶液,显红色 | Fe(NO3)2已经氧化变质 |
| B | 用pH试纸测定同浓度的NaCl和NaF溶液的pH,pH(NaCl)<pH(NaF) | 结合H+能力:Cl-<F- |
| C | 取1mL0.1mol/LKI溶液于试管中,加入5mL0.1mol/LFeCl3,充分反应后滴入5滴15%KSCN溶液 | 若溶液变血红色,则KI和FeCl3反应有一定限度 |
| D | 向2支盛有5mL不同浓度NaHSO3溶液的试管中,同时加入2mL5%H2O2溶液,观察并比较实验现象 | 探究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-02-23更新
|
220次组卷
|
3卷引用:黑龙江省哈尔滨市第一中学校2023-2024学年高二上学期期末考试化学试卷
名校
解题方法
6 . 三氯化钌 是重要的化工原料,广泛应用于催化、电镀、电解阳极、电子工业等。从
是重要的化工原料,广泛应用于催化、电镀、电解阳极、电子工业等。从 催化剂废料中分离制备
催化剂废料中分离制备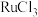 和
和 的一种工艺流程如图所示。
的一种工艺流程如图所示。 、
、 分别转化为
分别转化为 、
、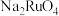 。
。
回答下列问题:
(1)下列状态的钴中,电离最外层一个电子所需能量最大的是___________(填序号)
(2)“还原”过程会产生 和
和 沉淀,则氧化产物和还原产物的物质的量之比为
沉淀,则氧化产物和还原产物的物质的量之比为___________ 。
(3)“酸溶”过程中,先加入盐酸溶解 ,然后加入盐酸羟胺
,然后加入盐酸羟胺 得到
得到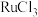 和
和 。则盐酸羟胺
。则盐酸羟胺 与
与 反应的化学方程式为
反应的化学方程式为___________ 。
(4)若维持 不变,让
不变,让 沉淀完全(
沉淀完全( 浓度不高于
浓度不高于 ),则混合体系中
),则混合体系中 的浓度不低于
的浓度不低于___________ 。[已知: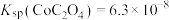 ,
, ,
, 结果保留三位小数]
结果保留三位小数]
(5)该流程中,还有一种重要成分 未提取,你认为在哪一步骤后进行最合适:
未提取,你认为在哪一步骤后进行最合适:___________ 。(填工序名称)
(6)沉钴过程中得到的主要成分是 。为测定草酸钴晶体的纯度,进行如下实验:
。为测定草酸钴晶体的纯度,进行如下实验:
①取草酸钴样品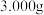 ,加入
,加入 酸性
酸性 溶液,加热充分反应至不再有
溶液,加热充分反应至不再有 气体产生(该条件下
气体产生(该条件下 不被氧化,杂质不参与反应)。
不被氧化,杂质不参与反应)。
②将溶液冷却,加水稀释定容至 。
。
③取 溶液,用
溶液,用 溶液滴定过量的
溶液滴定过量的 ,恰好完全反应时消耗
,恰好完全反应时消耗 溶液。
溶液。
Ⅰ.样品中 的质量分数为
的质量分数为___________ 。
Ⅱ.下列实验操作可能使测定结果偏低的是___________ 。
A. 标准溶液放置时间过长
标准溶液放置时间过长
B.锥形瓶水洗后未用待测液润洗
C.读数时,滴定前平视,滴定后俯视
D.由于操作不规范,滴定前无气泡,滴定后产生气泡
 是重要的化工原料,广泛应用于催化、电镀、电解阳极、电子工业等。从
是重要的化工原料,广泛应用于催化、电镀、电解阳极、电子工业等。从 催化剂废料中分离制备
催化剂废料中分离制备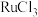 和
和 的一种工艺流程如图所示。
的一种工艺流程如图所示。
 、
、 分别转化为
分别转化为 、
、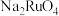 。
。回答下列问题:
(1)下列状态的钴中,电离最外层一个电子所需能量最大的是___________(填序号)
A. | B. | C. | D. |
(2)“还原”过程会产生
 和
和 沉淀,则氧化产物和还原产物的物质的量之比为
沉淀,则氧化产物和还原产物的物质的量之比为(3)“酸溶”过程中,先加入盐酸溶解
 ,然后加入盐酸羟胺
,然后加入盐酸羟胺 得到
得到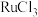 和
和 。则盐酸羟胺
。则盐酸羟胺 与
与 反应的化学方程式为
反应的化学方程式为(4)若维持
 不变,让
不变,让 沉淀完全(
沉淀完全( 浓度不高于
浓度不高于 ),则混合体系中
),则混合体系中 的浓度不低于
的浓度不低于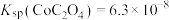 ,
, ,
, 结果保留三位小数]
结果保留三位小数](5)该流程中,还有一种重要成分
 未提取,你认为在哪一步骤后进行最合适:
未提取,你认为在哪一步骤后进行最合适:(6)沉钴过程中得到的主要成分是
 。为测定草酸钴晶体的纯度,进行如下实验:
。为测定草酸钴晶体的纯度,进行如下实验:①取草酸钴样品
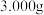 ,加入
,加入 酸性
酸性 溶液,加热充分反应至不再有
溶液,加热充分反应至不再有 气体产生(该条件下
气体产生(该条件下 不被氧化,杂质不参与反应)。
不被氧化,杂质不参与反应)。②将溶液冷却,加水稀释定容至
 。
。③取
 溶液,用
溶液,用 溶液滴定过量的
溶液滴定过量的 ,恰好完全反应时消耗
,恰好完全反应时消耗 溶液。
溶液。Ⅰ.样品中
 的质量分数为
的质量分数为Ⅱ.下列实验操作可能使测定结果偏低的是
A.
 标准溶液放置时间过长
标准溶液放置时间过长B.锥形瓶水洗后未用待测液润洗
C.读数时,滴定前平视,滴定后俯视
D.由于操作不规范,滴定前无气泡,滴定后产生气泡
您最近一年使用:0次
名校
解题方法
7 . 5.76g某部分氧化的Fe、Cu合金样品(氧化产物为 、CuO),经如下处理,下列说法正确的是
、CuO),经如下处理,下列说法正确的是

 、CuO),经如下处理,下列说法正确的是
、CuO),经如下处理,下列说法正确的是
| A.V=448 |
| B.样品中Fe元素的质量为2.14g |
| C.未氧化前Fe元素的质量分数约为38.89% |
| D.样品中CuO的质量为3.52g |
您最近一年使用:0次
名校
8 . 某同学推测钠能与 反应,进行如下探究:
反应,进行如下探究:
【实验】将燃烧的钠迅速伸入盛满 的集气瓶中,发现钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
的集气瓶中,发现钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
(1)瓶底附着黑色颗粒是___________ ,若反应生成0.06g该黑色颗粒,消耗钠质量为___________ g。
【提出假设】假设1:白色物质是
假设2:白色物质是
假设3:白色物质是。
(2)丙同学认为白色物质有可能是氢氧化钠。你是否同意丙同学的观点,并简述理由:___________ 。
【设计实验方案·验证假设】该小组对燃烧后的白色产物进行如下探究:
(3)甲同学认为方案1得到的结论不正确,其理由是:___________ 。
(4)乙同学认为方案2得到的结论正确,加入试剂为___________ 溶液,由此得出白色物质为___________ 。
(5)根据实验探究钠在二氧化碳中燃烧的化学方程式为:___________ ,则反应生成0.06g黑色颗粒时消耗的 在标准状况下的体积
在标准状况下的体积___________ mL。
 反应,进行如下探究:
反应,进行如下探究:【实验】将燃烧的钠迅速伸入盛满
 的集气瓶中,发现钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
的集气瓶中,发现钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。(1)瓶底附着黑色颗粒是
【提出假设】假设1:白色物质是

假设2:白色物质是

假设3:白色物质是。
(2)丙同学认为白色物质有可能是氢氧化钠。你是否同意丙同学的观点,并简述理由:
【设计实验方案·验证假设】该小组对燃烧后的白色产物进行如下探究:
| 方案 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变红色 | 白色物质为 |
| 2 | ①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入X溶液 | 出现白色沉淀 | |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
(4)乙同学认为方案2得到的结论正确,加入试剂为
(5)根据实验探究钠在二氧化碳中燃烧的化学方程式为:
 在标准状况下的体积
在标准状况下的体积
您最近一年使用:0次



