1 . 铝电解厂烟气净化的一种简单流程如下:
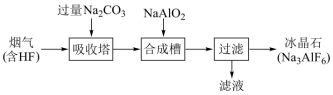
| A.不宜用陶瓷作吸收塔内衬材料 |
| B.采用溶液喷淋法可提高吸收塔内烟气吸收效率 |
| C.从吸收塔进入合成槽中的反应物为NaF |
| D.滤液可回收进入吸收塔循环利用 |
您最近一年使用:0次
名校
解题方法
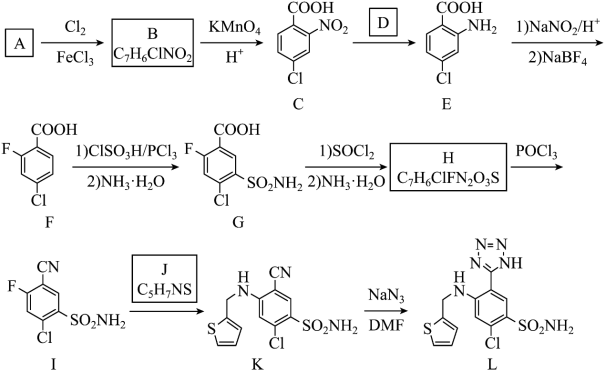
2 . 阿佐塞米(化合物L)是一种可用于治疗心脏、肝脏和肾脏病引起的水肿的药物。L的一种合成路线如下(部分试剂和条件略去)。 R-COCl
R-COCl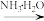 R-CONH2
R-CONH2
回答下列问题:
(1)A的化学名称是_______ ,B的结构简式为_______ 。
(2)反应条件D应选择_______ (填标号),反应类型为_______ 。
a.HNO3/H2SO4 b.Fe/HCl c.NaOH/C2H5OH d.AgNO3/NH3
(3)F中含氧官能团的名称是_______ 。
(4)H生成I的反应类型为_______ 。
(5)I和J生成K的化学方程为_______ 。
(6)与B具有相同官能团,且苯环上有两个取代基的芳香同分异构体有_______ 种(不考虑立体异构);与B具有相同官能团,核磁共振氢谱显示4组峰,且峰面积比为2:2:1:1的同分异构体结构简式为_______ 。
 R-COCl
R-COCl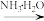 R-CONH2
R-CONH2回答下列问题:
(1)A的化学名称是
(2)反应条件D应选择
a.HNO3/H2SO4 b.Fe/HCl c.NaOH/C2H5OH d.AgNO3/NH3
(3)F中含氧官能团的名称是
(4)H生成I的反应类型为
(5)I和J生成K的化学方程为
(6)与B具有相同官能团,且苯环上有两个取代基的芳香同分异构体有
您最近一年使用:0次
名校
解题方法
3 . 亚硝酰氯NOCl常用于合成洗涤剂、触媒及用作中间体,是一种红褐色液体或黄色气体,其熔点-64.5℃,沸点-5.5℃,遇水易水解。某学习小组在实验室用Cl2与NO制备NOCl并测定其纯度。
(1)若用KClO3和浓盐酸制取Cl2反应的离子方程式为_______ 。
(2)NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为_______ 。
(3)利用制得的NO和Cl2制备NOCl,装置如图所示 (夹持装置略去):_______ (按气流自左向右方向,用小写字母表示)。
②装置I、Ⅱ除可进一步干燥NO、Cl2外,另一个作用是_______ 。
③装置VI在实验时可观察到的现象是_______ 。
④若不用装置Ⅳ中的干燥管对实验有何影响_______ (用化学方程式表示)。
(4)亚硝酰氯NOCl纯度的测定 (假设杂质不参与反应):取VI中所得液体100g溶于NaOH溶液中,然后加入一定量稀硫酸和KI,并通入足量N2,将NO全部赶出,最后将溶液稀释至250.00mL;取出25.00mL样品溶于锥形瓶中,用淀粉作指示剂,用c mol·L-1 Na2S2O3标准溶液滴定至终点,最终消耗标准溶液的体积为20.00mL。
已知:2NO +4H++2Ⅰ-=2NO+Ⅰ2+2H2O;Ⅰ2+2S2O
+4H++2Ⅰ-=2NO+Ⅰ2+2H2O;Ⅰ2+2S2O =S4O
=S4O +2Ⅰ-
+2Ⅰ-
①滴定终点的现象:当滴入最后半滴标准溶液后,_______ 。
②亚硝酰氯(NOCl)的质量分数为_______  。(用含c的代数式表示)
。(用含c的代数式表示)
(1)若用KClO3和浓盐酸制取Cl2反应的离子方程式为
(2)NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为
(3)利用制得的NO和Cl2制备NOCl,装置如图所示 (夹持装置略去):
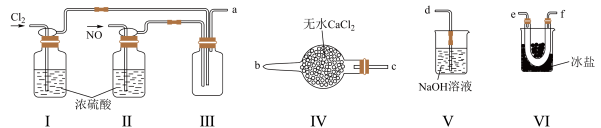
②装置I、Ⅱ除可进一步干燥NO、Cl2外,另一个作用是
③装置VI在实验时可观察到的现象是
④若不用装置Ⅳ中的干燥管对实验有何影响
(4)亚硝酰氯NOCl纯度的测定 (假设杂质不参与反应):取VI中所得液体100g溶于NaOH溶液中,然后加入一定量稀硫酸和KI,并通入足量N2,将NO全部赶出,最后将溶液稀释至250.00mL;取出25.00mL样品溶于锥形瓶中,用淀粉作指示剂,用c mol·L-1 Na2S2O3标准溶液滴定至终点,最终消耗标准溶液的体积为20.00mL。
已知:2NO
 +4H++2Ⅰ-=2NO+Ⅰ2+2H2O;Ⅰ2+2S2O
+4H++2Ⅰ-=2NO+Ⅰ2+2H2O;Ⅰ2+2S2O =S4O
=S4O +2Ⅰ-
+2Ⅰ-①滴定终点的现象:当滴入最后半滴标准溶液后,
②亚硝酰氯(NOCl)的质量分数为
 。(用含c的代数式表示)
。(用含c的代数式表示)
您最近一年使用:0次
名校
解题方法
4 . LiMn2O4、LiFePO4是锂离子电池常用的活性材料。某小组以含锰矿料(主要成分是MnCO3,含少量Fe2O3、Fe3O4、FeO、CoO和SiO2)为原料制备LiMn2O4的流程如图所示(部分条件和产物省略)。
(1)提高“酸浸”速率的措施为_______ (写一条即可)。
(2)“除杂1”时,加入MnO2的作用是_______ (用离子方程式表示)。
(3)要使“固体1”中除了含有MnO2外,只含另外一种固体,其化学式为_______ ,则“除杂1”过程调节pH范围为_______ 。
(4)在高温下“合成”LiMn2O4,反应的化学方程式为_______ 。
(5)已知:常温下,Ksp(CoS)=3.0 × 10−26、Ksp(MnS)=3.0 × 10−14。假设“除杂1”后的溶液中c( )为 0.1mol·L-1,为了使残液中 c(Co2 + )≤ 1.0 × 10−5 mol·L-1,必须控制c(S2−) 的范围为
)为 0.1mol·L-1,为了使残液中 c(Co2 + )≤ 1.0 × 10−5 mol·L-1,必须控制c(S2−) 的范围为_______ mol·L-1。
(6)工业上,制备高纯Li2CO3是向LiOH溶液中加入少量NH4HCO3溶液并共热,过滤、烘干得高纯Li2CO3,生成Li2CO3反应的化学方程式是_______ 。
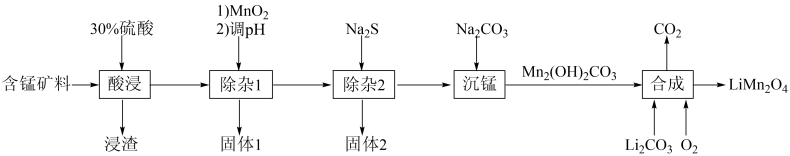
| 金属氢氧化物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Mn(OH)2 |
开始沉淀的pH | 2.7 | 7.5 | 7.6 | 7.8 |
完全沉淀的pH | 3.7 | 9.7 | 9.2 | 10.4 |
(1)提高“酸浸”速率的措施为
(2)“除杂1”时,加入MnO2的作用是
(3)要使“固体1”中除了含有MnO2外,只含另外一种固体,其化学式为
(4)在高温下“合成”LiMn2O4,反应的化学方程式为
(5)已知:常温下,Ksp(CoS)=3.0 × 10−26、Ksp(MnS)=3.0 × 10−14。假设“除杂1”后的溶液中c(
 )为 0.1mol·L-1,为了使残液中 c(Co2 + )≤ 1.0 × 10−5 mol·L-1,必须控制c(S2−) 的范围为
)为 0.1mol·L-1,为了使残液中 c(Co2 + )≤ 1.0 × 10−5 mol·L-1,必须控制c(S2−) 的范围为(6)工业上,制备高纯Li2CO3是向LiOH溶液中加入少量NH4HCO3溶液并共热,过滤、烘干得高纯Li2CO3,生成Li2CO3反应的化学方程式是
您最近一年使用:0次
名校
解题方法
5 . 以菱镁矿(主要成分为MgCO3,含少量SiO2、Fe2O3和Al2O3)为原料制备高纯镁砂的工艺流程如下:
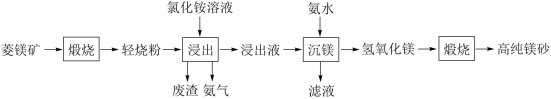
| A.煅烧时将菱镁矿粉碎,有利于加快反应速率 |
| B.浸出镁的反应为MgO+2NH4Cl = MgCl2+2NH3↑+H2O |
| C.流程中可循环使用的物质有NH3、NH4Cl |
| D.将反应温度调控在高温条件下进行浸出和沉镁操作,均有利于提高镁元素的转化率 |
您最近一年使用:0次
名校
解题方法
6 . 碘化钾为白色固体,可用作分析试剂、感光材料、制药和食品添加剂等,可通过碘酸钾与硫化氢反应制备。实验装置如图所示(夹持及加热装置已省略),下列说法错误的是
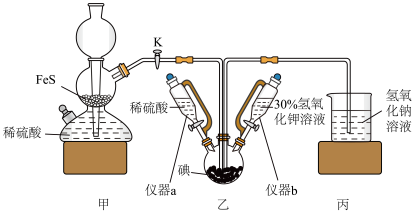
| A.仪器a、b名称是恒压滴液漏斗,实验中应先关闭K,打开仪器b,制备碘酸钾 |
| B.滴入30%氢氧化钾溶液后,乙装置中紫黑色固体溶解,棕黄色溶液逐渐变为无色 |
| C.如果乙装置中最终生成4.8g黄色沉淀,则理论上可制得碘化钾的质量为49.8g |
| D.待乙装置溶液变为无色后,接下来操作应该是打开K和仪器a,稀硫酸的作用仅是提供酸性条件促进碘酸钾与硫化氢氧化还原反应的发生 |
您最近一年使用:0次
名校
解题方法
7 . 某学习小组探究铁丝(含杂质碳)与浓硫酸(沸点:338℃)的反应,反应装置如下图。

| A.无法直接使用pH试纸来判断反应后硫酸是否剩余 |
| B.可用KSCN和K3[Fe(CN)6]检验反应后溶液中铁元素的价态 |
| C.生成的气体通入BaCl2溶液产生白色浑浊,说明一定是部分SO2被氧化所致 |
| D.将22.4mL(标准状况下)反应生成的气体通入足量氯水中,再滴加足量BaCl2溶液,最终得到沉淀质量小于0.233g,说明反应后得到的是混合气体 |
您最近一年使用:0次
名校
解题方法
8 . 室温下,下列实验探究方案不能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向一定量的无水乙醇中加入足量Na,测量生成气体的体积 | Na能置换出醇羟基中的氢 |
| B | 向盛有SO2水溶液的试管中滴加几滴品红溶液,振荡,加热试管,观察溶液颜色变化 | SO2具有漂白性 |
| C | 向盛有淀粉-KI溶液的试管中滴加几滴溴水,振荡,观察溶液颜色变化 | Br2的氧化性比I2的强 |
| D | 将Fe(NO3)2晶体溶于稀硫酸后滴加KSCN溶液,观察到溶液变红 | Fe(NO3)2晶体已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 下列叙述正确的是
| A.浓硫酸具有强吸水性,能吸收糖类化合物中的水分并使其炭化 |
| B.1mol SO3与1mol NO2分别通入1L水中可产生相同浓度的H2SO4和HNO3 |
| C.NaClO、KClO3等含氯的含氧酸盐的氧化性会随溶液的pH减小而增强 |
| D.0.1mol/L醋酸和0.1mol/L硼酸分别加入适量Na2CO3中均可得到CO2和H2O |
您最近一年使用:0次
名校
解题方法
10 . 下列物质混合后,因发生氧化还原反应使溶液 减小的是
减小的是
 减小的是
减小的是| A.向NaHSO4溶液中加入少量BaCl2溶液,生成白色沉淀 |
| B.向浓硝酸溶液中加入铜粉,产生红棕色气体 |
| C.向NaHCO3溶液中加入少量CuSO4溶液,生成蓝绿色沉淀Cu2(OH)2CO3 |
| D.向H2S溶液中通入氯气,生成黄色沉淀 |
您最近一年使用:0次



