1 . 根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计或结论不正确 的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
| A | 探究 和浓 和浓 反应后溶液呈绿色的原因 反应后溶液呈绿色的原因 | 将 通入下列溶液至饱和: 通入下列溶液至饱和:①浓  ②  和HNO3,混合溶液 和HNO3,混合溶液 | ①无色变黄色 ②蓝色变绿色 |  和浓 和浓 反应后溶液呈绿色的主要原因是溶有 反应后溶液呈绿色的主要原因是溶有 |
| B | 比较 与 与 结合 结合 的能力 的能力 | 向等物质的量浓度的 和 和 混合溶液中滴加几滴 混合溶液中滴加几滴 溶液,振荡 溶液,振荡 | 溶液颜色无明显变化 | 结合 的能力: 的能力: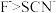 |
| C | 比较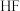 与 与 的酸性 的酸性 | 分别测定等物质的量浓度的 与 与 溶液的 溶液的 | 前者 小 小 | 酸性: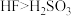 |
| D | 探究温度对反应速率的影响 | 等体积、等物质的量浓度的 与 与 溶液在不同温度下反应 溶液在不同温度下反应 | 温度高的溶液中先出现浑浊 | 温度升高,该反应速率加快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-02更新
|
3391次组卷
|
6卷引用:2024年浙江高考真题化学(1月)
2024年浙江高考真题化学(1月)浙江省余姚中学2023-2024学年高二下学期3月质量检测化学试题(已下线)通关练03 常考化学实验基础知识-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)山东省青岛一中2023-2024学年高二下学期第二次月考化学试卷 (已下线)选择题11-16(已下线)2024年高考化学真题完全解读(浙江1月卷)(讲义+课件)
真题
2 . 仅用下表提供的试剂和用品,不能 实现相应实验目的的是
| 选项 | 实验目的 | 试剂 | 用品 |
| A | 比较镁和铝的金属性强弱 |  溶液、 溶液、 溶液、氨水 溶液、氨水 | 试管、胶头滴管 |
| B | 制备乙酸乙酯 | 乙醇、乙酸、浓硫酸、饱和 溶液 溶液 | 试管、橡胶塞、导管、乳胶管铁架台(带铁夹)、碎瓷片、酒精灯、火柴 |
| C | 制备 溶液 溶液 |  溶液、氨水 溶液、氨水 | 试管、胶头滴管 |
| D | 利用盐类水解制备 胶体 胶体 | 饱和 溶液、蒸馏水 溶液、蒸馏水 | 烧杯、胶头滴管、石棉网、三脚架、酒精灯、火柴 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
真题
解题方法
3 . 测定铁矿石中铁含量的传统方法是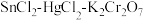 ,滴定法。研究小组用该方法测定质量为
,滴定法。研究小组用该方法测定质量为 的某赤铁矿试样中的铁含量。
的某赤铁矿试样中的铁含量。
【配制溶液】
①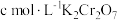 标准溶液。
标准溶液。
② 溶液:称取
溶液:称取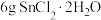 溶于
溶于 浓盐酸,加水至
浓盐酸,加水至 ,加入少量锡粒。
,加入少量锡粒。
【测定含量】按下图所示(加热装置路去)操作步骤进行实验。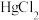 ,可将
,可将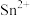 氧化为
氧化为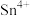 。难以氧化
。难以氧化 ;
; 可被
可被 还原为
还原为 。回答下列问题:
。回答下列问题:
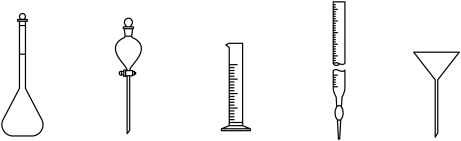
(1)下列仪器在本实验中必须用到的有_______ (填名称)。 溶液时加入锡粒的原因:
溶液时加入锡粒的原因:_______ 。
(3)步骤I中“微热”的原因是_______ 。
(4)步琛Ⅲ中,若未“立即滴定”,则会导致测定的铁含量_______ (填“偏大”“偏小”或“不变”)。
(5)若消耗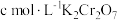 标准溶液
标准溶液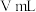 ,则
,则 试样中
试样中 的质量分数为
的质量分数为_______ (用含a、c、V的代数式表示)。
(6)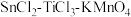 滴定法也可测定铁的含量,其主要原理是利用
滴定法也可测定铁的含量,其主要原理是利用 和
和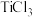 将铁矿石试样中
将铁矿石试样中 还原为
还原为 ,再用
,再用 标准溶液滴定。
标准溶液滴定。
①从环保角度分析,该方法相比于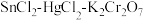 ,滴定法的优点是
,滴定法的优点是_______ 。
②为探究 溶液滴定时,
溶液滴定时, 在不同酸度下对
在不同酸度下对 测定结果的影响,分别向下列溶液中加入1滴
测定结果的影响,分别向下列溶液中加入1滴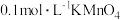 溶液,现象如下表:
溶液,现象如下表:
表中试剂X为_______ ;根据该实验可得出的结论是_______ 。
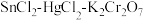 ,滴定法。研究小组用该方法测定质量为
,滴定法。研究小组用该方法测定质量为 的某赤铁矿试样中的铁含量。
的某赤铁矿试样中的铁含量。【配制溶液】
①
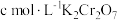 标准溶液。
标准溶液。②
 溶液:称取
溶液:称取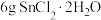 溶于
溶于 浓盐酸,加水至
浓盐酸,加水至 ,加入少量锡粒。
,加入少量锡粒。【测定含量】按下图所示(加热装置路去)操作步骤进行实验。
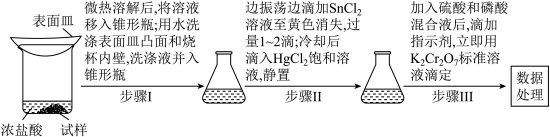
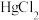 ,可将
,可将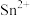 氧化为
氧化为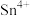 。难以氧化
。难以氧化 ;
; 可被
可被 还原为
还原为 。回答下列问题:
。回答下列问题:(1)下列仪器在本实验中必须用到的有
 溶液时加入锡粒的原因:
溶液时加入锡粒的原因:(3)步骤I中“微热”的原因是
(4)步琛Ⅲ中,若未“立即滴定”,则会导致测定的铁含量
(5)若消耗
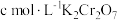 标准溶液
标准溶液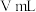 ,则
,则 试样中
试样中 的质量分数为
的质量分数为(6)
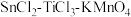 滴定法也可测定铁的含量,其主要原理是利用
滴定法也可测定铁的含量,其主要原理是利用 和
和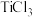 将铁矿石试样中
将铁矿石试样中 还原为
还原为 ,再用
,再用 标准溶液滴定。
标准溶液滴定。①从环保角度分析,该方法相比于
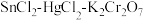 ,滴定法的优点是
,滴定法的优点是②为探究
 溶液滴定时,
溶液滴定时, 在不同酸度下对
在不同酸度下对 测定结果的影响,分别向下列溶液中加入1滴
测定结果的影响,分别向下列溶液中加入1滴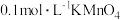 溶液,现象如下表:
溶液,现象如下表:| 溶液 | 现象 | |
| 空白实验 | 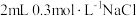 溶液 溶液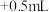 试剂X 试剂X | 紫红色不褪去 |
| 实验I | 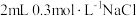 溶液 溶液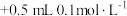 硫酸 硫酸 | 紫红色不褪去 |
| 实验ⅱ | 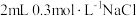 溶液 溶液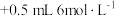 硫酸 硫酸 | 紫红色明显变浅 |
您最近一年使用:0次
真题
解题方法
4 . 市售的溴(纯度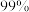 )中含有少量的
)中含有少量的 和
和 ,某化学兴趣小组利用氧化还原反应原理,设计实验制备高纯度的溴。回答下列问题:
,某化学兴趣小组利用氧化还原反应原理,设计实验制备高纯度的溴。回答下列问题:
(1)装置如图(夹持装置等略),将市售的溴滴入盛有浓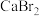 溶液的B中,水浴加热至不再有红棕色液体馏出。仪器C的名称为
溶液的B中,水浴加热至不再有红棕色液体馏出。仪器C的名称为_______ ;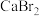 溶液的作用为
溶液的作用为_______ ;D中发生的主要反应的化学方程式为_______ 。_______ (填仪器名称)中,边加热边向其中滴加酸化的 溶液至出现红棕色气体,继续加热将溶液蒸干得固体R。该过程中生成
溶液至出现红棕色气体,继续加热将溶液蒸干得固体R。该过程中生成 的离子方程式为
的离子方程式为_______ 。
(3)利用图示相同装置,将R和 固体混合均匀放入B中,D中加入冷的蒸馏水。由A向B中滴加适量浓
固体混合均匀放入B中,D中加入冷的蒸馏水。由A向B中滴加适量浓 ,水浴加热蒸馏。然后将D中的液体分液、干燥、蒸馏,得到高纯度的溴。D中蒸馏水的作用为
,水浴加热蒸馏。然后将D中的液体分液、干燥、蒸馏,得到高纯度的溴。D中蒸馏水的作用为_______ 和_______ 。
(4)为保证溴的纯度,步骤(3)中 固体的用量按理论所需量的
固体的用量按理论所需量的 计算,若固体R质量为m克(以
计算,若固体R质量为m克(以 计),则需称取
计),则需称取_______ 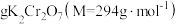 (用含m的代数式表示)。
(用含m的代数式表示)。
(5)本实验所用钾盐试剂均经重结晶的方法纯化。其中趁热过滤的具体操作为漏斗下端管口紧靠烧杯内壁,转移溶液时用_______ ,滤液沿烧杯壁流下。
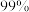 )中含有少量的
)中含有少量的 和
和 ,某化学兴趣小组利用氧化还原反应原理,设计实验制备高纯度的溴。回答下列问题:
,某化学兴趣小组利用氧化还原反应原理,设计实验制备高纯度的溴。回答下列问题:(1)装置如图(夹持装置等略),将市售的溴滴入盛有浓
 溶液的B中,水浴加热至不再有红棕色液体馏出。仪器C的名称为
溶液的B中,水浴加热至不再有红棕色液体馏出。仪器C的名称为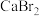 溶液的作用为
溶液的作用为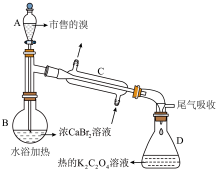
 溶液至出现红棕色气体,继续加热将溶液蒸干得固体R。该过程中生成
溶液至出现红棕色气体,继续加热将溶液蒸干得固体R。该过程中生成 的离子方程式为
的离子方程式为(3)利用图示相同装置,将R和
 固体混合均匀放入B中,D中加入冷的蒸馏水。由A向B中滴加适量浓
固体混合均匀放入B中,D中加入冷的蒸馏水。由A向B中滴加适量浓 ,水浴加热蒸馏。然后将D中的液体分液、干燥、蒸馏,得到高纯度的溴。D中蒸馏水的作用为
,水浴加热蒸馏。然后将D中的液体分液、干燥、蒸馏,得到高纯度的溴。D中蒸馏水的作用为(4)为保证溴的纯度,步骤(3)中
 固体的用量按理论所需量的
固体的用量按理论所需量的 计算,若固体R质量为m克(以
计算,若固体R质量为m克(以 计),则需称取
计),则需称取 (用含m的代数式表示)。
(用含m的代数式表示)。(5)本实验所用钾盐试剂均经重结晶的方法纯化。其中趁热过滤的具体操作为漏斗下端管口紧靠烧杯内壁,转移溶液时用
您最近一年使用:0次
5 . 通过电化学、热化学等方法,将 转化为
转化为 等化学品,是实现“双碳”目标的途径之一。请回答:
等化学品,是实现“双碳”目标的途径之一。请回答:
(1)某研究小组采用电化学方法将 转化为
转化为 ,装置如图。电极B上的电极反应式是
,装置如图。电极B上的电极反应式是_______ 。
 :
: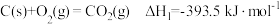
Ⅱ:
Ⅲ: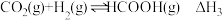
①
_______  。
。
②反应Ⅲ在恒温、恒容的密闭容器中进行, 和
和 的投料浓度均为
的投料浓度均为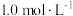 ,平衡常数
,平衡常数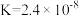 ,则
,则 的平衡转化率为
的平衡转化率为_______ 。
③用氨水吸收 ,得到
,得到 氨水和
氨水和 甲酸铵的混合溶液,
甲酸铵的混合溶液,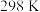 时该混合溶液的
时该混合溶液的
_______ 。[已知: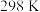 时,电离常数
时,电离常数 、
、 ]
]
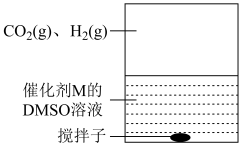
(3)为提高效率,该研究小组参考文献优化热化学方法,在如图密闭装置中充分搅拌催化剂M的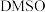 (有机溶剂)溶液,
(有机溶剂)溶液, 和
和 在溶液中反应制备
在溶液中反应制备 ,反应过程中保持
,反应过程中保持 和
和 的压强不变,总反应
的压强不变,总反应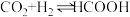 的反应速率为v,反应机理如下列三个基元反应,各反应的活化能
的反应速率为v,反应机理如下列三个基元反应,各反应的活化能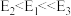 (不考虑催化剂活性降低或丧失)。
(不考虑催化剂活性降低或丧失)。
Ⅳ:

V: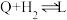

VI: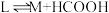

_______ 。
A.v与 的压强无关 B.v与溶液中溶解
的压强无关 B.v与溶液中溶解 的浓度无关
的浓度无关
C.温度升高,v不一定增大 D.在溶液中加入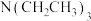 ,可提高
,可提高 转化率
转化率
②实验测得: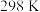 ,
, 下,v随催化剂M浓度c变化如图。
下,v随催化剂M浓度c变化如图。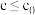 时,v随c增大而增大:
时,v随c增大而增大: 时,v不再显著增大。请解释原因
时,v不再显著增大。请解释原因_______ 。
 转化为
转化为 等化学品,是实现“双碳”目标的途径之一。请回答:
等化学品,是实现“双碳”目标的途径之一。请回答:(1)某研究小组采用电化学方法将
 转化为
转化为 ,装置如图。电极B上的电极反应式是
,装置如图。电极B上的电极反应式是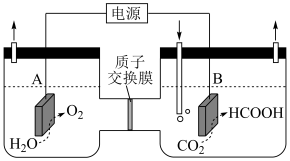
 :
: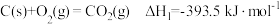
Ⅱ:

Ⅲ:
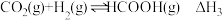
①

 。
。②反应Ⅲ在恒温、恒容的密闭容器中进行,
 和
和 的投料浓度均为
的投料浓度均为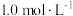 ,平衡常数
,平衡常数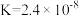 ,则
,则 的平衡转化率为
的平衡转化率为③用氨水吸收
 ,得到
,得到 氨水和
氨水和 甲酸铵的混合溶液,
甲酸铵的混合溶液,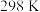 时该混合溶液的
时该混合溶液的
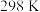 时,电离常数
时,电离常数 、
、 ]
](3)为提高效率,该研究小组参考文献优化热化学方法,在如图密闭装置中充分搅拌催化剂M的
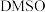 (有机溶剂)溶液,
(有机溶剂)溶液, 和
和 在溶液中反应制备
在溶液中反应制备 ,反应过程中保持
,反应过程中保持 和
和 的压强不变,总反应
的压强不变,总反应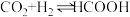 的反应速率为v,反应机理如下列三个基元反应,各反应的活化能
的反应速率为v,反应机理如下列三个基元反应,各反应的活化能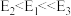 (不考虑催化剂活性降低或丧失)。
(不考虑催化剂活性降低或丧失)。Ⅳ:


V:
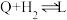

VI:
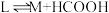

A.v与
 的压强无关 B.v与溶液中溶解
的压强无关 B.v与溶液中溶解 的浓度无关
的浓度无关C.温度升高,v不一定增大 D.在溶液中加入
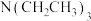 ,可提高
,可提高 转化率
转化率②实验测得:
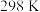 ,
, 下,v随催化剂M浓度c变化如图。
下,v随催化剂M浓度c变化如图。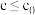 时,v随c增大而增大:
时,v随c增大而增大: 时,v不再显著增大。请解释原因
时,v不再显著增大。请解释原因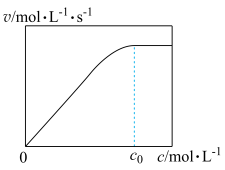
您最近一年使用:0次
2024-02-02更新
|
2625次组卷
|
4卷引用:2024年浙江高考真题化学(1月)
真题
解题方法
6 . 某小组采用如下实验流程制备 :
: 是一种无色晶体,吸湿性极强,可溶于热的正己烷,在空气中受热易被氧化。
是一种无色晶体,吸湿性极强,可溶于热的正己烷,在空气中受热易被氧化。
请回答:
(1)如图为步骤I的实验装置图(夹持仪器和尾气处理装置已省略),图中仪器A的名称是_______ ,判断步骤I反应结束的实验现象是_______ 。不正确 的是_______。
(3)所得粗产品呈浅棕黄色,小组成员认为其中混有碘单质,请设计实验方案验证_______ 。
(4)纯化与分析:对粗产品纯化处理后得到产品,再采用银量法测定产品中 含量以确定纯度。滴定原理为:先用过量
含量以确定纯度。滴定原理为:先用过量 标准溶液沉淀
标准溶液沉淀 ,再以
,再以 标准溶液回滴剩余的
标准溶液回滴剩余的 。已知:
。已知:
①从下列选项中选择合适的操作补全测定步骤_______ 。
称取产品 ,用少量稀酸A溶解后转移至
,用少量稀酸A溶解后转移至 容量瓶,加水定容得待测溶液。取滴定管检漏、水洗→_______→装液、赶气泡、调液面、读数→用移液管准确移取
容量瓶,加水定容得待测溶液。取滴定管检漏、水洗→_______→装液、赶气泡、调液面、读数→用移液管准确移取 待测溶液加入锥形瓶→_______→_______→加入稀酸B→用
待测溶液加入锥形瓶→_______→_______→加入稀酸B→用 标准溶液滴定→_______→读数。
标准溶液滴定→_______→读数。
a.润洗,从滴定管尖嘴放出液体
b.润洗,从滴定管上口倒出液体
c.滴加指示剂 溶液
溶液
d.滴加指示剂硫酸铁铵 溶液
溶液
e.准确移取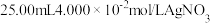 标准溶液加入锥形瓶
标准溶液加入锥形瓶
f.滴定至溶液呈浅红色
g.滴定至沉淀变白色
②加入稀酸B的作用是_______ 。
③三次滴定消耗 标准溶液的平均体积为
标准溶液的平均体积为 ,则产品纯度为
,则产品纯度为_______ 。
 :
:
 是一种无色晶体,吸湿性极强,可溶于热的正己烷,在空气中受热易被氧化。
是一种无色晶体,吸湿性极强,可溶于热的正己烷,在空气中受热易被氧化。请回答:
(1)如图为步骤I的实验装置图(夹持仪器和尾气处理装置已省略),图中仪器A的名称是

| A.步骤I中,反应物和溶剂在使用前除水 |
| B.步骤I中,若控温加热器发生故障,改用酒精灯(配石棉网)加热 |
| C.步骤Ⅲ中,在通风橱中浓缩至蒸发皿内出现晶膜 |
| D.步骤Ⅳ中,使用冷的正己烷洗涤 |
(4)纯化与分析:对粗产品纯化处理后得到产品,再采用银量法测定产品中
 含量以确定纯度。滴定原理为:先用过量
含量以确定纯度。滴定原理为:先用过量 标准溶液沉淀
标准溶液沉淀 ,再以
,再以 标准溶液回滴剩余的
标准溶液回滴剩余的 。已知:
。已知:| 难溶电解质 |  (黄色) (黄色) |  (白色) (白色) |  (红色) (红色) |
溶度积常数 | 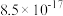 | 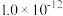 |  |
称取产品
 ,用少量稀酸A溶解后转移至
,用少量稀酸A溶解后转移至 容量瓶,加水定容得待测溶液。取滴定管检漏、水洗→_______→装液、赶气泡、调液面、读数→用移液管准确移取
容量瓶,加水定容得待测溶液。取滴定管检漏、水洗→_______→装液、赶气泡、调液面、读数→用移液管准确移取 待测溶液加入锥形瓶→_______→_______→加入稀酸B→用
待测溶液加入锥形瓶→_______→_______→加入稀酸B→用 标准溶液滴定→_______→读数。
标准溶液滴定→_______→读数。a.润洗,从滴定管尖嘴放出液体
b.润洗,从滴定管上口倒出液体
c.滴加指示剂
 溶液
溶液d.滴加指示剂硫酸铁铵
 溶液
溶液e.准确移取
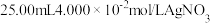 标准溶液加入锥形瓶
标准溶液加入锥形瓶f.滴定至溶液呈浅红色
g.滴定至沉淀变白色
②加入稀酸B的作用是
③三次滴定消耗
 标准溶液的平均体积为
标准溶液的平均体积为 ,则产品纯度为
,则产品纯度为
您最近一年使用:0次
真题
7 . 下列实验装置使用不正确 的是
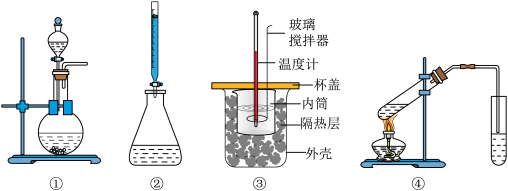
| A.图①装置用于二氧化锰和浓盐酸反应制氯气 |
| B.图②装置用于标准酸溶液滴定未知碱溶液 |
| C.图③装置用于测定中和反应的反应热 |
| D.图④装置用于制备乙酸乙酯 |
您最近一年使用:0次
真题
解题方法
8 .  可用于合成光电材料。某兴趣小组用
可用于合成光电材料。某兴趣小组用 与
与 反应制备液态
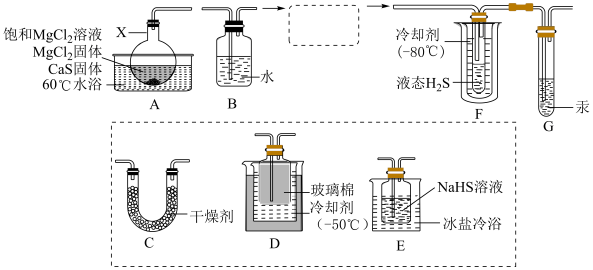
反应制备液态 ,实验装置如图,反应方程式为:
,实验装置如图,反应方程式为: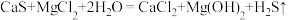 。
。 的沸点是
的沸点是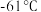 ,有毒:
,有毒:
②装置A内产生的 气体中含有酸性气体杂质。
气体中含有酸性气体杂质。
请回答:
(1)仪器X的名称是_______ 。
(2)完善虚框内的装置排序:A→B→_______ →F+G
(3)下列干燥剂,可用于装置C中的是_______。
(4)装置G中汞的两个作用是:①平衡气压:②_______ 。
(5)下列说法正确的是_______。
(6)取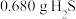 产品,与足量
产品,与足量 溶液充分反应后,将生成的
溶液充分反应后,将生成的 置于已恒重、质量为
置于已恒重、质量为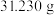 的坩埚中,煅烧生成
的坩埚中,煅烧生成 ,恒重后总质量为
,恒重后总质量为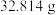 。产品的纯度为
。产品的纯度为_______ 。
 可用于合成光电材料。某兴趣小组用
可用于合成光电材料。某兴趣小组用 与
与 反应制备液态
反应制备液态 ,实验装置如图,反应方程式为:
,实验装置如图,反应方程式为: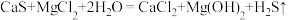 。
。
 的沸点是
的沸点是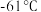 ,有毒:
,有毒:②装置A内产生的
 气体中含有酸性气体杂质。
气体中含有酸性气体杂质。请回答:
(1)仪器X的名称是
(2)完善虚框内的装置排序:A→B→
(3)下列干燥剂,可用于装置C中的是_______。
| A.氢氧化钾 | B.五氧化二磷 | C.氯化钙 | D.碱石灰 |
(4)装置G中汞的两个作用是:①平衡气压:②
(5)下列说法正确的是_______。
| A.该实验操作须在通风橱中进行 |
B.装置D的主要作用是预冷却 |
C.加入的 固体,可使 固体,可使 溶液保持饱和,有利于平稳持续产生 溶液保持饱和,有利于平稳持续产生 |
| D.该实验产生的尾气可用硝酸吸收 |
(6)取
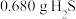 产品,与足量
产品,与足量 溶液充分反应后,将生成的
溶液充分反应后,将生成的 置于已恒重、质量为
置于已恒重、质量为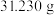 的坩埚中,煅烧生成
的坩埚中,煅烧生成 ,恒重后总质量为
,恒重后总质量为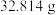 。产品的纯度为
。产品的纯度为
您最近一年使用:0次



