名校
1 . 氧化亚铜和溴化亚铜均是常见的一价铜化合物,氧化亚铜在强酸性溶液中易发生歧化反应,溴化亚铜常用作有机合成原料和反应催化剂。
(1)可利用葡萄糖还原CuSO4溶液制备氧化亚铜。
①配制490mL0.1mol·L-1CuSO4溶液,需要称取胆矾晶体的质量为___________ g。
②某同学为检验CuO样品中是否含有Cu2O,可向样品中加入足量稀硫酸,若观察到___________ ,则说明样品中含有Cu2O杂质。
(2)向CuSO4和NaBr的混合溶液中通入足量的二氧化硫可得到溴化亚铜沉淀。完成该反应的离子方程式:___________ 。
_______Cu2++_______Br-+_______SO2+_______H2O=______CuBr↓+_____ +_________。
+_________。
该反应完毕的现象标志是___________ ,洗涤CuBr沉淀时采用二氧化硫的水溶液而不采用蒸馏水的目的是___________ 。
(3)某小组同学取含有少量CuO杂质的Cu2O样品进行如下实验,以测定氧化亚铜的纯度。
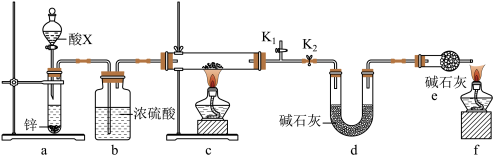
①装置a中所加的酸X是___________ (填化学式)。
②通过测定下列物理量,能达到实验目的的是___________ (填字母)。
A.反应前后装置a的质量 B.充分反应后装置c所得固体的质量
C.反应前后装置d的质量 D.反应前后装置e的质量
③点燃酒精灯前涉及的部分操作如下,正确的顺序是___________ 。
①打开K2:关闭K1②检查装置的气密性③连接仪器④关闭K2,打开K1,通氢气一段时间。
(1)可利用葡萄糖还原CuSO4溶液制备氧化亚铜。
①配制490mL0.1mol·L-1CuSO4溶液,需要称取胆矾晶体的质量为
②某同学为检验CuO样品中是否含有Cu2O,可向样品中加入足量稀硫酸,若观察到
(2)向CuSO4和NaBr的混合溶液中通入足量的二氧化硫可得到溴化亚铜沉淀。完成该反应的离子方程式:
_______Cu2++_______Br-+_______SO2+_______H2O=______CuBr↓+_____
 +_________。
+_________。该反应完毕的现象标志是
(3)某小组同学取含有少量CuO杂质的Cu2O样品进行如下实验,以测定氧化亚铜的纯度。

①装置a中所加的酸X是
②通过测定下列物理量,能达到实验目的的是
A.反应前后装置a的质量 B.充分反应后装置c所得固体的质量
C.反应前后装置d的质量 D.反应前后装置e的质量
③点燃酒精灯前涉及的部分操作如下,正确的顺序是
①打开K2:关闭K1②检查装置的气密性③连接仪器④关闭K2,打开K1,通氢气一段时间。
您最近一年使用:0次
2 . 根据实验目的,装置、现象及对应反应的离子方程式或化学方程式均正确的是
| 选项 | 目的 | 装置 | 现象 | 离子方程式或化学方程式 |
| A | 实验室乙酸乙酯制备 | 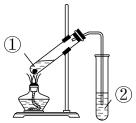 | ②中试管溶液分层,产生有特殊香味的物质 | CH3COOH+CH3CH2OH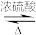 CH3COOCH2CH3+H2O CH3COOCH2CH3+H2O |
| B | 验证SO2的性质 | 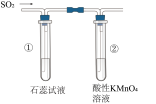 | ①先变红后褪色②中颜色变浅 | 5SO2+2H2O+2MnO =5SO =5SO +2Mn2++4H+ +2Mn2++4H+ |
| C | 实验室快速制取氯气 |  | 产生黄绿色气体 | 10Cl-+16H++2MnO =2Mn2++5Cl2↑+8H2O =2Mn2++5Cl2↑+8H2O |
| D | 检验NH |  | 蓝色石蕊试纸变红 | NH +OH- +OH- NH3↑+H2O NH3↑+H2O |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 含氮物质是中学化学中的一类常见物质,在人们的生产、生活活动中有重要作用,并产生了深远的影响。
(1)实验室中,采用一定浓度的 溶液和
溶液和 溶液作为反应物,通过加热可制备少量
溶液作为反应物,通过加热可制备少量 ,反应的离子方程式是
,反应的离子方程式是_______ ,收集 的方法是
的方法是_______ (填标号)。
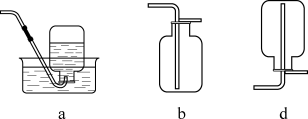
(2)“侯氏制碱法”是中国人的骄傲。某学习小组模拟“侯氏制碱法”原理,在实验室中制备少量 ,使用的装置如图:
,使用的装置如图:
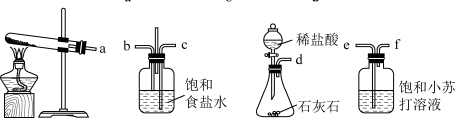
装置接口正确的连接顺序为_______ (填接口序号),由该装置可知,该实验中制备 的试剂是
的试剂是_______ (填化学式)。
(3)该学习小组在实验中,将 溶液滴入
溶液滴入 的
的 溶液中,观察到溶液为棕色,而不是预期的黄色。于是他们进行以下实验探究。
溶液中,观察到溶液为棕色,而不是预期的黄色。于是他们进行以下实验探究。
①实验目的:通过实验探究溶液产生棕色的原因。
②查阅资料:常温下,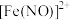 在溶液中能稳定存在,溶液为棕色,受热分解释放出
在溶液中能稳定存在,溶液为棕色,受热分解释放出 。
。
③提出猜想:溶液中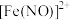 的棕色掩盖了
的棕色掩盖了 的黄色。
的黄色。
④设计实验、验证猜想
⑤现象分析、交流讨论滴加 溶液变红,说明溶液中存在的离子是
溶液变红,说明溶液中存在的离子是_______ (写离子符号),若猜想成立,则“实验2”还应有的现象是_______ 。溶液变棕色的离子方程式是_______ 、 。
。
⑥优化实验:请你设计一个简单的实验,验证“猜想”是否成立。实验设计:_______ ,预期的实验现象及结论:_______ 。
(1)实验室中,采用一定浓度的
 溶液和
溶液和 溶液作为反应物,通过加热可制备少量
溶液作为反应物,通过加热可制备少量 ,反应的离子方程式是
,反应的离子方程式是 的方法是
的方法是
(2)“侯氏制碱法”是中国人的骄傲。某学习小组模拟“侯氏制碱法”原理,在实验室中制备少量
 ,使用的装置如图:
,使用的装置如图:
装置接口正确的连接顺序为
 的试剂是
的试剂是(3)该学习小组在实验中,将
 溶液滴入
溶液滴入 的
的 溶液中,观察到溶液为棕色,而不是预期的黄色。于是他们进行以下实验探究。
溶液中,观察到溶液为棕色,而不是预期的黄色。于是他们进行以下实验探究。①实验目的:通过实验探究溶液产生棕色的原因。
②查阅资料:常温下,
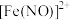 在溶液中能稳定存在,溶液为棕色,受热分解释放出
在溶液中能稳定存在,溶液为棕色,受热分解释放出 。
。③提出猜想:溶液中
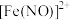 的棕色掩盖了
的棕色掩盖了 的黄色。
的黄色。④设计实验、验证猜想
| 实验序号 | 操作方法 | 现象 |
| 1 | 取上述滴有 溶液的棕色混合液,向其中滴加稀 溶液的棕色混合液,向其中滴加稀 溶液 溶液 | 溶液迅速变为红色 |
| 2 | 取上述棕色混合液,按如图所示加热 | 试管口处有红棕色气体逸出 |
 溶液变红,说明溶液中存在的离子是
溶液变红,说明溶液中存在的离子是 。
。⑥优化实验:请你设计一个简单的实验,验证“猜想”是否成立。实验设计:
您最近一年使用:0次
2022-03-13更新
|
289次组卷
|
2卷引用:广东省碧桂园学校2021-2022学年高三下学期 3月综合能力测试化学试题
名校
解题方法
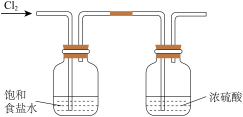
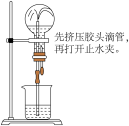
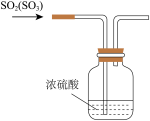
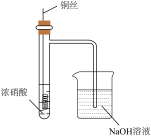
4 . 下列装置和操作不能达到实验目的的是。
|
|
|
|
A.净化浓盐酸与 反应制得的 反应制得的 | B.验证氨气极易溶于水 | C.除去 中的 中的 杂质 杂质 | D.观察浓硝酸与铜反应的现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-03更新
|
748次组卷
|
5卷引用:江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(选择题6-10)
(已下线)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(选择题6-10)(已下线)山东省济南市2022届高三3月高考模拟考试(一模)(选择题1-5)广东省茂名市第一中学2022-2023学年高三上学期期末化学诊断检测题重庆市2023届高三第一次联合诊断检测(一模)(康德卷)化学试题四川省达州市万源中学2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
5 . 某化学研究性学习小组设计实验探究铜的常见化学性质,过程设计如下所示:
【提出猜想】
问题1:在周期表中,铜与铝的位置很靠近,铜不如铝活泼,氢氧化铝具有两性。那么,氢氧化铜也具有两性吗?
问题2:铁和铜都有变价,一般情况下,正二价铁的稳定性小于正三价铁的稳定性。那么,正一价铜的稳定性也小于正二价铜的稳定性吗?
问题3:氧化铜具有氧化性,能被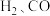 还原。那么,氧化铜也能被氮的某种气态氢化物还原吗?
还原。那么,氧化铜也能被氮的某种气态氢化物还原吗?
【实验探究】
Ⅰ.解决问题1
(1)需用到的药品除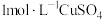 溶液、稀硫酸外,还需
溶液、稀硫酸外,还需____________ (填试剂的化学式)溶液。
(2)为达到本实验目的,你认为应进行的相关实验是(填实验内容):
①__________________ ;②__________________ 。
Ⅱ.解决问题2
取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到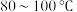 时得到黑色固体粉末;继续加热至
时得到黑色固体粉末;继续加热至 以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁浄试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验现象回答问题:
以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁浄试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验现象回答问题:
(3)写出氧化亚铜与稀硫酸(或盐酸)反应的离子方程式:______________________________ 。
(4)从实验Ⅱ可得出的结论是:__________________________________________ 。
(5)往蓝色溶液中逐滴加入过量的氨水,发生反应的离子方程式为:______________ 、______________ 。
Ⅲ.解决问题3
设计如图装置(夹持装置未画出):

当氮的某种气态氢化物(X)缓缓通过灼热的氧化铜时,观察到氧化铜由黑色变成了红色,无水 变成了蓝色,生成物中还有一种无污染的单质气体Y;将X通入灼热的
变成了蓝色,生成物中还有一种无污染的单质气体Y;将X通入灼热的 燃烧管完全反应后,消耗
燃烧管完全反应后,消耗 ,测得B装置增重
,测得B装置增重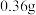 ,并收集到
,并收集到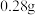 单质气体Y。
单质气体Y。
(6)C装置中发生反应的化学方程式为________________________________ 。
【提出猜想】
问题1:在周期表中,铜与铝的位置很靠近,铜不如铝活泼,氢氧化铝具有两性。那么,氢氧化铜也具有两性吗?
问题2:铁和铜都有变价,一般情况下,正二价铁的稳定性小于正三价铁的稳定性。那么,正一价铜的稳定性也小于正二价铜的稳定性吗?
问题3:氧化铜具有氧化性,能被
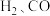 还原。那么,氧化铜也能被氮的某种气态氢化物还原吗?
还原。那么,氧化铜也能被氮的某种气态氢化物还原吗?【实验探究】
Ⅰ.解决问题1
(1)需用到的药品除
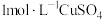 溶液、稀硫酸外,还需
溶液、稀硫酸外,还需(2)为达到本实验目的,你认为应进行的相关实验是(填实验内容):
①
Ⅱ.解决问题2
取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到
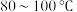 时得到黑色固体粉末;继续加热至
时得到黑色固体粉末;继续加热至 以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁浄试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验现象回答问题:
以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁浄试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验现象回答问题:(3)写出氧化亚铜与稀硫酸(或盐酸)反应的离子方程式:
(4)从实验Ⅱ可得出的结论是:
(5)往蓝色溶液中逐滴加入过量的氨水,发生反应的离子方程式为:
Ⅲ.解决问题3
设计如图装置(夹持装置未画出):

当氮的某种气态氢化物(X)缓缓通过灼热的氧化铜时,观察到氧化铜由黑色变成了红色,无水
 变成了蓝色,生成物中还有一种无污染的单质气体Y;将X通入灼热的
变成了蓝色,生成物中还有一种无污染的单质气体Y;将X通入灼热的 燃烧管完全反应后,消耗
燃烧管完全反应后,消耗 ,测得B装置增重
,测得B装置增重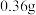 ,并收集到
,并收集到 单质气体Y。
单质气体Y。(6)C装置中发生反应的化学方程式为
您最近一年使用:0次
名校
解题方法
6 . 较活泼金属与硝酸反应,产物复杂。如一定浓度的硝酸与镁反应,可同时得到 、
、 、
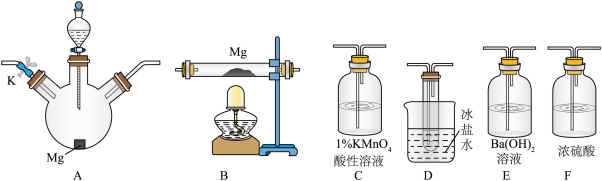
、 三种气体。某同学欲用下列仪器组装装置来直接验证有
三种气体。某同学欲用下列仪器组装装置来直接验证有 、
、 生成并制取氮化镁。(假设实验中每步转化均是完全的)
生成并制取氮化镁。(假设实验中每步转化均是完全的)
已知:① 沸点是21.1℃、熔点是
沸点是21.1℃、熔点是 ℃;
℃; 的沸点是
的沸点是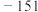 ℃、熔点是
℃、熔点是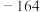 ℃;
℃;
②氮化镁遇水会发生水解。
回答下列问题:
(1)为达到上述实验目的,所选用的仪器的正确连接方式是_________ (填序号)
a.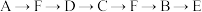 b.
b.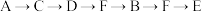
c.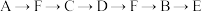 d.
d.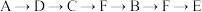
(2)实验中两次使用装置 ,第二次使用装置
,第二次使用装置 的作用是
的作用是_________ 。
(3)实验前需先打开开关 ,向装置内通
,向装置内通 气体,其目的是
气体,其目的是_________ ,当_________ 时停止通入 。
。
(4)实验过程中,发现在 中产生预期现象的同时,
中产生预期现象的同时, 中溶液颜色慢慢褪去,试写出
中溶液颜色慢慢褪去,试写出 中反应的离子方程式
中反应的离子方程式_________ 。
 、
、 、
、 三种气体。某同学欲用下列仪器组装装置来直接验证有
三种气体。某同学欲用下列仪器组装装置来直接验证有 、
、 生成并制取氮化镁。(假设实验中每步转化均是完全的)
生成并制取氮化镁。(假设实验中每步转化均是完全的)
已知:①
 沸点是21.1℃、熔点是
沸点是21.1℃、熔点是 ℃;
℃; 的沸点是
的沸点是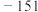 ℃、熔点是
℃、熔点是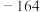 ℃;
℃;②氮化镁遇水会发生水解。
回答下列问题:
(1)为达到上述实验目的,所选用的仪器的正确连接方式是
a.
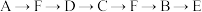 b.
b.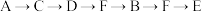
c.
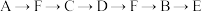 d.
d.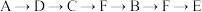
(2)实验中两次使用装置
 ,第二次使用装置
,第二次使用装置 的作用是
的作用是(3)实验前需先打开开关
 ,向装置内通
,向装置内通 气体,其目的是
气体,其目的是 。
。(4)实验过程中,发现在
 中产生预期现象的同时,
中产生预期现象的同时, 中溶液颜色慢慢褪去,试写出
中溶液颜色慢慢褪去,试写出 中反应的离子方程式
中反应的离子方程式
您最近一年使用:0次
名校
7 . 已知:①氧化亚铜在酸性条件下能发生歧化反应: ;②红热的铜能与氮的氧化物反应。某化学小组设计实验探究一氧化氮和铜反应的氧化产物,装置如图(部分夹持装置未画出)。
;②红热的铜能与氮的氧化物反应。某化学小组设计实验探究一氧化氮和铜反应的氧化产物,装置如图(部分夹持装置未画出)。
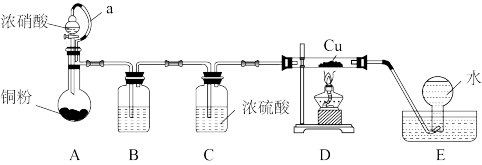
(1)①a管的作用是_______ ,②装置A中发生反应的离子方程式为_______ 。
(2)实验开始时,先打开A中分液漏斗活塞,过一会儿,点燃D处酒精灯,①这样操作的目的是_______ ,当Cu充分反应,实验结束时,②下列操作中应首先进行的是_______ (填序号)。
①停止滴加浓硝酸②熄灭酒精灯③从E装置中取出导气管
(3)为了探究氧化产物是否含有 ,取少量完全反应后的产物,进行如下实验:
,取少量完全反应后的产物,进行如下实验:
(甲)加入足量的稀硝酸,观察是否完全溶解
(乙)加入足量的稀硫酸,观察是否完全溶解
(丙)加入足量的浓硝酸,观察是否完全溶解
(丁)在加热条件下通入乙醇蒸气,观察固体是否变为红色。其中,能达到实验目的的是_______ (填代号)。
(4)查文献发现:铜与浓酸反应一旦发生就变快,是因为开始生成的 溶于水形成
溶于水形成 (弱酸,不稳定,易分解),它再和Cu反应,反应就加快。对生成
(弱酸,不稳定,易分解),它再和Cu反应,反应就加快。对生成 后反应变快的原因进行探究。
后反应变快的原因进行探究。
a.Ⅰ中加入的固体为_______ 。b.Ⅱ中“放置一段时间”的目的是_______ 。
实验Ⅰ、Ⅱ说明 氧化Cu的反应速率比
氧化Cu的反应速率比 氧化Cu快。
氧化Cu快。
(5)某同学将铜片放入盛有稀 的试管中,开始无明显现象,渐有小气泡产生,液面上方出现浅红棕色,溶液呈蓝色。结合上述实验,分析判断该反应慢的原因,除了硝酸浓度小、反应温度较低影响反应速率外,另一个重要原因是
的试管中,开始无明显现象,渐有小气泡产生,液面上方出现浅红棕色,溶液呈蓝色。结合上述实验,分析判断该反应慢的原因,除了硝酸浓度小、反应温度较低影响反应速率外,另一个重要原因是_______ 。
(6)若产物为CuO和 的混合物,取混合物5.92g与足量稀硝酸反应,测得生成448mL标准状况下NO气体,则CuO和
的混合物,取混合物5.92g与足量稀硝酸反应,测得生成448mL标准状况下NO气体,则CuO和 的物质的量之比为
的物质的量之比为_______ 。
 ;②红热的铜能与氮的氧化物反应。某化学小组设计实验探究一氧化氮和铜反应的氧化产物,装置如图(部分夹持装置未画出)。
;②红热的铜能与氮的氧化物反应。某化学小组设计实验探究一氧化氮和铜反应的氧化产物,装置如图(部分夹持装置未画出)。
(1)①a管的作用是
(2)实验开始时,先打开A中分液漏斗活塞,过一会儿,点燃D处酒精灯,①这样操作的目的是
①停止滴加浓硝酸②熄灭酒精灯③从E装置中取出导气管
(3)为了探究氧化产物是否含有
 ,取少量完全反应后的产物,进行如下实验:
,取少量完全反应后的产物,进行如下实验:(甲)加入足量的稀硝酸,观察是否完全溶解
(乙)加入足量的稀硫酸,观察是否完全溶解
(丙)加入足量的浓硝酸,观察是否完全溶解
(丁)在加热条件下通入乙醇蒸气,观察固体是否变为红色。其中,能达到实验目的的是
(4)查文献发现:铜与浓酸反应一旦发生就变快,是因为开始生成的
 溶于水形成
溶于水形成 (弱酸,不稳定,易分解),它再和Cu反应,反应就加快。对生成
(弱酸,不稳定,易分解),它再和Cu反应,反应就加快。对生成 后反应变快的原因进行探究。
后反应变快的原因进行探究。| 序号 | 实验操作 | 实验现象 |
| Ⅰ | 取B中溶液,加入一定量_______固体,再加入铜片 | 立即产生无色气体;液面上方呈红棕色 |
| Ⅱ | 取B中溶液,放置一段时间,溶液变为无色,再加入钢片 | 产生无色气体,较Ⅰ慢;液面上方呈浅红棕色 |
实验Ⅰ、Ⅱ说明
 氧化Cu的反应速率比
氧化Cu的反应速率比 氧化Cu快。
氧化Cu快。(5)某同学将铜片放入盛有稀
 的试管中,开始无明显现象,渐有小气泡产生,液面上方出现浅红棕色,溶液呈蓝色。结合上述实验,分析判断该反应慢的原因,除了硝酸浓度小、反应温度较低影响反应速率外,另一个重要原因是
的试管中,开始无明显现象,渐有小气泡产生,液面上方出现浅红棕色,溶液呈蓝色。结合上述实验,分析判断该反应慢的原因,除了硝酸浓度小、反应温度较低影响反应速率外,另一个重要原因是(6)若产物为CuO和
 的混合物,取混合物5.92g与足量稀硝酸反应,测得生成448mL标准状况下NO气体,则CuO和
的混合物,取混合物5.92g与足量稀硝酸反应,测得生成448mL标准状况下NO气体,则CuO和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
8 . 下列实验操作和现象能达到相应实验目的的是
| 选项 | 实验操作 | 现象 | 实验目的 |
| A | 向浓硝酸中加入红热的炭 | 产生红棕色气体 | 制备 气体 气体 |
| B | 用铜电极电解稀硫酸 | 阴极上产生无色气体 | 比较 和 和 的氧化性强弱 的氧化性强弱 |
| C | 向某溶液中滴加双氧水 | 溶液变为黄色 | 检验溶液中含有 |
| D | 向含 和 和 的混合溶液中加入MgO 的混合溶液中加入MgO | 产生红褐色沉淀 | 用MgO除去镁盐溶液中的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 室温下,下列实验探究方案不能达到实验目的的是
| 选项 | 探究方案 | 实验目的 |
| A | 向2mL1mol·L-1CH3COOH溶液中滴加1mol·L-1Na2CO3溶液,观察现象 | 比较Ka(CH3COOH)和Ka1(H2CO3)的大小 |
| B | 向4mL0.1mol·L-1CuSO4溶液中滴加1mol·L-1氨水至沉淀溶解,再加入8mL95%乙醇,过滤 | 制备[Cu(NH3)4]SO4•H2O晶体 |
| C | 把两个体积相同、封装有等量NO2和N2O4混合气体的烧瓶分别同时浸泡在热水和冰水中,观察混合气体的颜色变化 | 探究温度对化学平衡的影响 |
| D | 向溶液X中滴加少量稀硝酸,然后滴入几滴Ba(NO3)2溶液,观察现象 | 检验溶液X是否含有SO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-09-08更新
|
887次组卷
|
5卷引用:江苏省南京市2023届高三9月学情调研化学试题
江苏省南京市2023届高三9月学情调研化学试题(已下线)2022年辽宁高考真题化学试题变式题(选择题11-15)黑龙江省齐齐哈尔市2023届高三一模理综化学试题(已下线)专题12 化学实验方案的设计与评价黑龙江省大庆市大庆中学2023届高三下学期模拟预测理综化学试题
10 . 下列实验操作、现象及结论都正确的是
| 选项 | 实验目的 | 实验操作 | 现象和结论 |
| A | 探究甲烷气体中是否含有氢气 | 将气体样品通入灼热的氧化铜,然后再通过CuSO4粉末 | 氧化铜固体变为红色,CuSO4粉末变蓝色,说明含有氢气 |
| B | 探究Fe与水蒸气高温反应的固体产物中铁元素的化合价 | 取少量反应后固体于试管中,加足量的稀盐酸溶解,分成两份:一份中滴加硫氰化钾溶液,另一份中滴加酸性高锰酸钾溶液 | 若前者溶液变血红色,后者溶液紫色褪去,则固体产物中铁元素有+2、+3两种化合价 |
| C | 探究乙烯能否被酸性高锰酸钾氧化 | 向乙醇中加入适量浓硫酸制备乙烯,将产生的气体通入酸性高锰酸钾溶液中 | 溶液紫红色褪去,说明乙烯能被酸性高锰酸钾氧化 |
| D | 探究Fe3+、Cu2+对H2O2溶液分解的催化效果强弱 | 在a、b两支试管中各加2mL 5% H2O2溶液,分别滴入0.2mol/L FeCl3溶液和0.3mol/L CuCl2溶液各0.5mL | 若a中产生气泡快于b中,则说明Fe3+的催化效果强于Cu2+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次