名校
1 . 实验室常用如下方法制备少量 :
: ,
, 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是
 :
: ,
, 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是A.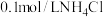 溶液中 溶液中 数目小于 数目小于 |
B.标准状况下,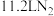 含π键数目为 含π键数目为 |
| C.氯化钠溶液可以导电,所以氯化钠溶液是电解质 |
D.上述反应中每生成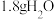 转移电子数目为 转移电子数目为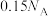 |
您最近一年使用:0次
2 . 纳米球状红磷可提高钠离子电池的性能,制备原理:  。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 含 含 键数目为 键数目为 |
B.每生成 转移电子数目为 转移电子数目为 |
C. 晶体中含离子数目为 晶体中含离子数目为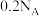 |
D. 晶体中含分子数目为 晶体中含分子数目为 |
您最近一年使用:0次
3 . 磷酸氢二铵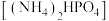 常用作干粉灭火剂,可用磷酸吸收氨气制备。设
常用作干粉灭火剂,可用磷酸吸收氨气制备。设 为阿伏加德罗常数的值,下列叙述错误的是
为阿伏加德罗常数的值,下列叙述错误的是
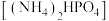 常用作干粉灭火剂,可用磷酸吸收氨气制备。设
常用作干粉灭火剂,可用磷酸吸收氨气制备。设 为阿伏加德罗常数的值,下列叙述错误的是
为阿伏加德罗常数的值,下列叙述错误的是A. 晶体中含有的离子总数为 晶体中含有的离子总数为 |
B.标准状况下,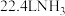 中含有的电子数为 中含有的电子数为 |
C.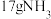 中含有的共价键数目为 中含有的共价键数目为 |
D.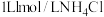 溶液中含有的阳离子数目小于 溶液中含有的阳离子数目小于 |
您最近一年使用:0次
4 . 火箭采用偏二甲肼和四氧化二氮作为推进剂,发生如下反应: 。设
。设 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 。设
。设 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.1mol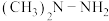 所含共价键的数目为 所含共价键的数目为 |
B.标准状况下,22.4L 所含分子数为 所含分子数为 |
C.44g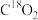 所含质子数为 所含质子数为 |
D.反应生成1mol ,转移的电子数为 ,转移的电子数为 |
您最近一年使用:0次
5 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.7.1g  与足量铁粉反应转移的电子数为0.2 与足量铁粉反应转移的电子数为0.2 |
B.1molL-1  溶液中含离子总数为3 溶液中含离子总数为3 |
C.标准状况下,2.24L  分子中含有的σ键的数目为0.4 分子中含有的σ键的数目为0.4 |
D.44g  中 中 杂化的碳原子数目为2 杂化的碳原子数目为2 |
您最近一年使用:0次
2024·广东佛山·二模
6 . 设 为阿伏加德罗常数的值。制备莫尔盐[
为阿伏加德罗常数的值。制备莫尔盐[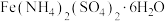 ]用到Fe、
]用到Fe、 、
、 、
、 等物质,下列说法正确的是
等物质,下列说法正确的是
 为阿伏加德罗常数的值。制备莫尔盐[
为阿伏加德罗常数的值。制备莫尔盐[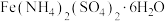 ]用到Fe、
]用到Fe、 、
、 、
、 等物质,下列说法正确的是
等物质,下列说法正确的是A.1L pH=1的 溶液中阳离子总数为0.1 溶液中阳离子总数为0.1 |
B.标准状况下,2.24L  所含共价键数为0.2 所含共价键数为0.2 |
C.0.1  溶液中, 溶液中, 的数目为0.2 的数目为0.2 |
D.5.6g Fe与足量的浓硫酸反应制备 ,转移的电子数为0.2 ,转移的电子数为0.2 |
您最近一年使用:0次
名校
7 . 设 为阿伏加德罗常数的数值,下列说法正确的是
为阿伏加德罗常数的数值,下列说法正确的是
 为阿伏加德罗常数的数值,下列说法正确的是
为阿伏加德罗常数的数值,下列说法正确的是A.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2 |
B.含2mol  的浓硫酸和足量的Cu反应可生成 的浓硫酸和足量的Cu反应可生成 个 个 分子 分子 |
C.标准状况下,22.4L  和 和 混合气中含 混合气中含 个原子 个原子 |
D.18g  和18g 和18g  中含有的质子数均为10 中含有的质子数均为10 |
您最近一年使用:0次
解题方法
8 . 按要求填空
(1)实验室要配制240mL 0.1mol/L 溶液,请回答:配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、天平、量筒、
溶液,请回答:配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、天平、量筒、_______ 、_______
(2)用托盘天平称取碳酸钠固体,其质量为_______
(3)下列主要操作步骤的正确顺序是_______ (填序号)。
①称取一定质量的 ,放入烧杯中,用适量蒸馏水溶解;
,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③将溶液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)如果实验过程中缺少步骤⑤,会造成所配溶液的物质的量浓度_______ (填“偏高”或“偏低”或“无影响”下同)。
定容前,容量瓶中有少量蒸馏水,结果所配溶液的物质的量浓度_______ 。定容时必须使溶液的凹液面与刻度相平,若仰视会使结果浓度_______ 。
(1)实验室要配制240mL 0.1mol/L
 溶液,请回答:配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、天平、量筒、
溶液,请回答:配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、天平、量筒、(2)用托盘天平称取碳酸钠固体,其质量为
(3)下列主要操作步骤的正确顺序是
①称取一定质量的
 ,放入烧杯中,用适量蒸馏水溶解;
,放入烧杯中,用适量蒸馏水溶解;②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③将溶液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)如果实验过程中缺少步骤⑤,会造成所配溶液的物质的量浓度
定容前,容量瓶中有少量蒸馏水,结果所配溶液的物质的量浓度
您最近一年使用:0次
9 . 设阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是A.1mol  和Fe充分反应,转移电子数为3 和Fe充分反应,转移电子数为3 | B.标准状况下,2.24L水含有H的个数为0.2 |
C.1.7g  含有电子数为1 含有电子数为1 | D.0.5mol/L  溶液中 溶液中 的数目为1 的数目为1 |
您最近一年使用:0次
名校
解题方法
10 . I.将39g锌与50mL18.4mol/L的浓硫酸充分反应,锌完全溶解,同时收集到标准状况下气体VL,将反应后的溶液稀释到500mL,测得溶液中氢离子的浓度为0.08mol/L。
(1)反应过程中消耗 的物质的量是
的物质的量是_______ 。
(2)气体的成分是_______ ,V=_______ 。
Ⅱ.将1.52g铜镁合金完全溶解于50mL8mol/L的浓硝酸中,得到NO和 的混合气体896mL(标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。
的混合气体896mL(标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。
(3)此时加入的1.0mol/LNaOH溶液的体积为_______ mL。
(4)混合气体中,NO和 的物质的量之比为
的物质的量之比为_______ 。
(5)若将上述生成的混合气体全部与 一起通入水中,使其完全转化为
一起通入水中,使其完全转化为 ,需通入标准状况下的氧气至少
,需通入标准状况下的氧气至少_______ mL。
(1)反应过程中消耗
 的物质的量是
的物质的量是(2)气体的成分是
Ⅱ.将1.52g铜镁合金完全溶解于50mL8mol/L的浓硝酸中,得到NO和
 的混合气体896mL(标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。
的混合气体896mL(标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。(3)此时加入的1.0mol/LNaOH溶液的体积为
(4)混合气体中,NO和
 的物质的量之比为
的物质的量之比为(5)若将上述生成的混合气体全部与
 一起通入水中,使其完全转化为
一起通入水中,使其完全转化为 ,需通入标准状况下的氧气至少
,需通入标准状况下的氧气至少
您最近一年使用:0次



