名校
1 . 研究含氮元素物质的反应对生产、生活、科研等方面具有重要的意义。请回答下列问题: 不稳定,在水溶液中就会发生歧化反应,其中一种产物为
不稳定,在水溶液中就会发生歧化反应,其中一种产物为 。
。
请回答:
(1)写出肼的电子式______ 。
(2)写出反应I的化学方程式______ 。
(3)下列说法正确的是______。
(4)已知: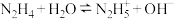 ,
, 与
与 溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
①生成的气体M和白色沉淀N的成分分别是______ 、______ (填化学式)。
②请设计实验验证白色沉淀N的组成元素______ 。

已知:①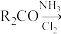
 (异肼)
(异肼)
 不稳定,在水溶液中就会发生歧化反应,其中一种产物为
不稳定,在水溶液中就会发生歧化反应,其中一种产物为 。
。请回答:
(1)写出肼的电子式
(2)写出反应I的化学方程式
(3)下列说法正确的是______。
A.碱性: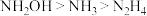 |
| B.肼可以用做还原剂,也可用做配合物的配体 |
| C.肼在水中的溶解度小于在苯中的溶解度 |
| D.反应Ⅱ中的产物之一可以循环利用 |
(4)已知:
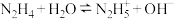 ,
, 与
与 溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。①生成的气体M和白色沉淀N的成分分别是
②请设计实验验证白色沉淀N的组成元素
您最近一年使用:0次
2 . 请回答:
(1)氯仿的分子式________ 。
(2)羟基的电子式________ 。
(3)将光亮的铜丝在酒精灯上灼烧后插入乙醇中,过程中观察到铜丝变化的现象是________ 。
(4)以乙烯为原料制备氯乙烷的化学方程式________ 。(要求有机物写结构简式)
(1)氯仿的分子式
(2)羟基的电子式
(3)将光亮的铜丝在酒精灯上灼烧后插入乙醇中,过程中观察到铜丝变化的现象是
(4)以乙烯为原料制备氯乙烷的化学方程式
您最近一年使用:0次
名校
解题方法
3 . 现有部分元素的性质与原子(或分子)结构如下表(T、X、Y、Z都为前20号元素),请回答:
(1)画出元素T的二价阴离子的结构示意图______
(2)上述元素中,非金属性最强的元素在元素周期表中的位置______ ;表中T、X、Y元素的简单氢化物的稳定性由强到弱的顺序为______ (用化学式表示)。
(3)写出X单质与Z的最高价氧化物对应的水化物反应的化学方程式______
(4)镓(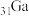 )的化合物砷化镓(GaAs)具有耐高温、耐高电压等特性,可作为第三代半导体材料。废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出
)的化合物砷化镓(GaAs)具有耐高温、耐高电压等特性,可作为第三代半导体材料。废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出 气体,同时生成
气体,同时生成 和
和 。写出该反应的化学方程式
。写出该反应的化学方程式______ 。
元素编号 | 元素性质与原子(或分子)结构 |
T | 其二价阴离子核外电子数为18 |
X | 第三周期非金属性最强的元素 |
Y | L层比K层多5个电子 |
Z | 位于第4周期,内层电子数是最外层电子数的9倍 |
(2)上述元素中,非金属性最强的元素在元素周期表中的位置
(3)写出X单质与Z的最高价氧化物对应的水化物反应的化学方程式
(4)镓(
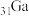 )的化合物砷化镓(GaAs)具有耐高温、耐高电压等特性,可作为第三代半导体材料。废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出
)的化合物砷化镓(GaAs)具有耐高温、耐高电压等特性,可作为第三代半导体材料。废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出 气体,同时生成
气体,同时生成 和
和 。写出该反应的化学方程式
。写出该反应的化学方程式
您最近一年使用:0次
名校
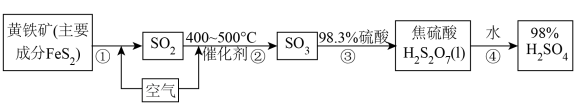
4 . 工业上用黄铁矿为原料制备硫酸的流程如图所示:
(1)已知FeS2的阴离子达到稳定结构,则FeS2的电子式为___________ 。
(2)已知: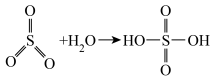 ,请写出焦硫酸的结构式
,请写出焦硫酸的结构式___________ 。
(3)写出步骤①的化学方程式___________ 。
(4)室温下,SO3为液体,SO2为气体。SO3熔点高于SO2的原因___________ 。
(5)下列说法正确的是___________ 。
A.步骤①,产生的气体进入接触室之前无需净化处理
B.步骤②,使用催化剂能使SO2的转化率达到100%
C.步骤③,吸收设备中填充瓷环可提高SO3吸收率
D.可以预测:Na2S2O7的水溶液呈酸性,H2S2能将Fe2+氧化成Fe3+
E.17.8g H2S2O7与2.2g水充分混合后,可获得98%浓硫酸
(6)若硫铁矿煅烧不充分,则炉渣中混有+2价的铁元素,试设计一个简单的实验证明之。简述实验操作和有关的实验现象___________ 。(供选择的试剂:KSCN溶液、稀硫酸、稀盐酸、KMnO4溶液、品红溶液、NaOH溶液)
(1)已知FeS2的阴离子达到稳定结构,则FeS2的电子式为
(2)已知:
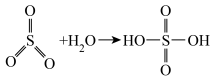 ,请写出焦硫酸的结构式
,请写出焦硫酸的结构式(3)写出步骤①的化学方程式
(4)室温下,SO3为液体,SO2为气体。SO3熔点高于SO2的原因
(5)下列说法正确的是
A.步骤①,产生的气体进入接触室之前无需净化处理
B.步骤②,使用催化剂能使SO2的转化率达到100%
C.步骤③,吸收设备中填充瓷环可提高SO3吸收率
D.可以预测:Na2S2O7的水溶液呈酸性,H2S2能将Fe2+氧化成Fe3+
E.17.8g H2S2O7与2.2g水充分混合后,可获得98%浓硫酸
(6)若硫铁矿煅烧不充分,则炉渣中混有+2价的铁元素,试设计一个简单的实验证明之。简述实验操作和有关的实验现象
您最近一年使用:0次
5 . A、B、C、D、E、F是原子序数依次增大的前四周期元素,A元素电子只有一种自旋取向;B元素原子的价电子排布是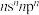 ,C是地壳中含量最多的非金属元素;
,C是地壳中含量最多的非金属元素; 第三周期中半径最小的简单离子;E元素负一价离子的能层结构与氩相同;F元素基态原子核外有7个能级上有电子且有4个未成对电子。
第三周期中半径最小的简单离子;E元素负一价离子的能层结构与氩相同;F元素基态原子核外有7个能级上有电子且有4个未成对电子。
请回答:
(1)A是_______ 区的元素,BC元素形成的双原子分子结构与 相似,写出该双原子分子的电子式
相似,写出该双原子分子的电子式_______ 。
(2)C、D、E的简单离子的半径从大到小的顺序_______ (用离子符号表示)。
(3)F元素有两种常见的价态,比较这两种价态阳离子的稳定性
_______ 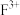 (填“>”、“<”或“=”),理由是
(填“>”、“<”或“=”),理由是_______ 。
(4)与D元素成“对角线规则”关系的某短周期元素的最高价氧化物对应的水化物具有两性,写出该两性物质与E元素的最高价氧化物对应的水化物反应的化学方程式_______ 。
(5)物质X由ABC三种元素构成。按下图实验装置(部分装置略)对X进行元素分析:

①依次点燃煤气灯_______ →_______ ,进行实验。实验过程中CuO的作用是_______ (举1例,用化学方程式表示)。
②若样品X质量为2.36g,实验结束后,c管增重1.08g,d管增重3.52g。质谱测得该有机物的相对分子量为118,其分子式为_______ 。
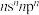 ,C是地壳中含量最多的非金属元素;
,C是地壳中含量最多的非金属元素; 第三周期中半径最小的简单离子;E元素负一价离子的能层结构与氩相同;F元素基态原子核外有7个能级上有电子且有4个未成对电子。
第三周期中半径最小的简单离子;E元素负一价离子的能层结构与氩相同;F元素基态原子核外有7个能级上有电子且有4个未成对电子。请回答:
(1)A是
 相似,写出该双原子分子的电子式
相似,写出该双原子分子的电子式(2)C、D、E的简单离子的半径从大到小的顺序
(3)F元素有两种常见的价态,比较这两种价态阳离子的稳定性

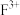 (填“>”、“<”或“=”),理由是
(填“>”、“<”或“=”),理由是(4)与D元素成“对角线规则”关系的某短周期元素的最高价氧化物对应的水化物具有两性,写出该两性物质与E元素的最高价氧化物对应的水化物反应的化学方程式
(5)物质X由ABC三种元素构成。按下图实验装置(部分装置略)对X进行元素分析:

①依次点燃煤气灯
②若样品X质量为2.36g,实验结束后,c管增重1.08g,d管增重3.52g。质谱测得该有机物的相对分子量为118,其分子式为
您最近一年使用:0次
解题方法
6 . 回答下列问题。
(1)请写出NH4Br的电子式___________ ;请写出H2O2的结构式:___________ 。
(2)请写出亚硫酸在水中电离的方程式:___________ 。
(3)请写出一种能比较碳元素和硅元素非金属性强弱的方程式:___________ 。
(4)水晶中主要成分的化学式为:___________ 。
(1)请写出NH4Br的电子式
(2)请写出亚硫酸在水中电离的方程式:
(3)请写出一种能比较碳元素和硅元素非金属性强弱的方程式:
(4)水晶中主要成分的化学式为:
您最近一年使用:0次
名校
7 . 请回答:
(1)Na的原子结构示意图是________________ ;MgCl2电子式是___________________ 。
(2)足量SO2通入酸性高锰酸钾溶液后溶液褪色,说明了SO2具有________________ 性。
(3)实验室制备氯气时用氢氧化钠溶液吸收尾气,该反应的离子方程式是________________ 。
(4)在氯化铁溶液中滴加2滴KSCN溶液,现象是________________ ;此反应的离子方程式是________________ 。然后在溶液中再加入足量的铁粉,现象是________________ ,此时反应的离子方程式是________________ 。
(1)Na的原子结构示意图是
(2)足量SO2通入酸性高锰酸钾溶液后溶液褪色,说明了SO2具有
(3)实验室制备氯气时用氢氧化钠溶液吸收尾气,该反应的离子方程式是
(4)在氯化铁溶液中滴加2滴KSCN溶液,现象是
您最近一年使用:0次
解题方法
8 . 请回答下列问题:
(1)氯原子的最外层电子数为___________ ;其最高价氧化物的化学式是___________ 。
(2)维生素 又称“抗坏血酸”,能将
又称“抗坏血酸”,能将 转化为
转化为 ,说明维生素
,说明维生素 具有
具有___________ 性(填“还原”或“氧化”)。
(3)写出白色的氢氧化亚铁沉淀在空气中变色的化学反应方程式___________ 。
(1)氯原子的最外层电子数为
(2)维生素
 又称“抗坏血酸”,能将
又称“抗坏血酸”,能将 转化为
转化为 ,说明维生素
,说明维生素 具有
具有(3)写出白色的氢氧化亚铁沉淀在空气中变色的化学反应方程式
您最近一年使用:0次
名校
解题方法
9 . 含氮化合物种类多,用途广。回答下列问题。
(1)NH3的电子式为__________ ,NH3与NaClO在一定条件下可生成N2H4,化学方程式为__________ 。
(2) 又称联氨,为二元弱碱,不如氨气稳定,还原性强于氨气。
又称联氨,为二元弱碱,不如氨气稳定,还原性强于氨气。
①联氨在水中的电离方程式与氨相似,则联氨第一步的电离方程式为__________ 。
②肼-空气燃料电池是一种碱性燃料电池,生成无污染的物质。电解质溶液是 的KOH溶液。肼空气燃料电池放电时,负极的电极反应式是
的KOH溶液。肼空气燃料电池放电时,负极的电极反应式是__________ 。
③从分子结构角度分析,N2H4不如氨气稳定的原因是__________ 。
(3)常温下,在NH4Cl溶液中加入NaOH(s)至中性,则 =
=__________ (常温下NH3·H2O的电离平衡常数为 )。
)。
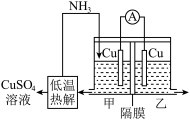
(4)利用热再生氨电池可实现CuSO4电镀废液的浓缩再生。电池装置如图所示,甲、乙两室均预加相同的CuSO4电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是__________。
(5)在加热条件下通入过量的NH3与CuO反应,可得到红色固体。设计实验验证尾气中比较活泼的两种气体__________ 。
(1)NH3的电子式为
(2)
 又称联氨,为二元弱碱,不如氨气稳定,还原性强于氨气。
又称联氨,为二元弱碱,不如氨气稳定,还原性强于氨气。①联氨在水中的电离方程式与氨相似,则联氨第一步的电离方程式为
②肼-空气燃料电池是一种碱性燃料电池,生成无污染的物质。电解质溶液是
 的KOH溶液。肼空气燃料电池放电时,负极的电极反应式是
的KOH溶液。肼空气燃料电池放电时,负极的电极反应式是③从分子结构角度分析,N2H4不如氨气稳定的原因是
(3)常温下,在NH4Cl溶液中加入NaOH(s)至中性,则
 =
= )。
)。(4)利用热再生氨电池可实现CuSO4电镀废液的浓缩再生。电池装置如图所示,甲、乙两室均预加相同的CuSO4电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是__________。

| A.甲室Cu电极为负极 |
| B.Cu2+通过隔膜进入乙室 |
| C.电池总反应为:Cu2++4NH3=[Cu(NH3)4]2+ |
| D.NH3扩散到乙室不会对电池电压产生影响 |
(5)在加热条件下通入过量的NH3与CuO反应,可得到红色固体。设计实验验证尾气中比较活泼的两种气体
您最近一年使用:0次
10 . 化学物质丰富多彩,在生产、生活、科研等方面都起着重要的作用。
(1)磁铁矿主要成分的化学式是_______ ; CO₂的电子式_______ 。
(2)家庭厨卫管道常因留有菜渣、毛发而造成堵塞,可用管道疏通剂疏通。常用的管道疏通剂主要成分有铝粉和氢氧化钠,请用离子方程式表达其疏通原理_______ 。
(3)工业上用焦炭还原石英砂可以制得含有少量杂质的粗硅。请写出化学方程式_______ 。
(1)磁铁矿主要成分的化学式是
(2)家庭厨卫管道常因留有菜渣、毛发而造成堵塞,可用管道疏通剂疏通。常用的管道疏通剂主要成分有铝粉和氢氧化钠,请用离子方程式表达其疏通原理
(3)工业上用焦炭还原石英砂可以制得含有少量杂质的粗硅。请写出化学方程式
您最近一年使用:0次



