名校
1 . 电子式表示下列物质的形成过程
(1) :
:_____ ;
(2) :
:_____ ;
(3) :
:_____ 。
(1)
 :
:(2)
 :
:(3)
 :
:
您最近一年使用:0次
名校
2 . 写出给定物质的电子式

_____ ;
_____ ;
_____ ;
_____ ;




您最近一年使用:0次
名校
解题方法
3 . 请用化学用语(化学方程式或离子方程式或电子式等)解释以下事实:
(1)NaCl固体溶于水可导电_______ 。
(2)工业酸性废水中含有的重铬酸根离子(Cr2O )有毒,可用硫酸亚铁转化成无毒的Cr3+处理达标后安全排放(离子方程式)
)有毒,可用硫酸亚铁转化成无毒的Cr3+处理达标后安全排放(离子方程式)________ 。
(3)钠与水剧烈反应(离子方程式)________ 。
(4)过氧化钠可做潜水艇氧气来源_______ 。
(5)实验室常用舎勒的方法制备氯气________ 。
(6)氯气溶于水能杀菌消毒(离子方程式)________ 。
(7)工业上将Cl2转化成更易保存的漂白粉________ 。
(8)炽热的铁水或钢水注入模具之前,模具必须进行充分的干燥处理_______ 。
(9)工业上用FeCl3溶液刻蚀覆铜板(离子方程式)________ 。
(10)由Na和Cl形成离子键的过程:________ 。
(1)NaCl固体溶于水可导电
(2)工业酸性废水中含有的重铬酸根离子(Cr2O
 )有毒,可用硫酸亚铁转化成无毒的Cr3+处理达标后安全排放(离子方程式)
)有毒,可用硫酸亚铁转化成无毒的Cr3+处理达标后安全排放(离子方程式)(3)钠与水剧烈反应(离子方程式)
(4)过氧化钠可做潜水艇氧气来源
(5)实验室常用舎勒的方法制备氯气
(6)氯气溶于水能杀菌消毒(离子方程式)
(7)工业上将Cl2转化成更易保存的漂白粉
(8)炽热的铁水或钢水注入模具之前,模具必须进行充分的干燥处理
(9)工业上用FeCl3溶液刻蚀覆铜板(离子方程式)
(10)由Na和Cl形成离子键的过程:
您最近一年使用:0次
名校
解题方法
4 . 有A、B、C、D四种有机物,A、B属于烃类物质,C、D都是烃的衍生物。A是含氢质量分数最大的有机物,分子结构为正四面体;B的球棍模型为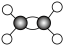 ;C的相对分子质量为46,能与Na反应,但不能与NaOH反应;D的比例模型为
;C的相对分子质量为46,能与Na反应,但不能与NaOH反应;D的比例模型为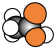 ,该物质的水溶液中滴加石蕊变红色。请回答下列问题:
,该物质的水溶液中滴加石蕊变红色。请回答下列问题:
(1)A的电子式是___________ ,C中官能团的名称是___________ 。
(2)B的结构简式是___________ ,该物质发生加聚反应的化学方程式为___________ 。
(3)C与D在一定条件下反应生成一种有香味的物质,写出其化学方程式___________ 。
(4)下列说法正确的是___________ (填序号),
①B与其加聚反应产物组成元素及其原子个数比相同
②A与B都属于烃类,二者互为同系物
③C和D中都有—OH,其水溶液都显酸性
 ;C的相对分子质量为46,能与Na反应,但不能与NaOH反应;D的比例模型为
;C的相对分子质量为46,能与Na反应,但不能与NaOH反应;D的比例模型为 ,该物质的水溶液中滴加石蕊变红色。请回答下列问题:
,该物质的水溶液中滴加石蕊变红色。请回答下列问题:(1)A的电子式是
(2)B的结构简式是
(3)C与D在一定条件下反应生成一种有香味的物质,写出其化学方程式
(4)下列说法正确的是
①B与其加聚反应产物组成元素及其原子个数比相同
②A与B都属于烃类,二者互为同系物
③C和D中都有—OH,其水溶液都显酸性
您最近一年使用:0次
名校
解题方法
5 . 钠及其化合物在认识物质转化规律以及生产生活中均有重要应用。
(1)金属与水的反应
①Na的原子结构示意图是__________ 。
②钠与水反应的化学方程式是__________ 。
③钠与水的反应放出热量的现象是__________ 。
(2)钠失火时,可用不同的灭火剂灭火。如可用Na2CO3干粉灭火,但不能用NaHCO3灭火,结合反应方程式说明原因__________ 。

(1)金属与水的反应
①Na的原子结构示意图是
②钠与水反应的化学方程式是
③钠与水的反应放出热量的现象是
(2)钠失火时,可用不同的灭火剂灭火。如可用Na2CO3干粉灭火,但不能用NaHCO3灭火,结合反应方程式说明原因
您最近一年使用:0次
名校
6 . 填写下列表格。
| 元素(原子团)名称 | 化学式 | 质子数 | 原子(离子)结构示意图 | 核外电子数 |
| 硫离子 | ||||
| 硫酸根 | ||||
| 铵根 |
您最近一年使用:0次
名校
7 . 填空。
(1)镁离子符号______________________ ,结构示意图______________________ 。
(2)氯离子符号______________________ ,结构示意图______________________ 。
(1)镁离子符号
(2)氯离子符号
您最近一年使用:0次
解题方法
8 . 甲酸 被认为是一种有前途的储氢化合物。在催化剂作用下,甲酸分解制氢的过程如图所示。
被认为是一种有前途的储氢化合物。在催化剂作用下,甲酸分解制氢的过程如图所示。
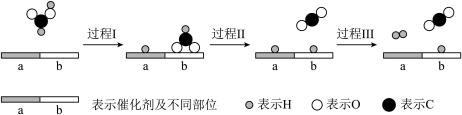
(1) 中官能团的名称是
中官能团的名称是_______ 。
(2)常压下甲酸的沸点是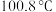 。甲酸沸腾的过程中,外界提供的能量的作用是
。甲酸沸腾的过程中,外界提供的能量的作用是_______ 。
(3)过程Ⅰ中断裂的化学键是_______ ,过程Ⅲ中形成的化学键是_______ 。
(4) 分解制氢的总反应方程式是
分解制氢的总反应方程式是_______ ,两种产物的电子式分别是_______ 、_______ 。
(5) 分解制氢是一个可逆反应。在密闭容器中,通入
分解制氢是一个可逆反应。在密闭容器中,通入 蒸汽,一段时间后,核素
蒸汽,一段时间后,核素 存在于以下分子中:
存在于以下分子中:_______ 。
 被认为是一种有前途的储氢化合物。在催化剂作用下,甲酸分解制氢的过程如图所示。
被认为是一种有前途的储氢化合物。在催化剂作用下,甲酸分解制氢的过程如图所示。
(1)
 中官能团的名称是
中官能团的名称是(2)常压下甲酸的沸点是
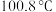 。甲酸沸腾的过程中,外界提供的能量的作用是
。甲酸沸腾的过程中,外界提供的能量的作用是(3)过程Ⅰ中断裂的化学键是
(4)
 分解制氢的总反应方程式是
分解制氢的总反应方程式是(5)
 分解制氢是一个可逆反应。在密闭容器中,通入
分解制氢是一个可逆反应。在密闭容器中,通入 蒸汽,一段时间后,核素
蒸汽,一段时间后,核素 存在于以下分子中:
存在于以下分子中:
您最近一年使用:0次
9 . 依据A~E几种烃分子的示意图填空。
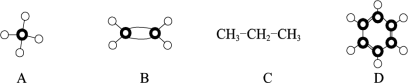
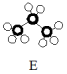
(1)D的分子式是________________ ,B的名称是____________ 。
(2)上述分子中属于C的同系物的是_____________ (填字母)。
(3)上述符号中属于结构简式的是_____________ (填字母)。
(4)A分子与氯气反应的第一步反应化学方程式为:_______ ,该反应属于_______ (填反应类型)
(5)B通入Br2的四氯化碳溶液,现象为___________ ,该反应属于_______ (填反应类型);B还可在一定条件下发生_____________ (填反应类型)反应生成聚合物,化学方程式是______ 。


(1)D的分子式是
(2)上述分子中属于C的同系物的是
(3)上述符号中属于结构简式的是
(4)A分子与氯气反应的第一步反应化学方程式为:
(5)B通入Br2的四氯化碳溶液,现象为
您最近一年使用:0次
22-23高三上·天津南开·期末
解题方法
10 . Na、Mg、Fe、Cu是四种重要的金属元素。回答下列问题:
(1)基态Mg原子的价层电子轨道表示式为__________________ 。
(2) 的电子式为
的电子式为____________ 。
(3)在钢铁厂的生产中,炽热的铁水注入模具之前,模具必须进行充分的干燥处理,不得留有水,请用化学方程式解释原因:__________________ 。
(4)检验 溶液中是否残留
溶液中是否残留 的试剂是
的试剂是__________________ 。
(5)NaCl熔点为800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式为 ,加入
,加入 的目的是
的目的是____________ 。
(6)采用空气和Na为原料可直接制备 。空气与熔融金属Na反应前,需依次通过
。空气与熔融金属Na反应前,需依次通过____________ 、____________ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d. 溶液
溶液
(7)天然碱的主要成分为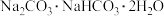 ,2 mol
,2 mol 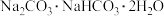 经充分加热得到
经充分加热得到 的质量为
的质量为______ g。
(8)一个 晶胞(如图)中,Cu原子的数目为
晶胞(如图)中,Cu原子的数目为______ 。
(1)基态Mg原子的价层电子轨道表示式为
(2)
 的电子式为
的电子式为(3)在钢铁厂的生产中,炽热的铁水注入模具之前,模具必须进行充分的干燥处理,不得留有水,请用化学方程式解释原因:
(4)检验
 溶液中是否残留
溶液中是否残留 的试剂是
的试剂是(5)NaCl熔点为800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式为
 ,加入
,加入 的目的是
的目的是(6)采用空气和Na为原料可直接制备
 。空气与熔融金属Na反应前,需依次通过
。空气与熔融金属Na反应前,需依次通过a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.
 溶液
溶液(7)天然碱的主要成分为
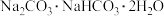 ,2 mol
,2 mol 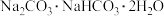 经充分加热得到
经充分加热得到 的质量为
的质量为(8)一个
 晶胞(如图)中,Cu原子的数目为
晶胞(如图)中,Cu原子的数目为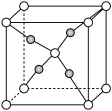
您最近一年使用:0次
2023-02-20更新
|
546次组卷
|
4卷引用:结构与性质
(已下线)结构与性质天津市南开区2022~2023 学年高三上学期阶段性质量监测 (二) 化学试题(已下线)2022年天津市普通高中学业水平等级性考试化学试题变式题(结构与性质)天津市八校2024届高三下学期联合模拟考试化学试题(二)



