解题方法
1 . 回答下列问题。
(1)氮元素在元素周期表中的位置是第___________ 周期,第___________ 族。
(2) 是元素周期表中第
是元素周期表中第___________ 号元素。
(3) 的M能层电子排布式是
的M能层电子排布式是___________ ,价层电子排布图是___________ ,原子结构示意图是___________ 。
(1)氮元素在元素周期表中的位置是第
(2)
 是元素周期表中第
是元素周期表中第(3)
 的M能层电子排布式是
的M能层电子排布式是
您最近一年使用:0次
名校
2 . 根据要求完成下列填空。
(1)画出氯原子结构示意图______ 。
(2)写出氨气和氢氧化钠的电子式:氨气_______ ,氢氧化钠______ 。
(3)写出氯化铁和铁反应的离子方程式_________ 。
(4)除去 固体中混入的
固体中混入的 杂质最佳方法是
杂质最佳方法是____ ,化学方程式为________ 。
(1)画出氯原子结构示意图
(2)写出氨气和氢氧化钠的电子式:氨气
(3)写出氯化铁和铁反应的离子方程式
(4)除去
 固体中混入的
固体中混入的 杂质最佳方法是
杂质最佳方法是
您最近一年使用:0次
名校
3 . 现有下列九组物质:① Cl、
Cl、 Cl;②金刚石、石墨;③O2、O3;④二氧化碳;⑤ H2O、D2O;⑥氯化镁;⑦H、D、T;⑧ Ba(OH)2;⑨ NH4Cl。
Cl;②金刚石、石墨;③O2、O3;④二氧化碳;⑤ H2O、D2O;⑥氯化镁;⑦H、D、T;⑧ Ba(OH)2;⑨ NH4Cl。
(1)互为同位素的是_______ (填序号,下同),互为同素异形体是_______ 。
(2)⑧的电子式为_______ ,④的结构式为_______ 。
(3)用电子式表示⑥的形成过程_______ 。
(4)⑨中含有的化学键类型有_______。
 Cl、
Cl、 Cl;②金刚石、石墨;③O2、O3;④二氧化碳;⑤ H2O、D2O;⑥氯化镁;⑦H、D、T;⑧ Ba(OH)2;⑨ NH4Cl。
Cl;②金刚石、石墨;③O2、O3;④二氧化碳;⑤ H2O、D2O;⑥氯化镁;⑦H、D、T;⑧ Ba(OH)2;⑨ NH4Cl。(1)互为同位素的是
(2)⑧的电子式为
(3)用电子式表示⑥的形成过程
(4)⑨中含有的化学键类型有_______。
| A.离子键 | B.极性共价键 | C.非极性共价键 | D.氢键 |
您最近一年使用:0次
名校
解题方法
4 . 根据要求完成下列填空。
(1)标准状况下,33.6LHCl溶于水配成1L的溶液,则溶液的物质的量浓度为___________ mol/L。
(2)钠是活泼金属,能与水剧烈反应,请写出反应的该反应的离子方程式___________ 。
(3)写出水和氯化镁的电子式:水___________ 、氯化镁___________ 。
(4)用电子式描述氯化钠和氯化氢的形成过程
氯化钠:___________ 。
氯化氢:___________ 。
(1)标准状况下,33.6LHCl溶于水配成1L的溶液,则溶液的物质的量浓度为
(2)钠是活泼金属,能与水剧烈反应,请写出反应的该反应的离子方程式
(3)写出水和氯化镁的电子式:水
(4)用电子式描述氯化钠和氯化氢的形成过程
氯化钠:
氯化氢:
您最近一年使用:0次
名校
5 . 按要求回答下列问题:
(1)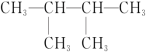 的系统命名为
的系统命名为_______ 。
(2)2,3-二甲基-4-乙基己烷的结构简式______ 。
(3) 的结构简式为
的结构简式为_______ ,分子式为_______ 。
(4)松油醇(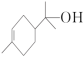 )含氧官能团的名称为
)含氧官能团的名称为_______ ,sp3杂化的碳原子数为_______ 。
(1)
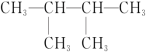 的系统命名为
的系统命名为(2)2,3-二甲基-4-乙基己烷的结构简式
(3)
 的结构简式为
的结构简式为(4)松油醇(
 )含氧官能团的名称为
)含氧官能团的名称为
您最近一年使用:0次
6 . 请回答:
(1)Na2O2的电子式___________ 。
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由___________ 。
(3)KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为
_______KClO3+_______HCl(浓)=_______KCl+_______ClO2↑+_______Cl2↑+_______
① 请配平上述化学方程式。___________
② 浓盐酸在反应中显示出来的性质是___________
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③若反应中生成标准状况下13.44L气体,则消耗还原剂的物质的量为___________ 。
④ClO2具有很强的氧化性,常用作消毒剂,其消毒的效率(以单位物质的量得到的电子数表示)是H2O2的___________ 倍。
(4)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为___________ 。
(1)Na2O2的电子式
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由
(3)KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为
_______KClO3+_______HCl(浓)=_______KCl+_______ClO2↑+_______Cl2↑+_______

① 请配平上述化学方程式。
② 浓盐酸在反应中显示出来的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③若反应中生成标准状况下13.44L气体,则消耗还原剂的物质的量为
④ClO2具有很强的氧化性,常用作消毒剂,其消毒的效率(以单位物质的量得到的电子数表示)是H2O2的
(4)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
您最近一年使用:0次
名校
7 . 科学家发现:具有2、8、20、28、50、82、114、126等数目的质子或中子的原子核具有特别的稳定性,并将这些偶数称为“幻数”,而具有双幻数的 、
、 、
、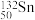 、
、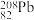 等尤为稳定。根据此信息回答下列问题:
等尤为稳定。根据此信息回答下列问题:
(1)写出前两种质子数为“幻数”的元素原子的结构示意图,并标明元素符号___________ 。
(2)已知氧有三种同位素 、
、 、
、 ,根据上述“幻数”规律,氧的同位素中原子核最稳定的是
,根据上述“幻数”规律,氧的同位素中原子核最稳定的是___________ 。
(3)根据现有元素周期律推算,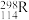 位于元素周期表的第
位于元素周期表的第___________ 周期第___________ 族,核稳定性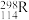
___________ 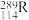 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
 、
、 、
、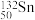 、
、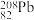 等尤为稳定。根据此信息回答下列问题:
等尤为稳定。根据此信息回答下列问题:(1)写出前两种质子数为“幻数”的元素原子的结构示意图,并标明元素符号
(2)已知氧有三种同位素
 、
、 、
、 ,根据上述“幻数”规律,氧的同位素中原子核最稳定的是
,根据上述“幻数”规律,氧的同位素中原子核最稳定的是(3)根据现有元素周期律推算,
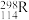 位于元素周期表的第
位于元素周期表的第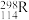
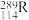 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
您最近一年使用:0次
名校
8 . 已知H与O可以形成H2O和H2O2两种化合物。请完成下列空白:
(1)H2O内的O—H、水分子间的范德华力和氢键,三种作用从强到弱依次为___________ 。 可与H2O形成
可与H2O形成 ,
, 中O采用
中O采用___________ 杂化。 中
中 键角比CH4中的键角
键角比CH4中的键角___________ (填“大”或“小”),原因为_______ 。
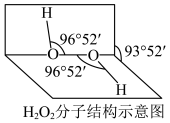
(2) 是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。
是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。 的电子式是
的电子式是___________ 。 是
是___________ 分子(填“极性”或“非极性”)。 能与水混溶,却不溶于
能与水混溶,却不溶于 ,请予以解释:
,请予以解释:___________ 。
(1)H2O内的O—H、水分子间的范德华力和氢键,三种作用从强到弱依次为
 可与H2O形成
可与H2O形成 ,
, 中O采用
中O采用 中
中 键角比CH4中的键角
键角比CH4中的键角(2)
 是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。
是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。 的电子式是
的电子式是 是
是 能与水混溶,却不溶于
能与水混溶,却不溶于 ,请予以解释:
,请予以解释:
您最近一年使用:0次
名校
解题方法
9 . 回答下列问题
(1)用VSEPR 理论判断:
(2)基态Fe原子有___________ 个未成对电子,Fe3+的价电子排布式为___________ 。Fe在周期表中位于___________ 列。
(3)Cl的核外电子排布式为___________ 。
(4)22Ti的原子结构示意图___________ 。
(5)Sn为ⅣA族元素,单质Sn与干燥 反应生成
反应生成 。常温常压下
。常温常压下 为无色液体,
为无色液体, 空间构型为
空间构型为___________ 。
(1)用VSEPR 理论判断:
| 物质 | 孤对电子对数 | 轨道杂化方式 | 分子或离子的空间结构 |
PO | |||
| COCl2 |
(3)Cl的核外电子排布式为
(4)22Ti的原子结构示意图
(5)Sn为ⅣA族元素,单质Sn与干燥
 反应生成
反应生成 。常温常压下
。常温常压下 为无色液体,
为无色液体, 空间构型为
空间构型为
您最近一年使用:0次
10 . 某酸性有机物只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子。

(1)该分子模型是___________ (填:“比例模型”、“球棍模型”)。
(2)该物质中所含官能团的名称为_______________________ 。
(3)该物质的结构简式为_______________________________ 。
(4)写出该分子的一种同分异构体的结构简式_____________ 。

(1)该分子模型是
(2)该物质中所含官能团的名称为
(3)该物质的结构简式为
(4)写出该分子的一种同分异构体的结构简式
您最近一年使用:0次



