名校
1 . 按要求回答下列问题:
(1)写出乙烯分子的结构式:___________ 。
(2)写出有机物2-甲基-1,3-丁二烯的结构简式___________ 。
(3)下列物质的沸点按由高到低的顺序排列正确的是___________。
①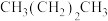 ②
②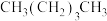 ③
③ ④
④
(4)下列选项中互为同系物的是___________ ;互为同分异构体的是___________ ;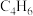 的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为
的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为___________ 。
(1)写出乙烯分子的结构式:
(2)写出有机物2-甲基-1,3-丁二烯的结构简式
(3)下列物质的沸点按由高到低的顺序排列正确的是___________。
①
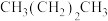 ②
②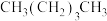 ③
③ ④
④
| A.②④①③ | B.④②①③ | C.④③②① | D.②④③① |
(4)下列选项中互为同系物的是
① 和
和 ②
② 、
、 、
、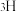 ③
③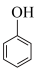 与
与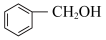 ④
④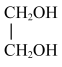 与
与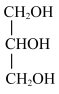 ⑤
⑤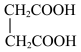 与
与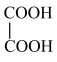 ⑥戊烯和环戊烷 ⑦
⑥戊烯和环戊烷 ⑦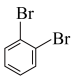 与
与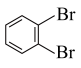
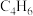 的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为
的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为
您最近一年使用:0次
2024-05-04更新
|
438次组卷
|
3卷引用:辽宁省铁岭市昌图县第一高级中学2023-2024学年高二下学期4月月考化学试卷
解题方法
2 . A~D是四种烃分子的球棍模型(如图)
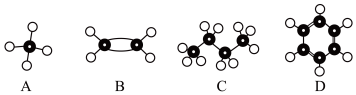
(1)A的分子式___________ 。
(2)能使酸性高锰酸钾溶液褪色的物质是___________ (填序号)。
(3)B的结构简式___________ 。
(4)从下列各组物质中,找出合适的序号填在对应的空格内:
①甲烷和丙烷②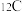 和
和 ③金刚石和石墨④H和D
③金刚石和石墨④H和D
⑤异戊烷( )和新戊烷(
)和新戊烷(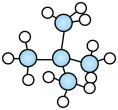 )⑥
)⑥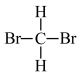 和
和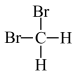
⑦正丁烷和异丁烷⑧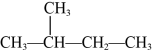 和
和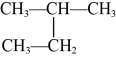 ⑨
⑨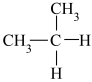 和
和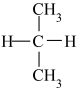
(一)互为同位素的是___________ (填序号,下同)。
(二)互为同分异构体的是___________ 。
(三)互为同系物的是___________ 。
(四)互为同素异形体的是___________ 。
(5)一定温度下,在体积为2 L的恒容密闭容器中充入1 mol N2和3 mol H2,一定条件下发生反应: ,测得其中N2的物质的量随时间的变化如图所示。
,测得其中N2的物质的量随时间的变化如图所示。
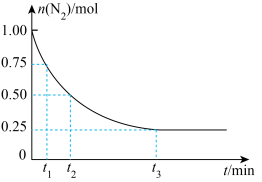
从开始反应到t2 min,氮气的平均反应速率为___________ 。

(1)A的分子式
(2)能使酸性高锰酸钾溶液褪色的物质是
(3)B的结构简式
(4)从下列各组物质中,找出合适的序号填在对应的空格内:
①甲烷和丙烷②
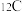 和
和 ③金刚石和石墨④H和D
③金刚石和石墨④H和D⑤异戊烷(
 )和新戊烷(
)和新戊烷( )⑥
)⑥ 和
和
⑦正丁烷和异丁烷⑧
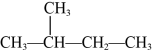 和
和 ⑨
⑨ 和
和
(一)互为同位素的是
(二)互为同分异构体的是
(三)互为同系物的是
(四)互为同素异形体的是
(5)一定温度下,在体积为2 L的恒容密闭容器中充入1 mol N2和3 mol H2,一定条件下发生反应:
 ,测得其中N2的物质的量随时间的变化如图所示。
,测得其中N2的物质的量随时间的变化如图所示。
从开始反应到t2 min,氮气的平均反应速率为
您最近一年使用:0次
名校
3 . 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以合成诸多化合物。
(1)乙炔的电子式为___________ 。
(2)以乙炔为原料可制氯丁橡胶,其过程包括如下反应:

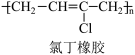
①已知A的分子式为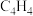 ,A的结构简式为
,A的结构简式为___________ 。
②用系统命名法为B命名,则B的名称为___________ 。
③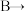 氯丁橡胶的反应的化学方程式为
氯丁橡胶的反应的化学方程式为___________ 。
(3)聚丙烯腈俗称人造羊毛,以乙炔为原料制聚丙烯腈的过程包括如下反应:

①M的化学式为___________ ;
②C的结构简式为___________ ,分子中碳原子的杂化方式为___________ 。
(1)乙炔的电子式为
(2)以乙炔为原料可制氯丁橡胶,其过程包括如下反应:


①已知A的分子式为
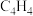 ,A的结构简式为
,A的结构简式为②用系统命名法为B命名,则B的名称为
③
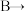 氯丁橡胶的反应的化学方程式为
氯丁橡胶的反应的化学方程式为(3)聚丙烯腈俗称人造羊毛,以乙炔为原料制聚丙烯腈的过程包括如下反应:

①M的化学式为
②C的结构简式为
您最近一年使用:0次
名校
4 . 近年来,人们对微生物的氮转化进行了深入研究,将其归纳为如图1所示过程。请回答下列问题:
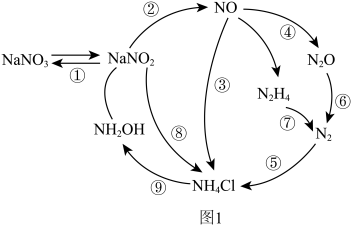
(1)N2的电子式为_____ ;羟胺(NH2OH)的结构式为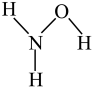 ,属于
,属于_____ (填“离子”或“共价”)化合物。
(2)笑气(N2O)可用作医用麻醉剂、制冷剂,实验室通过加热NH4NO3分解制备N2O,只有两种产物,写出该反应的化学方程式:_____ 。
(3)图1转化过程中具有固氮功能的是_____ (填标号)。
(4)实验室常用氢氧化钙和氯化铵制备氨气,反应装置如图2所示。
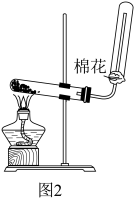
I.写出该反应的化学方程式:_____ 。
Ⅱ.棉花的作用为_____ 。
(5)NaNO2和食盐性状相似,社会上曾多次发生将NaNO2误当食盐食用的事件。可用0.1mol•L-1酸性KMnO4溶液来测定某亚硝酸钠样品中NaNO2的含量(假设杂质不与KMnO4溶液反应),进行三次实验,每次取ag样品,消耗酸性KMnO4溶液的平均体积为20.00mL。测定原理为NO +MnO
+MnO +H+→NO
+H+→NO +Mn2++H2O。
+Mn2++H2O。
I.请配平该离子方程式:_____ 。
Ⅱ.NaNO2的质量分数为_____ %。

(1)N2的电子式为
 ,属于
,属于(2)笑气(N2O)可用作医用麻醉剂、制冷剂,实验室通过加热NH4NO3分解制备N2O,只有两种产物,写出该反应的化学方程式:
(3)图1转化过程中具有固氮功能的是
(4)实验室常用氢氧化钙和氯化铵制备氨气,反应装置如图2所示。

I.写出该反应的化学方程式:
Ⅱ.棉花的作用为
(5)NaNO2和食盐性状相似,社会上曾多次发生将NaNO2误当食盐食用的事件。可用0.1mol•L-1酸性KMnO4溶液来测定某亚硝酸钠样品中NaNO2的含量(假设杂质不与KMnO4溶液反应),进行三次实验,每次取ag样品,消耗酸性KMnO4溶液的平均体积为20.00mL。测定原理为NO
 +MnO
+MnO +H+→NO
+H+→NO +Mn2++H2O。
+Mn2++H2O。I.请配平该离子方程式:
Ⅱ.NaNO2的质量分数为
您最近一年使用:0次
2023-04-18更新
|
402次组卷
|
3卷引用:辽宁省部分学校联考2022-2023学年高一下学期4月月考化学试题
5 . I、下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:
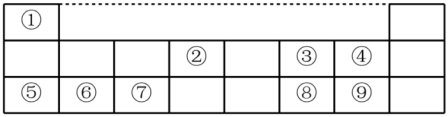
(1)元素⑧在周期表中的位置___________ ;
(2)在①~⑨元素中,某种元素的氧化物可用于呼吸面具中氧气来源,请写出该氧化物的电子式___________
(3)等质量的单质⑦分别与足量的稀硫酸和氢氧化钠溶液反应,相同条件下产生的气体体积之比为___________ 。
(4)①②③⑤可以形成一种盐,①③⑤⑧也能形成一种盐,这两种盐能相互反应,请写出该反应的化学方程式___________ 。
II、
(5)现在含有元素硒( )的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多
)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多 个电子层,则下列叙述中正确的是___________。
个电子层,则下列叙述中正确的是___________。
(6)下列变化:①I2升华;②烧碱熔化;③NaCl溶于水;④HCl溶于水;⑤O2溶于水;⑥NH4HCO3受热分解。其中仅共价键被破坏的是___________ ;(填序号,下同)仅离子键被破坏的是___________ 。
(7)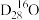 的摩尔质量为
的摩尔质量为___________ ,相同质量的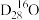 与
与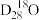 所含中子数之比为
所含中子数之比为___________

(1)元素⑧在周期表中的位置
(2)在①~⑨元素中,某种元素的氧化物可用于呼吸面具中氧气来源,请写出该氧化物的电子式
(3)等质量的单质⑦分别与足量的稀硫酸和氢氧化钠溶液反应,相同条件下产生的气体体积之比为
(4)①②③⑤可以形成一种盐,①③⑤⑧也能形成一种盐,这两种盐能相互反应,请写出该反应的化学方程式
II、
(5)现在含有元素硒(
 )的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多
)的保健品开始进入市场,已知硒元素与氧元素同主族,比氧多 个电子层,则下列叙述中正确的是___________。
个电子层,则下列叙述中正确的是___________。| A.原子序数为34 | B.气态氢化物的稳定性H2Se>H2S |
| C.SeO2不能与氢氧化钠反应 | D.SeO2既有氧化性又有还原性 |
(7)
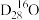 的摩尔质量为
的摩尔质量为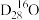 与
与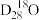 所含中子数之比为
所含中子数之比为
您最近一年使用:0次
解题方法
6 . 元素周期表的发现是近现代化学理论诞生的标志,全世界几乎所有化学教科书后都附有元素周期表。下表为元素周期表的一部分,请回答下列有关问题。
(1)由元素①和④可形成四核 的分子,写出该分子的电子式
的分子,写出该分子的电子式_______ 。
(2)元素④和⑤可构成一种淡黄色固体化合物,写出该化合物与②的最高价氧化物反应的化学方程式_______ 。
(3)元素②、③、④简单氢化物的稳定性由高到低顺序为_______ (用化学式表示)。
(4)元素⑦、⑧、⑨的简单离子半径由大到小顺序为_______ (用离子符号表示)。
(5)写出单质⑥与元素⑤的最高价氧化物对应水化物反应的化学方程式_______ 。
(6)元素的非金属性:⑧_______ ⑩(填“>”或“<”),下列事实不能说明上述结论的是_______ 。
A.元素⑧的单质与⑩的氢化物的水溶液发生反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
F.常温下单质⑧为气态,单质⑩为液态
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
 的分子,写出该分子的电子式
的分子,写出该分子的电子式(2)元素④和⑤可构成一种淡黄色固体化合物,写出该化合物与②的最高价氧化物反应的化学方程式
(3)元素②、③、④简单氢化物的稳定性由高到低顺序为
(4)元素⑦、⑧、⑨的简单离子半径由大到小顺序为
(5)写出单质⑥与元素⑤的最高价氧化物对应水化物反应的化学方程式
(6)元素的非金属性:⑧
A.元素⑧的单质与⑩的氢化物的水溶液发生反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
F.常温下单质⑧为气态,单质⑩为液态
您最近一年使用:0次
2023-01-04更新
|
730次组卷
|
3卷引用:辽宁省重点高中2022-2023学年高一上学期期末联考化学试题
解题方法
7 . 根据题意填空:
(1)表中是几种短周期元素的原子半径及主要化合价。
则L元素的名称是_____ ,R元素在周期表中的位置为_____ 。
(2)某种融雪剂的主要成分为XY2,且X、Y均为周期表中前20号元素。XY2中阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子,则该融雪剂主要成分的电子式为_____ 。
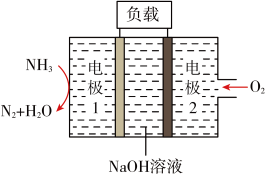
(3)瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池如图所示,该燃料电池工作时,负极的电极反应式为_____ ;电池的总反应为_____ 。
(1)表中是几种短周期元素的原子半径及主要化合价。
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.111 | 0.106 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
则L元素的名称是
(2)某种融雪剂的主要成分为XY2,且X、Y均为周期表中前20号元素。XY2中阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子,则该融雪剂主要成分的电子式为
(3)瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池如图所示,该燃料电池工作时,负极的电极反应式为

您最近一年使用:0次
8 . A~D是四种烃分子的球棍模型(如图)
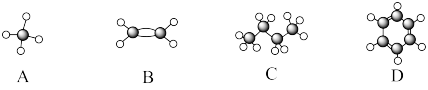
(1)A的分子式_______
(2)能使酸性高锰酸钾溶液褪色的物质是_______ (填序号)。
(3)B的结构简式_______
(4)下列各组物质中,属于同分异构体的是_______ ;
①甲烷和己烷 ②CH3—CH2—CH2—CH3与CH3—CH2—C2H5 ③12C和13C ④O2和O3 ⑤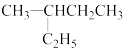 和
和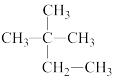

(1)A的分子式
(2)能使酸性高锰酸钾溶液褪色的物质是
(3)B的结构简式
(4)下列各组物质中,属于同分异构体的是
①甲烷和己烷 ②CH3—CH2—CH2—CH3与CH3—CH2—C2H5 ③12C和13C ④O2和O3 ⑤
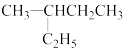 和
和
您最近一年使用:0次
9 . X、Y、Z是三种常见元素的单质,甲、乙是两种常见的化合物,它们之间有如图转化关系。

回答下列问题:
(1)若X基态原子的外围电子排布式为 ,甲是由第二周期两种元素形成的化合物,且会引起温室效应,则Y基态原子的电子排布式为
,甲是由第二周期两种元素形成的化合物,且会引起温室效应,则Y基态原子的电子排布式为_______ ,乙属于_______ (填“离子”或“共价”)化合物。
(2)若基态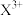 的外围电子排布式为
的外围电子排布式为 ,甲常温下为一种液体,则甲的电子式为
,甲常温下为一种液体,则甲的电子式为___ ,乙的化学式为_______ 。
(3)若X、Y均为金属单质,X基态原子的外围电子排布式为 ,甲为具有磁性的黑色固体,则X原子的电子排布图为
,甲为具有磁性的黑色固体,则X原子的电子排布图为_______ ,Y的价电子排布式为___ 。
(4)若X是最活泼的非金属单质,甲是一种常见的溶剂,则乙分子的电子数为_______ 。

回答下列问题:
(1)若X基态原子的外围电子排布式为
 ,甲是由第二周期两种元素形成的化合物,且会引起温室效应,则Y基态原子的电子排布式为
,甲是由第二周期两种元素形成的化合物,且会引起温室效应,则Y基态原子的电子排布式为(2)若基态
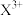 的外围电子排布式为
的外围电子排布式为 ,甲常温下为一种液体,则甲的电子式为
,甲常温下为一种液体,则甲的电子式为(3)若X、Y均为金属单质,X基态原子的外围电子排布式为
 ,甲为具有磁性的黑色固体,则X原子的电子排布图为
,甲为具有磁性的黑色固体,则X原子的电子排布图为(4)若X是最活泼的非金属单质,甲是一种常见的溶剂,则乙分子的电子数为
您最近一年使用:0次
10 . 实验室加热液体时,常加入沸石、其主要成分为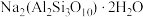 ,根据其组成元素完成下列填空:
,根据其组成元素完成下列填空:
(1)指出 元素在周期表中的位置
元素在周期表中的位置_______ 。
(2)沸石中的元素可形成多种化合物; 元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为
元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为_______ ;化合物乙可作为呼吸面具或潜艇氧气的来源,乙是_______ (填化学式),化合物乙中存在的化学键类型为_______ 。
(3)O元素和其同周期相邻的两种元素分别形成的简单氢化物中最稳定的是_______ (填化学式)。
(4)已知硅酸(H2SiO3)为白色胶状沉淀。
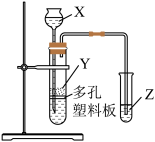
实验室中现有药品:①稀盐酸、②稀硫酸、③NaHCO3固体、④CaCO3固体、⑤Na2SiO3溶液,请选择合适药品利用上述装置设计实验验证C、Si的非金属性的变化规律;装置X、Y、Z处所盛装或放置的药品分别为_______ 、_______ 、_______ (填序号)。但有同学认为该实验所得现象无法充分证明C、Si的非金属性强弱,如何改进?_______ 。
(5)Uue是暂时未合成的化学元素,与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则 中A=
中A=_______ 、Z=_______ 。
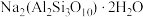 ,根据其组成元素完成下列填空:
,根据其组成元素完成下列填空:(1)指出
 元素在周期表中的位置
元素在周期表中的位置(2)沸石中的元素可形成多种化合物;
 元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为
元素与原子半径最小的元素组成化合物甲,常作强还原剂,化合物甲的电子式为(3)O元素和其同周期相邻的两种元素分别形成的简单氢化物中最稳定的是
(4)已知硅酸(H2SiO3)为白色胶状沉淀。

实验室中现有药品:①稀盐酸、②稀硫酸、③NaHCO3固体、④CaCO3固体、⑤Na2SiO3溶液,请选择合适药品利用上述装置设计实验验证C、Si的非金属性的变化规律;装置X、Y、Z处所盛装或放置的药品分别为
(5)Uue是暂时未合成的化学元素,与Na同主族,位于第八周期,称为类钫,其一种可能存在的核素原子核中有180个中子,则
 中A=
中A=
您最近一年使用:0次



