名校
1 . 氮、氧、硫、氯是四种重要的非金属元素,研究它们的性质及用途对生产、生活、科研具有重要意义。
(1) 、
、 、
、 、
、 等物质常被用作消毒剂。
等物质常被用作消毒剂。
①一氯胺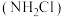 是一种长效缓释水消毒剂,在中性或酸性环境中会发生水解反应,生成一种具有强烈杀菌作用的物质
是一种长效缓释水消毒剂,在中性或酸性环境中会发生水解反应,生成一种具有强烈杀菌作用的物质 ,请写出物质
,请写出物质 的电子式
的电子式___________ 。
②二氧化氯 是一种黄绿色易溶于水的气体,常用于饮用水消毒。工业上可用
是一种黄绿色易溶于水的气体,常用于饮用水消毒。工业上可用 氧化
氧化 溶液制取
溶液制取 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为___________ 。
③等物质的量下列物质消毒效率最高的是___________ (填序号;已知:消毒效率可用单位物质的量的消毒剂的氧化能力衡量)。
a. b.
b. c.
c. d.
d.
(2) 、
、 两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收
两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收 能得到含
能得到含 和
和 的吸收液。写出生成
的吸收液。写出生成 的离子方程式:
的离子方程式:___________ 。若向吸收液中通入过量 ,
, 能与
能与 发生反应生成
发生反应生成 和
和 ,写出该反应的离子方程式:
,写出该反应的离子方程式:___________ 。
(3) 与
与 溶液反应可制取“84”消毒液。用过量的冷
溶液反应可制取“84”消毒液。用过量的冷 溶液吸收氯气,制得
溶液吸收氯气,制得 溶液(不含
溶液(不含 ),此时
),此时 的浓度为
的浓度为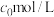 ;加热时
;加热时 能转化为
能转化为 ,测得
,测得 时刻溶液中
时刻溶液中 的浓度为
的浓度为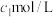 (不考虑加热前后溶液体积的变化)。
(不考虑加热前后溶液体积的变化)。
①写出溶液中 分解生成
分解生成 的化学方程式:
的化学方程式:___________ 。
② 时刻溶液中
时刻溶液中
___________  (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
(1)
 、
、 、
、 、
、 等物质常被用作消毒剂。
等物质常被用作消毒剂。①一氯胺
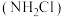 是一种长效缓释水消毒剂,在中性或酸性环境中会发生水解反应,生成一种具有强烈杀菌作用的物质
是一种长效缓释水消毒剂,在中性或酸性环境中会发生水解反应,生成一种具有强烈杀菌作用的物质 ,请写出物质
,请写出物质 的电子式
的电子式②二氧化氯
 是一种黄绿色易溶于水的气体,常用于饮用水消毒。工业上可用
是一种黄绿色易溶于水的气体,常用于饮用水消毒。工业上可用 氧化
氧化 溶液制取
溶液制取 ,该反应中氧化剂与还原剂的物质的量之比为
,该反应中氧化剂与还原剂的物质的量之比为③等物质的量下列物质消毒效率最高的是
a.
 b.
b. c.
c. d.
d.
(2)
 、
、 两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收
两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收 能得到含
能得到含 和
和 的吸收液。写出生成
的吸收液。写出生成 的离子方程式:
的离子方程式: ,
, 能与
能与 发生反应生成
发生反应生成 和
和 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(3)
 与
与 溶液反应可制取“84”消毒液。用过量的冷
溶液反应可制取“84”消毒液。用过量的冷 溶液吸收氯气,制得
溶液吸收氯气,制得 溶液(不含
溶液(不含 ),此时
),此时 的浓度为
的浓度为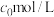 ;加热时
;加热时 能转化为
能转化为 ,测得
,测得 时刻溶液中
时刻溶液中 的浓度为
的浓度为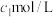 (不考虑加热前后溶液体积的变化)。
(不考虑加热前后溶液体积的变化)。①写出溶液中
 分解生成
分解生成 的化学方程式:
的化学方程式:②
 时刻溶液中
时刻溶液中
 (用含
(用含 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
解题方法
2 . 现有7个化学符号:①18O;②2H;③32S8;④23Na;⑤14N;⑥16O;⑦1H2;⑧12C60;⑨32S2
(1)互为同位素的是_______ ;互为同素异形体的是_______ 。
(2)写出NaOH的电子式_______ ;NH3的结构式 _______ 。
(3)请用电子式表示NaCl 的形成过程:_______ 。
(4)现有以下物质:①H2;②Na2O2;③NaOH;④H2O2;⑤CaCl2;⑥NH4NO3;⑦H2S。其中既有离子键,又有非极性共价键构成的物质是_______ (填序号,下同),属于共价化合物的是_______ 。
(1)互为同位素的是
(2)写出NaOH的电子式
(3)请用电子式表示NaCl 的形成过程:
(4)现有以下物质:①H2;②Na2O2;③NaOH;④H2O2;⑤CaCl2;⑥NH4NO3;⑦H2S。其中既有离子键,又有非极性共价键构成的物质是
您最近一年使用:0次
3 . 用化学用语表示。
(1)氖气_____ ;
(2)碘酒中的溶剂_____ ;
(3)镁离子的结构示意图为_____ ;
(4)标出氢氧化铝中铝元素的化合价_____ 。
(1)氖气
(2)碘酒中的溶剂
(3)镁离子的结构示意图为
(4)标出氢氧化铝中铝元素的化合价
您最近一年使用:0次
名校
4 . 利用如图所示的“价-类”二维图,可以从物质类别、化合价角度认识含氯元素的物质的性质及其转化关系,图中甲~辛均为含氯元素的物质。回答下列问题:
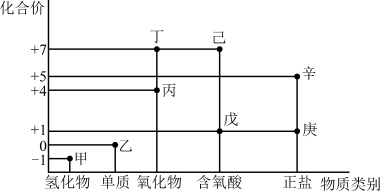
(1)将新制乙的水溶液滴加几滴到干燥的有色纸条上观察到的现象是_____ 。
(2)戊的结构式为______ ;甲、乙、丙、戊中,属于非电解质的是______ (填化学式)。
(3)丙是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂,丙在杀菌消毒过程中会产生副产物亚氯酸盐(ClO ),需将其转化为Cl-除去。下列试剂中,可将ClO
),需将其转化为Cl-除去。下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是_____ (填字母序号)。
a.Fe2(SO4)3 b.HClO4 c.SO2 d.KMnO4
(4)庚是“84”消毒液的有效成分,能有效灭菌,某化学社团模拟生产厂家配制了500mL“84消毒液”,并在瓶体贴上标签,如图所示,回答下列问题:
①写出氯气和NaOH溶液生产此消毒液的离子方程式______ ;该“84消毒液”有效成分的物质的量浓度为_____ (结果保留1位小数)。
②“84消毒液”与稀硫酸混合使用可增强消毒能力,该社团成员用18.0mol/L的浓硫酸配制90mL 0.90mol/L的稀硫酸用于增强“84消毒液”的消毒能力,需要量取上述浓硫酸的体积为_____ mL(结果保留1位小数).若所配制的稀硫酸浓度大于0.90mol/L,则可能的原因是_____ 。
A.配制前,容量瓶未干燥
B.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
C.浓硫酸溶解后未恢复到室温,立即转移至容量瓶定容
D.转移硫酸溶液至容量瓶时,有少量溶液溅出
E.定容时,仰视容量瓶刻度线进行定容

(1)将新制乙的水溶液滴加几滴到干燥的有色纸条上观察到的现象是
(2)戊的结构式为
(3)丙是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂,丙在杀菌消毒过程中会产生副产物亚氯酸盐(ClO
 ),需将其转化为Cl-除去。下列试剂中,可将ClO
),需将其转化为Cl-除去。下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是a.Fe2(SO4)3 b.HClO4 c.SO2 d.KMnO4
(4)庚是“84”消毒液的有效成分,能有效灭菌,某化学社团模拟生产厂家配制了500mL“84消毒液”,并在瓶体贴上标签,如图所示,回答下列问题:
| 84消毒液 有效成分 NaClO 规格 500mL 质量分数 25% 密度 1.19g•cm-3 |
②“84消毒液”与稀硫酸混合使用可增强消毒能力,该社团成员用18.0mol/L的浓硫酸配制90mL 0.90mol/L的稀硫酸用于增强“84消毒液”的消毒能力,需要量取上述浓硫酸的体积为
A.配制前,容量瓶未干燥
B.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
C.浓硫酸溶解后未恢复到室温,立即转移至容量瓶定容
D.转移硫酸溶液至容量瓶时,有少量溶液溅出
E.定容时,仰视容量瓶刻度线进行定容
您最近一年使用:0次
名校
解题方法
5 . 氯化钠是一种重要的化工原料,用它可以制取日常生活中常使的消毒剂、清洁剂等多种物质,如下图所示。
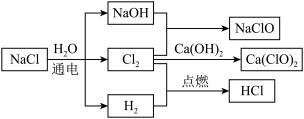
(1)氯元素在周期表中的位置是_______ , 的电子式为
的电子式为_______
(2)下列有关氯气的说法正确的是_______(填字母)。
(3)漂白粉的有效成分是_______ (填化学式);工业上制取漂白粉的化学方程式为_______ 。
(4)曾有报道,因“洁厕灵”(主要成分是盐酸)与“84”消毒液(主要成分是 )混合使用而发生中毒事件,请结合离子方程式分析其原因:
)混合使用而发生中毒事件,请结合离子方程式分析其原因:_______
(5)写出 水溶液通电后发生反应的离子方程式
水溶液通电后发生反应的离子方程式_______

(1)氯元素在周期表中的位置是
 的电子式为
的电子式为(2)下列有关氯气的说法正确的是_______(填字母)。
| A.氯气溶于水只发生化学变化 | B.氯气是黄绿色有毒气体 |
| C.钠在氯气中燃烧产生白烟 | D.将氯气通入鼠洞灭鼠,利用的是氯气易液化和有毒性的性质 |
(4)曾有报道,因“洁厕灵”(主要成分是盐酸)与“84”消毒液(主要成分是
 )混合使用而发生中毒事件,请结合离子方程式分析其原因:
)混合使用而发生中毒事件,请结合离子方程式分析其原因:(5)写出
 水溶液通电后发生反应的离子方程式
水溶液通电后发生反应的离子方程式
您最近一年使用:0次
2023-02-11更新
|
307次组卷
|
2卷引用:重庆市南开中学校2022-2023学年高一上学期期末联合检测化学试题
名校
6 . 按要求填空:现有7个化学符号:18O;14C;32S8;23Na;14N;16O;1H2;12C60;32S2
(1)表示核素的符号共_______ 种;互为同位素的是_______ 和_______ 。
(2)互为同素异形体的是_______ 和_______ 。
(3)写出以下物质的电子式:PH3_______ ;CS2_______ 。
(4)2.2g铵根离子(14ND )的核外电子数是
)的核外电子数是_______ ;某单核微粒含有17个质子,20个中子,18个核外电子,则表示该粒子构成的化学符号是_______ 。
(5)现有以下物质:①H2;②Na2O2;③NaOH;④H2O2;⑤CaCl2;⑥NH4NO3;⑦H2S。其中由离子键和非极性共价键构成的物质是_______ (填序号,下同),属于共价化合物的是_______ 。
(1)表示核素的符号共
(2)互为同素异形体的是
(3)写出以下物质的电子式:PH3
(4)2.2g铵根离子(14ND
 )的核外电子数是
)的核外电子数是(5)现有以下物质:①H2;②Na2O2;③NaOH;④H2O2;⑤CaCl2;⑥NH4NO3;⑦H2S。其中由离子键和非极性共价键构成的物质是
您最近一年使用:0次
名校
7 . I.现有下列十种物质:①液态氯化氢;②小苏打;③固体纯碱;④氨气;⑤葡萄糖;⑥氯化镁;⑦ ;⑧氯水;⑨
;⑧氯水;⑨ ;⑩硫酸铁溶液。
;⑩硫酸铁溶液。
(1)上述十种物质中,属于电解质的有_______ ,属于非电解质的有_______ 。
(2)④的电子式为_______ 。
(3)用电子式表示⑥的形成过程_______ 。
(4)除去③中少量②的相应化学方程式为_______ 。
(5)⑦中含有的化学键为_______ 。
II.写出下列反应的离子方程式(已知还原性: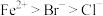 ):
):
(6)向 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 )
)_______ ;
(7)向 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为1∶l∶
的化学计量数之比为1∶l∶_______ 。
 ;⑧氯水;⑨
;⑧氯水;⑨ ;⑩硫酸铁溶液。
;⑩硫酸铁溶液。(1)上述十种物质中,属于电解质的有
(2)④的电子式为
(3)用电子式表示⑥的形成过程
(4)除去③中少量②的相应化学方程式为
(5)⑦中含有的化学键为
II.写出下列反应的离子方程式(已知还原性:
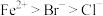 ):
):(6)向
 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 )
)(7)向
 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为1∶l∶
的化学计量数之比为1∶l∶
您最近一年使用:0次
解题方法
8 . I.有机物的表示方法多种多样,下面是常用的有机物的表示方法:
① ②
② ③CH3(CH2)3CH=CH2④CH3CH3⑤
③CH3(CH2)3CH=CH2④CH3CH3⑤ ⑥
⑥ ⑦CH3COOC2H5⑧
⑦CH3COOC2H5⑧ ⑨
⑨ ⑩
⑩ ⑪
⑪
(1)写出⑧的分子式:_______ ;
(2)用系统命名法给⑨命名,其名称为_______ 。
(3)属于酯的是_______ (填序号,下同),与②互为同分异构体的是_______ ;
(4)上述表示方法中属于结构式的为_______ ;属于键线式的为_______ ;
II.有机化合物A常用于食品行业。已知9.0gA在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增加5.4g和13.2g, 经检验剩余气体为O2。
(5)A分子的质谱图如图所示,则A的分子式是_______ 。

(6)A分子的核磁共振氢谱有4组吸收峰,能与NaHCO3溶液发生反应生成CO2气体,峰面积之比是1:1:1:3,则A的结构简式是_______ 。
①
 ②
② ③CH3(CH2)3CH=CH2④CH3CH3⑤
③CH3(CH2)3CH=CH2④CH3CH3⑤ ⑥
⑥ ⑦CH3COOC2H5⑧
⑦CH3COOC2H5⑧ ⑨
⑨ ⑩
⑩ ⑪
⑪
(1)写出⑧的分子式:
(2)用系统命名法给⑨命名,其名称为
(3)属于酯的是
(4)上述表示方法中属于结构式的为
II.有机化合物A常用于食品行业。已知9.0gA在足量O2中充分燃烧,将生成的混合气体依次通过足量的浓硫酸和碱石灰,分别增加5.4g和13.2g, 经检验剩余气体为O2。
(5)A分子的质谱图如图所示,则A的分子式是

(6)A分子的核磁共振氢谱有4组吸收峰,能与NaHCO3溶液发生反应生成CO2气体,峰面积之比是1:1:1:3,则A的结构简式是
您最近一年使用:0次
9 . 下表是有机物A、B的有关信息。
根据表中信息回答下列问题:
(1)A的名称为___________ , A在一定条件下生成高分子化合物的反应方程式___________ 。
(2)写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:___________ 。
(3)B与液溴的混合物中加入铁粉的化学方程式:___________ 。
| A | B |
| ①能使溴的四氯化碳溶液褪色 ②比例模型为:  ③能与水在一定条件下反应生成醇 | ①由C、H两种元素组成 ②球棍模型为:  |
(1)A的名称为
(2)写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:
(3)B与液溴的混合物中加入铁粉的化学方程式:
您最近一年使用:0次
10 . 按要求填空:
(1)乙炔的电子式是___________ ;
(2) 用系统命名法命名为
用系统命名法命名为___________ ; :
:___________ ; :
:___________ 。
(3)2-甲基-1,3-丁二烯的结构简式为___________ ;
(1)乙炔的电子式是
(2)
 用系统命名法命名为
用系统命名法命名为 :
: :
:(3)2-甲基-1,3-丁二烯的结构简式为
您最近一年使用:0次



