名校
解题方法
1 . 下列化学用语使用正确的是
A. 的电子式: 的电子式: |
B.乙醚的结构简式为: |
C. 中C的杂化轨道电子云轮廓图: 中C的杂化轨道电子云轮廓图: |
D. 在水中的电离方程式: 在水中的电离方程式: |
您最近一年使用:0次
2024·浙江·模拟预测
解题方法
2 . 下列说法不正确 的是
A.Fe2+的价层电子轨道表示式为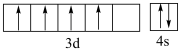 |
B.用电子式表示K2S的形成: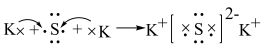 |
| C.HClO的分子的VSEPR模型为四面体形 |
D.聚己二酰己二胺的结构简式: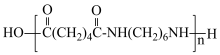 |
您最近一年使用:0次
名校
解题方法
3 . 下列化学用语或图示表达正确的是
A.光导纤维主要成分的分子式: |
B. 的价层电子对互斥模型: 的价层电子对互斥模型: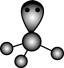 |
C.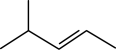 的名称:2-甲基-3-戊烯 的名称:2-甲基-3-戊烯 |
D.基态 的价层电子轨道表示式: 的价层电子轨道表示式: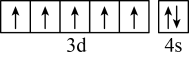 |
您最近一年使用:0次
名校
解题方法
4 . 下列化学用语只能用来表示一种微粒的是
A. | B. |
C. | D. |
您最近一年使用:0次
昨日更新
|
50次组卷
|
2卷引用:河北省唐山市第二中学2024届高三下学期五月联考化学试卷
5 . 下列化学用语或表述正确的是
A.聚丙烯酸的结构简式: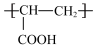 |
B. 的电子式: 的电子式: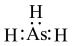 |
| C.基态Mg原子核外电子的空间运动状态有12种 |
D.HBr的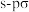 键电子云图: 键电子云图: |
您最近一年使用:0次
2024·上海·模拟预测
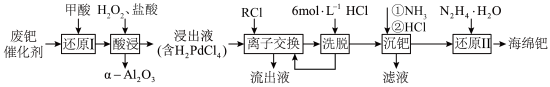
6 . 钯催化剂(主要成分为Pd、α-Al2O3,还含少量铁、铜等)是石油化工中催化加氢和催化氧化等反应的重要催化剂。一种从废钯催化剂中回收海绵钯的工艺流程如下:
②常温下,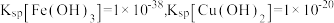 。
。
回答下列问题:
(1)“还原Ⅰ”过程中加入甲酸的主要目的是还原___________ (填化学式)。
(2)“酸浸”过程中Pd转化的离子方程式为___________ 。
(3)“酸浸”过程中温度、固液比对浸取率的影响如图,则“酸浸”最佳条件为___________ 。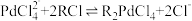 ,流出液通入NH3调节pH后过滤,滤液经一系列操作可以得到CuCl2·2H2O。若假设流出液中各金属离子的浓度均为0.01 mol/L,常温下,需要调节pH的范围是
,流出液通入NH3调节pH后过滤,滤液经一系列操作可以得到CuCl2·2H2O。若假设流出液中各金属离子的浓度均为0.01 mol/L,常温下,需要调节pH的范围是___________ 。
(5)“沉钯”过程钯元素主要发生如下转化:H2PdCl4 (稀溶液) [Pd(NH3)4]Cl2 (稀溶液)
[Pd(NH3)4]Cl2 (稀溶液) [Pd(NH3)2]Cl2(沉淀)。则滤液中溶质的主要成分为
[Pd(NH3)2]Cl2(沉淀)。则滤液中溶质的主要成分为___________ (填化学式)。
(6)N2H4的电子式为___________ 。
(7)“还原Ⅱ”过程中产生无毒无害气体。由[Pd(NH3)2]Cl2生成海绵钯的化学方程式为___________ 。
(8)H2和O2在钯的配合物离子[PdCl4]2-的作用下合成H2O2,反应历程如图。下列说法不正确的是 。
②常温下,
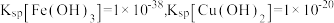 。
。回答下列问题:
(1)“还原Ⅰ”过程中加入甲酸的主要目的是还原
(2)“酸浸”过程中Pd转化的离子方程式为
(3)“酸浸”过程中温度、固液比对浸取率的影响如图,则“酸浸”最佳条件为

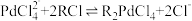 ,流出液通入NH3调节pH后过滤,滤液经一系列操作可以得到CuCl2·2H2O。若假设流出液中各金属离子的浓度均为0.01 mol/L,常温下,需要调节pH的范围是
,流出液通入NH3调节pH后过滤,滤液经一系列操作可以得到CuCl2·2H2O。若假设流出液中各金属离子的浓度均为0.01 mol/L,常温下,需要调节pH的范围是(5)“沉钯”过程钯元素主要发生如下转化:H2PdCl4 (稀溶液)
 [Pd(NH3)4]Cl2 (稀溶液)
[Pd(NH3)4]Cl2 (稀溶液) [Pd(NH3)2]Cl2(沉淀)。则滤液中溶质的主要成分为
[Pd(NH3)2]Cl2(沉淀)。则滤液中溶质的主要成分为(6)N2H4的电子式为
(7)“还原Ⅱ”过程中产生无毒无害气体。由[Pd(NH3)2]Cl2生成海绵钯的化学方程式为
(8)H2和O2在钯的配合物离子[PdCl4]2-的作用下合成H2O2,反应历程如图。下列说法不正确的是 。

| A.H2O2中存在极性键和非极性键 |
| B.[PdCl4]2-中Pd2+提供空轨道形成配位键 |
| C.反应①、②、③均属于氧化还原反应 |
| D.等物质的量的H2和O2发生反应时,反应①和反应②转移的电子数之比为1:1 |
您最近一年使用:0次
名校
解题方法
7 . 下列表示正确的是
A.醛基的电子式: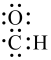 | B.SO2的价层电子对互斥(VSEPR)模型: |
C.H2O2分子的球棍模型: | D.某烷烃名称为:2-甲基-3-乙基戊烷 |
您最近一年使用:0次
名校
8 . 下列化学用语或表述错误的是
A.基态氧原子价电子的轨道表示式为: |
B.基态Al原子最高能级的电子云轮廓图: |
C.离子结构示意图 ,既可以表示 ,既可以表示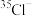 ,也可以表示 ,也可以表示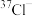 |
| D.次氯酸钠中含有的化学键类型:极性键、离子键 |
您最近一年使用:0次
9 . 下列化学用语使用正确的是
A.NaCl晶体的晶胞: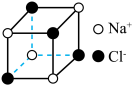 | B. 的化学名称:N-二甲基甲酰胺 的化学名称:N-二甲基甲酰胺 |
C.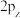 的电子云图: 的电子云图: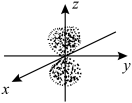 | D.丁二烯的键线式: |
您最近一年使用:0次
名校
解题方法
10 . 下列化学用语的表达正确的是
A.基态铍原子最外层电子的电子云轮廓图: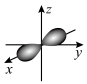 |
B. 的质谱图: 的质谱图: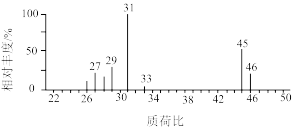 |
C.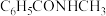 的名称: 的名称: 甲基苯甲酰胺 甲基苯甲酰胺 |
D. 的电子式为 的电子式为 |
您最近一年使用:0次



