名校
解题方法
1 . 下列有关电子式表示正确的是
①次氯酸的电子式: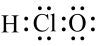
②甲醛的电子式: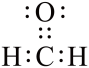
③HCl的电子式:
④由Na和Cl形成离子键的过程: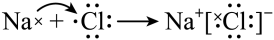
①次氯酸的电子式:
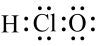
②甲醛的电子式:
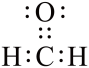
③HCl的电子式:

④由Na和Cl形成离子键的过程:

| A.①③ | B.②③ | C.②④ | D.①④ |
您最近一年使用:0次
名校
2 . 肼(N2H4)是发射航天飞船常用的高能燃料,可通过反应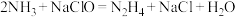 制备。下列有关微粒的描述不正确的是
制备。下列有关微粒的描述不正确的是
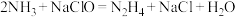 制备。下列有关微粒的描述不正确的是
制备。下列有关微粒的描述不正确的是A.N2H4的结构式为 | B.NH3的电子式为 |
C. 的结构示意图: 的结构示意图: | D.NaClO中存在离子键和共价键 |
您最近一年使用:0次
3 . 下图中反应①是制备 的一种方法,其副产物
的一种方法,其副产物 是优质的镁资源。回答下列问题:
是优质的镁资源。回答下列问题:
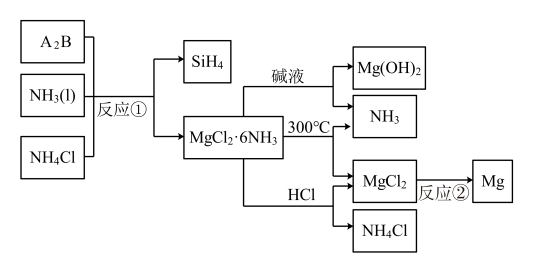
(1) 在元素周期表中的位置:
在元素周期表中的位置:___________ , 的电子式:
的电子式:___________ 。
(2) 的化学式为
的化学式为___________ 。反应②的必备条件是___________ 。上图中可以循环使用的物质有___________ 。
(3)在一定条件下,由 和
和 反应生成
反应生成 和一种固体耐磨材料
和一种固体耐磨材料___________ (写化学式)。
(4)为实现燃煤脱硫,向煤中加入浆状 ,使燃烧产生的
,使燃烧产生的 转化为稳定的
转化为稳定的 化合物,写出该反应的化学方程式:
化合物,写出该反应的化学方程式:___________ 。
(5)用 制成的格式试剂(RMgBr)常用于有机合成,例如制备醇类化合物的合成路线如下:
制成的格式试剂(RMgBr)常用于有机合成,例如制备醇类化合物的合成路线如下:
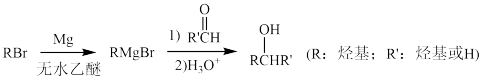
依据上述信息,写出制备 所需醛的可能结构简式:
所需醛的可能结构简式:___________ 。
 的一种方法,其副产物
的一种方法,其副产物 是优质的镁资源。回答下列问题:
是优质的镁资源。回答下列问题:
(1)
 在元素周期表中的位置:
在元素周期表中的位置: 的电子式:
的电子式:(2)
 的化学式为
的化学式为(3)在一定条件下,由
 和
和 反应生成
反应生成 和一种固体耐磨材料
和一种固体耐磨材料(4)为实现燃煤脱硫,向煤中加入浆状
 ,使燃烧产生的
,使燃烧产生的 转化为稳定的
转化为稳定的 化合物,写出该反应的化学方程式:
化合物,写出该反应的化学方程式:(5)用
 制成的格式试剂(RMgBr)常用于有机合成,例如制备醇类化合物的合成路线如下:
制成的格式试剂(RMgBr)常用于有机合成,例如制备醇类化合物的合成路线如下:
依据上述信息,写出制备
 所需醛的可能结构简式:
所需醛的可能结构简式:
您最近一年使用:0次
名校
解题方法
4 . 化学用语是学习化学的重要工具,下列化学用语正确的是
A.丙炔的键线式: |
B.CaO2的电子式: |
C.BF3的空间充填模型: |
D.Fe2+的离子结构示意图: |
您最近一年使用:0次
5 . 联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,回答下列问题:
I、
(1)联氨的结构式为___________ 。
(2)火箭发射时可以用联氨作燃料,NO2作氧化剂,二者反应生成N2和水蒸气。已知:
①2O2(g)+N2(g)=2NO2(g) △H1=+66.4kJ/mol
②N2H4(l)+O2(g)=N2(g)+2H2O(l) △H2=-622.0kJ/mol
③H2O(l)=H2O(g) △H3=+44.0kJ/mol
请写出N2H4(l)与NO2(g)反应的热化学方程式___________ 。
II、肼(N2H4)─空气燃料电池是一种理想的电池,具有容量大、能量转化率高、产物无污染等特点,某学习小组利用该电池来探究某些工业原理,其中乙装置中X为阳离子交换膜(即只允许阳离子通过)。
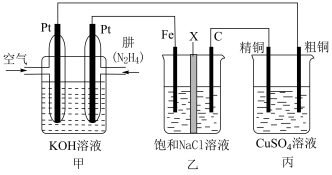
(3)乙装置中石墨电极为___________ 极(填“正”或“负”、“阴”或“阳”),Fe电极反应式为___________ 。
(4)丙装置模拟工业中的粗铜精炼原理,电解后精铜质量增加3.2g,则理论上甲装置中肼消耗质量为___________ g。
(5)如果将丙中的粗铜电极换为Pt电极,该溶液中pH___________ (填“变大”“变小”“不变”),电解一段时间后溶液蓝色变浅,但并未消失,要想把此时的溶液恢复至原状态,需加入适量的___________ (填化学式)。
I、
(1)联氨的结构式为
(2)火箭发射时可以用联氨作燃料,NO2作氧化剂,二者反应生成N2和水蒸气。已知:
①2O2(g)+N2(g)=2NO2(g) △H1=+66.4kJ/mol
②N2H4(l)+O2(g)=N2(g)+2H2O(l) △H2=-622.0kJ/mol
③H2O(l)=H2O(g) △H3=+44.0kJ/mol
请写出N2H4(l)与NO2(g)反应的热化学方程式
II、肼(N2H4)─空气燃料电池是一种理想的电池,具有容量大、能量转化率高、产物无污染等特点,某学习小组利用该电池来探究某些工业原理,其中乙装置中X为阳离子交换膜(即只允许阳离子通过)。

(3)乙装置中石墨电极为
(4)丙装置模拟工业中的粗铜精炼原理,电解后精铜质量增加3.2g,则理论上甲装置中肼消耗质量为
(5)如果将丙中的粗铜电极换为Pt电极,该溶液中pH
您最近一年使用:0次
解题方法
6 . 下列化学用语使用正确的是
A.乙烯的电子式: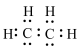 | B. 的离子结构示意图: 的离子结构示意图: |
| C.Fe2+的价层电子排布式:3d5 | D.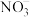 的空间结构:平面三角形 的空间结构:平面三角形 |
您最近一年使用:0次
解题方法
7 . Ⅰ.下列均为中学化学中常见的物质:①明矾 ②氯化铁溶液 ③水玻璃 ④纯碱 ⑤硅酸钠 ⑥过氧化钠 ⑦小苏打 ⑧干冰。
(1)属于电解质的有___________ (填序号)。
(2)写出⑥的电子式___________ ,利用上述物质证明碳酸酸性比硅酸强的化学方程式为___________ 。
(3)明矾净水的原理是___________ 。
Ⅱ.在Na+浓度为0.5 mol/L的某澄清溶液中,还可能含有K+、Ag+、Ba2+、 、
、 、
、 等离子,取该溶液100 mL进行下图连续实验(所加试剂均过量,气体全部逸出)。
等离子,取该溶液100 mL进行下图连续实验(所加试剂均过量,气体全部逸出)。

(4)该溶液中除Na+外,肯定不存在的离子是___________ (填离子符号,下同),肯定存在的离子是___________ ,可能存在的离子是___________ 。
(1)属于电解质的有
(2)写出⑥的电子式
(3)明矾净水的原理是
Ⅱ.在Na+浓度为0.5 mol/L的某澄清溶液中,还可能含有K+、Ag+、Ba2+、
 、
、 、
、 等离子,取该溶液100 mL进行下图连续实验(所加试剂均过量,气体全部逸出)。
等离子,取该溶液100 mL进行下图连续实验(所加试剂均过量,气体全部逸出)。
(4)该溶液中除Na+外,肯定不存在的离子是
您最近一年使用:0次
8 . 请回答:
(1)Na2O2的电子式___________ 。
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由___________ 。
(3)KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为
_______KClO3+_______HCl(浓)=_______KCl+_______ClO2↑+_______Cl2↑+_______
① 请配平上述化学方程式。___________
② 浓盐酸在反应中显示出来的性质是___________
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③若反应中生成标准状况下13.44L气体,则消耗还原剂的物质的量为___________ 。
④ClO2具有很强的氧化性,常用作消毒剂,其消毒的效率(以单位物质的量得到的电子数表示)是H2O2的___________ 倍。
(4)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为___________ 。
(1)Na2O2的电子式
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由
(3)KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为
_______KClO3+_______HCl(浓)=_______KCl+_______ClO2↑+_______Cl2↑+_______

① 请配平上述化学方程式。
② 浓盐酸在反应中显示出来的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③若反应中生成标准状况下13.44L气体,则消耗还原剂的物质的量为
④ClO2具有很强的氧化性,常用作消毒剂,其消毒的效率(以单位物质的量得到的电子数表示)是H2O2的
(4)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
您最近一年使用:0次
解题方法
9 . 制备氢氧化铝的化学方程式是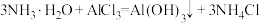 。下列说法正确的是
。下列说法正确的是
① 的结构示意图:
的结构示意图: ;②
;② 的电子式:
的电子式: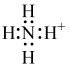 ;③
;③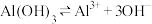 ;
;
④ 的比例模型:
的比例模型: ;⑤
;⑤ 是离子化合物,只含有离子键。
是离子化合物,只含有离子键。
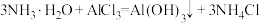 。下列说法正确的是
。下列说法正确的是①
 的结构示意图:
的结构示意图: ;②
;② 的电子式:
的电子式: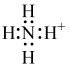 ;③
;③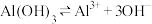 ;
;④
 的比例模型:
的比例模型: ;⑤
;⑤ 是离子化合物,只含有离子键。
是离子化合物,只含有离子键。| A.①③④ | B.①②⑤ | C.③④ | D.④⑤ |
您最近一年使用:0次
名校
解题方法
10 . 已知COS分子的结构类似于二氧化碳且各原子都达到8电子稳定结构,下列正确的是
A.COS的电子式为: | B.COS 是非极性分子 |
| C.COS沸点高于CO2 | D.COS完全燃烧后得到的氧化产物是CO2和SO2 |
您最近一年使用:0次



