名校
1 . 下列叙述正确的是
| A.熟石膏的化学式:CaSO4·2H2O |
B.过氧化钠的电子式:  |
C.基态氧原子的电子排布图: |
D.Ba(OH)2溶液中滴入少量稀硫酸发生反应的离子方程式: |
您最近一年使用:0次
2024-03-19更新
|
676次组卷
|
4卷引用:山东省名校联盟2024届高三下学期5月模拟考试化学试题
(已下线)山东省名校联盟2024届高三下学期5月模拟考试化学试题辽宁省辽阳市2024届高三第一次模拟考试化学试卷2024届吉林省通化市梅河口市第五中学高三下学期一模化学试题(已下线)化学(辽宁卷02)-2024年高考押题预测卷
名校
解题方法
2 . 下列有关化学用语正确的是
A.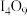 (碘酸碘)中碘的化合价为 (碘酸碘)中碘的化合价为 、 、 |
B.用电子式表示氧化钠的形成过程: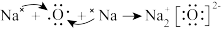 |
C.HF分子间的氢键: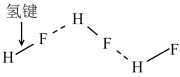 |
D.砷原子结构示意图: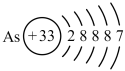 |
您最近一年使用:0次
2022-06-01更新
|
657次组卷
|
3卷引用:山东省泰安市2023届高三下学期二模考试化学试题
名校
解题方法
3 . 下列有关化学用语的表述正确的是
A.中子数是20的氯原子: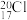 |
B.氢化锂(LiH)中氢离子结构示意图: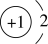 |
C.一氧化碳的结构式: |
D. 水解的离子方程式: 水解的离子方程式: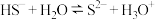 |
您最近一年使用:0次
2022-04-08更新
|
633次组卷
|
4卷引用:山东省青岛市2022高考一模化学试题
名校
解题方法
4 . 化学用语可以表达化学过程。下列化学用语的表达错误的是
A.用离子方程式表示铜在氨水中被腐蚀: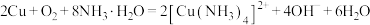 |
B.用电子式表示水分子的形成过程: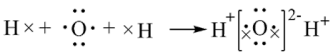 |
C.牙膏中添加氟化物能预防龋齿的原因: |
D.用化学方程式表示钢铁表面进行“烤蓝”处理: |
您最近一年使用:0次
2024-03-17更新
|
401次组卷
|
2卷引用:2024届山东省泰安肥城市高考仿真模拟(一)化学试题
解题方法
5 . 砷的化合物可用于半导体领域,如我国“天宫”空间站的核心舱“天和号”就是采用砷化镓薄膜电池来供电。一种从酸性高浓度含砷废水[砷主要以亚砷酸( )形式存在]中回收砷的工艺流程如下:
)形式存在]中回收砷的工艺流程如下:
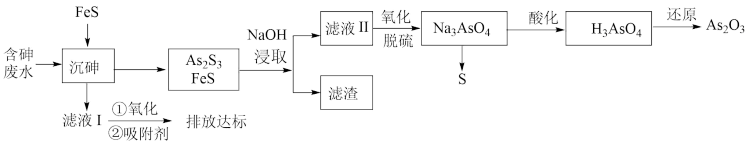
已知:
Ⅰ.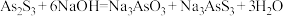
Ⅱ.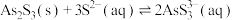
Ⅲ.砷酸( )在酸性条件下有强氧化性,能被
)在酸性条件下有强氧化性,能被 、氢碘酸等还原
、氢碘酸等还原
(1) 中砷元素的化合价为
中砷元素的化合价为___________ 价。
(2)“沉砷”过程中FeS是否可以用过量的 替换
替换___________ (填“是”或“否”);请从平衡移动的角度解释原因:___________ 。
(3)向滤液Ⅱ中通入氧气进行“氧化脱硫”,请写出脱硫的离子反应方程式___________ 。
(4)用 “还原”过程中,若需检验还原后溶液中是否仍存在砷酸。则还需要的实验试剂有
“还原”过程中,若需检验还原后溶液中是否仍存在砷酸。则还需要的实验试剂有___________ 。
(5)已知:常温下,pH>7.1时,吸附剂表面带负电,pH越大,吸附剂表面带的负电荷越多;pH<7.1时,吸附剂表面带正电,pH越小,吸附剂表面带的正电荷越多。
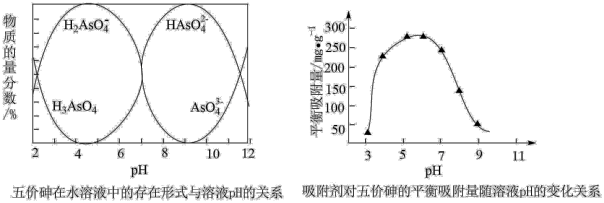
当溶液pH介于7~9,吸附剂对五价砷的平衡吸附量随pH的升高而下降,试分析其原因_____ 。
(6)含砷废水也可采用另一种化学沉降法处理:向废水中先加入适量氧化剂,再加入生石灰调节pH,将砷元素转化为 沉淀。若沉降后上层清液中
沉淀。若沉降后上层清液中 为
为 mol/L,则溶液中
mol/L,则溶液中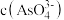 的浓度为
的浓度为_____ mol/L。该处理后的溶液是否符合国家排放标准___________ (填“是”或“否”)。(已知: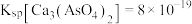 ,国家规定工业废水排放中砷元素含量<0.5mg/L)
,国家规定工业废水排放中砷元素含量<0.5mg/L)
 )形式存在]中回收砷的工艺流程如下:
)形式存在]中回收砷的工艺流程如下:
已知:
Ⅰ.
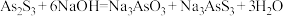
Ⅱ.
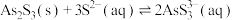
Ⅲ.砷酸(
 )在酸性条件下有强氧化性,能被
)在酸性条件下有强氧化性,能被 、氢碘酸等还原
、氢碘酸等还原(1)
 中砷元素的化合价为
中砷元素的化合价为(2)“沉砷”过程中FeS是否可以用过量的
 替换
替换(3)向滤液Ⅱ中通入氧气进行“氧化脱硫”,请写出脱硫的离子反应方程式
(4)用
 “还原”过程中,若需检验还原后溶液中是否仍存在砷酸。则还需要的实验试剂有
“还原”过程中,若需检验还原后溶液中是否仍存在砷酸。则还需要的实验试剂有(5)已知:常温下,pH>7.1时,吸附剂表面带负电,pH越大,吸附剂表面带的负电荷越多;pH<7.1时,吸附剂表面带正电,pH越小,吸附剂表面带的正电荷越多。

当溶液pH介于7~9,吸附剂对五价砷的平衡吸附量随pH的升高而下降,试分析其原因
(6)含砷废水也可采用另一种化学沉降法处理:向废水中先加入适量氧化剂,再加入生石灰调节pH,将砷元素转化为
 沉淀。若沉降后上层清液中
沉淀。若沉降后上层清液中 为
为 mol/L,则溶液中
mol/L,则溶液中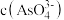 的浓度为
的浓度为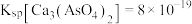 ,国家规定工业废水排放中砷元素含量<0.5mg/L)
,国家规定工业废水排放中砷元素含量<0.5mg/L)
您最近一年使用:0次
6 . 3D打印对钛粉末的要求很高。熔盐电解精炼是制取钛粉的有效途径。精炼时一般采用等摩尔比的KCl-NaCl熔盐,其中含有一定浓度的低价氯化钛(TiClx,x=2、3)。(已知:①熔盐中Ti3+少,Ti2+多熔盐电解精炼制得的钛粉颗粒相对粗大;②钛的熔点为1668℃,TiCl4熔点-24. 1℃、沸点136. 4℃)。
(1)精炼时,粗品质的海绵钛、废钛材等做电解池的_______ 极。
(2)采用海绵钛与TiCl4制取低价钛离子的电解质熔盐时,熔盐中存下如下4个反应:
ⅰ.3Ti4++Ti0→4Ti3+△H1
ⅱ.Ti4++Ti0→2Ti2+△H2
ⅲ.Ti4++Ti2+→2Ti3+△H3
ⅳ._______ △H4
①反应ⅳ的化学方程式为_______ 。
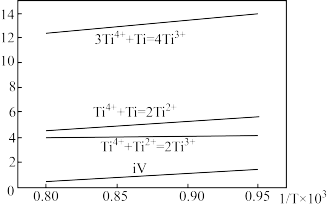
②上述4个反应的平衡常数与温度的关系如下图。由此可知△H1_______ 3△H2(填“>”、“<”或“=”)。
③有助于制取低价钛离子的电解质熔盐的措施为_______ 。
(3)向下图装置中加入海绵钛,从石英管中缓慢加入a mol TiCl4,恒温条件下进行反应。
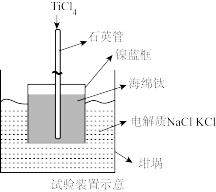
①平衡时,测得消耗海绵钛及TiCl4的物质的量分别为b mol、c mol。熔盐中低价钛离子的平均价态为_______ 。
②用各离子的物质的量分数表示平衡浓度,则反应ⅲ的平衡常数K3=_______ 。
③若向此平衡体系中继续注入TiCl4,则再次平衡后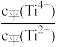
_______ (填“增大”、“减小”或“不变”)
(4)电解精炼制钛粉,偶尔会得到一些相对粗大的钛粉颗粒而影响产品质量,请分析产生的原因_______ (写出1条原因,合理即可。)
(1)精炼时,粗品质的海绵钛、废钛材等做电解池的
(2)采用海绵钛与TiCl4制取低价钛离子的电解质熔盐时,熔盐中存下如下4个反应:
ⅰ.3Ti4++Ti0→4Ti3+△H1
ⅱ.Ti4++Ti0→2Ti2+△H2
ⅲ.Ti4++Ti2+→2Ti3+△H3
ⅳ._______ △H4
①反应ⅳ的化学方程式为
②上述4个反应的平衡常数与温度的关系如下图。由此可知△H1

③有助于制取低价钛离子的电解质熔盐的措施为
(3)向下图装置中加入海绵钛,从石英管中缓慢加入a mol TiCl4,恒温条件下进行反应。

①平衡时,测得消耗海绵钛及TiCl4的物质的量分别为b mol、c mol。熔盐中低价钛离子的平均价态为
②用各离子的物质的量分数表示平衡浓度,则反应ⅲ的平衡常数K3=
③若向此平衡体系中继续注入TiCl4,则再次平衡后
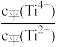
(4)电解精炼制钛粉,偶尔会得到一些相对粗大的钛粉颗粒而影响产品质量,请分析产生的原因
您最近一年使用:0次
解题方法
7 . 下列化学用语正确的是
A. 的比例模型: 的比例模型: |
B.丙醛的键线式: |
C.次氯酸的电子式: |
D. 的电离方程式: 的电离方程式: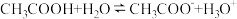 |
您最近一年使用:0次
解题方法
8 . 下列相关化学用语表述正确的是
A.乙醇的球棍模型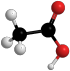 |
B.次氯酸的电子式 |
C.1个丙酮( )分子中含有3个σ键 )分子中含有3个σ键 |
D.碳酸氢钠的电离方程式: NaHCO3 Na+ + HCO Na+ + HCO |
您最近一年使用:0次
名校
9 . 下列化学用语或描述中,不正确的有
①F-的结构示意图:
②氢氧根的电子式:
③HClO的结构式:H—Cl—O
④SO3的水溶液能导电,说明SO3是电解质
⑤NaHSO3在水中的电离方程式:NaHSO3=Na++H++SO32-
⑥同素异形体间的转化和同位素间的转化都是化学变化
①F-的结构示意图:

②氢氧根的电子式:

③HClO的结构式:H—Cl—O
④SO3的水溶液能导电,说明SO3是电解质
⑤NaHSO3在水中的电离方程式:NaHSO3=Na++H++SO32-
⑥同素异形体间的转化和同位素间的转化都是化学变化
| A.1项 | B.2项 | C.5项 | D.6项 |
您最近一年使用:0次
2018-10-22更新
|
1182次组卷
|
4卷引用:山东省临沂市第十九中学2019届高三上学期第三次质量调研考试化学试题
解题方法
10 . 由一种阳离子与两种酸根阴离子组成的盐称为混盐。向混盐Na4S2O3中加入足量稀硫酸,发生反应: 。下列说法正确的是( )
。下列说法正确的是( )
 。下列说法正确的是( )
。下列说法正确的是( )| A. Na4S2O3的水溶液显碱性 |
| B.1mol Na4S2O3中共含离子数为5NA |
| C.上述反应中,每产生3molS,转移电子的物质的量为6mol |
| D.CaOCl2也可称为混盐,向CaOCl2中加入足量稀硫酸会有Cl2产生 |
您最近一年使用:0次
2020-06-11更新
|
517次组卷
|
3卷引用:山东省日照市2020届高三校际联合考试(二模)化学试题



