名校
解题方法
1 . 卤族元素相关物质在生产、生活中应用广泛。回答下列问题:
(1) 的离子结构示意图为
的离子结构示意图为______ 。
(2)卤素单质有着相似的化学性质,但同时也有差别。比如 与NaOH反应生成NaCl、NaClO和水,而
与NaOH反应生成NaCl、NaClO和水,而 与NaOH发生如下反应:
与NaOH发生如下反应: 。其中
。其中 的电子式为
的电子式为______ ,用电子式描述NaF的形成过程:______ 。
(3)根据卤族元素性质的相似性和递变性,推测元素砹(At)的单质为有色固体,HAt的稳定性______ (填“大于”或“小于”)HI的稳定性,AgAt______ (填“易”或“难”)溶于水。
(4)不同卤素原子之间以共价键相结合形成的化合物称为卤素互化物,如 等。它们与卤素单质性质相似。
等。它们与卤素单质性质相似。
① 与水反应的产物可能为
与水反应的产物可能为______ (填化学式)。
②下列说法不正确的是______ 。
A.HF、HCl、HBr的沸点依次升高
B. 沸点依次升高
沸点依次升高
C.已知离子半径大小会影响离子键的强弱,从而影响物质的熔点:若离子半径越大,离子键越弱。据此推测NaF、NaCl、NaBr熔点依次降低
D. (X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
(X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
(1)
 的离子结构示意图为
的离子结构示意图为(2)卤素单质有着相似的化学性质,但同时也有差别。比如
 与NaOH反应生成NaCl、NaClO和水,而
与NaOH反应生成NaCl、NaClO和水,而 与NaOH发生如下反应:
与NaOH发生如下反应: 。其中
。其中 的电子式为
的电子式为(3)根据卤族元素性质的相似性和递变性,推测元素砹(At)的单质为有色固体,HAt的稳定性
(4)不同卤素原子之间以共价键相结合形成的化合物称为卤素互化物,如
 等。它们与卤素单质性质相似。
等。它们与卤素单质性质相似。①
 与水反应的产物可能为
与水反应的产物可能为②下列说法不正确的是
A.HF、HCl、HBr的沸点依次升高
B.
 沸点依次升高
沸点依次升高C.已知离子半径大小会影响离子键的强弱,从而影响物质的熔点:若离子半径越大,离子键越弱。据此推测NaF、NaCl、NaBr熔点依次降低
D.
 (X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
(X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
您最近一年使用:0次
2024-04-04更新
|
197次组卷
|
2卷引用:重庆市巴蜀中学校2023-2024学年高一下学期3月月考化学试题
2 . 电子在原子核外的区域内作高速运动,根据电子的能量高低划分为电子层,在各电子层上电子的排布也遵循着一定的规律。
(1)下列所列各项中,与元素的化学性质关系最密切的是
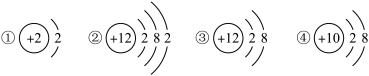
(2)下列是几种粒子的结构示意图,有关说法正确的是
(3)反应8NH3+3Cl2=6NH4Cl+N2可用于氯气管道的检漏。下列表示相关微粒的表示或说法正确的是
(1)下列所列各项中,与元素的化学性质关系最密切的是
| A.元素的相对原子质量 | B.元素的核电荷数 |
| C.原子的核外电子数 | D.原子的最外层电子数 |

| A.①和②两种粒子的化学性质相似 | B.③和④均属于离子结构示意图 |
| C.粒子②在化学反应中容易失去电子 | D.①②③④共表示四种元素的粒子 |
A.中子数为9的氮原子: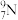 | B.每个NH3分子中含10个电子 |
C.N原子的电子式: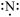 | D.Cl的结构示意图: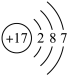 |
您最近一年使用:0次
名校
解题方法
3 . 原子结构与化学键
人们运用化学科学,从分子、原子水平上研究了物质及其变化规律。原子结构理论和化学键理论从微观层次揭示了物质的结构。
(1)日本的福岛核废水中含有一种对环境有害的放射性核素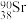 ,关于该核素说法错误是___________。
,关于该核素说法错误是___________。
(2)硒是人体必需的微量元素,如图是元素硒的信息,关于硒元素的说法错误的是___________。

(3)下列性质的比较,不能用元素周期律解释的是___________。
(4)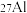 是地壳中最丰富的金属元素,其原子含有中子数为
是地壳中最丰富的金属元素,其原子含有中子数为___________ ,与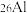 互为
互为___________ 。用化学符号表示铝离子的结构示意图___________ 。A1与 两种微粒在结构上相同的是
两种微粒在结构上相同的是___________ (填选项字母)。
A.质子数 B.核外电子数 C.电子层数 D.最外层电子数
(5)汽车安全气囊中的填充物有 (叠氮酸钠)、
(叠氮酸钠)、 、
、 等物质,
等物质, 遇撞击时能生成金属钠和
遇撞击时能生成金属钠和 ,气囊的体积迅速膨胀,达到保护驾乘人员的目的。
,气囊的体积迅速膨胀,达到保护驾乘人员的目的。
①写出 的电子式
的电子式___________ 。
② 是由一种单原子离子和一种多原子离子以1∶1的比例构成的化合物。
是由一种单原子离子和一种多原子离子以1∶1的比例构成的化合物。 晶体中存在的化学键类型是
晶体中存在的化学键类型是___________ 。
③汽车安全气囊填充物的三种物质中属于共价化合物的是___________ (填化学式),所涉及的5种元素中,原子半径最大的是___________ (填元素符号)。
④某品牌汽车的安全气囊中若有13g ,遇撞击时能产生气体
,遇撞击时能产生气体___________ L(标准状况下),转移电子___________ mol。
(6) 、
、 能与金属钠发生反应生成
能与金属钠发生反应生成 ,化学方程式如下所示:
,化学方程式如下所示:
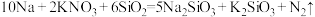
①用单线桥法在上述的化学方程式中标出电子转移的方向和数目___________ 。
②上述反应中氧化剂是___________ (填写化学式,下同),氧化产物是___________ 。
人们运用化学科学,从分子、原子水平上研究了物质及其变化规律。原子结构理论和化学键理论从微观层次揭示了物质的结构。
(1)日本的福岛核废水中含有一种对环境有害的放射性核素
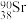 ,关于该核素说法错误是___________。
,关于该核素说法错误是___________。A.与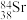 的化学性质几乎相同 的化学性质几乎相同 | B.中子数与质子数之差为52 |
C.与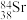 互为同位素 互为同位素 | D.Sr在元素周期表中位于ⅡA族 |

| A.位于ⅥA族 | B.质量数为34 |
| C.位于第四周期 | D.相对原子质量为78.96 |
| A.非金属性:F>O>N |
| B.碱性:KOH>NaOH>LiOH |
C.热稳定性: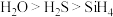 |
D.酸性: |
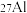 是地壳中最丰富的金属元素,其原子含有中子数为
是地壳中最丰富的金属元素,其原子含有中子数为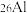 互为
互为 两种微粒在结构上相同的是
两种微粒在结构上相同的是A.质子数 B.核外电子数 C.电子层数 D.最外层电子数
(5)汽车安全气囊中的填充物有
 (叠氮酸钠)、
(叠氮酸钠)、 、
、 等物质,
等物质, 遇撞击时能生成金属钠和
遇撞击时能生成金属钠和 ,气囊的体积迅速膨胀,达到保护驾乘人员的目的。
,气囊的体积迅速膨胀,达到保护驾乘人员的目的。①写出
 的电子式
的电子式②
 是由一种单原子离子和一种多原子离子以1∶1的比例构成的化合物。
是由一种单原子离子和一种多原子离子以1∶1的比例构成的化合物。 晶体中存在的化学键类型是
晶体中存在的化学键类型是③汽车安全气囊填充物的三种物质中属于共价化合物的是
④某品牌汽车的安全气囊中若有13g
 ,遇撞击时能产生气体
,遇撞击时能产生气体(6)
 、
、 能与金属钠发生反应生成
能与金属钠发生反应生成 ,化学方程式如下所示:
,化学方程式如下所示: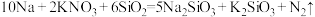
①用单线桥法在上述的化学方程式中标出电子转移的方向和数目
②上述反应中氧化剂是
您最近一年使用:0次
4 . 请按要求书写:
(1)写出丙烷的结构简式:_______ 。
(2)甲烷的电子式为:_______ 。
(3)乙烯与氯化氢化学反应为:_______ 。
(4)写出少量二氧化碳气体中通入硅酸钠溶液的化学方程式:_______ 。
(5)写出硫化氢溶液中通入二氧化硫气体的化学方程式:_______ 。
(6)乙烷与氯气光照生成一氯代物的化学方程式_______ 。
(7)相对分子质量为72的烷烃的分子式为_______ ,其中直链烷烃的习惯命名为_______ 。
(8)焦炭和石英高温条件下制粗硅的化学方程式_______ 。
(9)实验室制氨气的化学方程式_______ 。
(1)写出丙烷的结构简式:
(2)甲烷的电子式为:
(3)乙烯与氯化氢化学反应为:
(4)写出少量二氧化碳气体中通入硅酸钠溶液的化学方程式:
(5)写出硫化氢溶液中通入二氧化硫气体的化学方程式:
(6)乙烷与氯气光照生成一氯代物的化学方程式
(7)相对分子质量为72的烷烃的分子式为
(8)焦炭和石英高温条件下制粗硅的化学方程式
(9)实验室制氨气的化学方程式
您最近一年使用:0次
解题方法
5 . 填空。
(1)①写出高温结构陶瓷氮化硅的化学式_______ ;
②写出硬脂酸甘油酯的结构简式_______ ;
(2)已知NaCN中C、N原子最外层均满足8电子结构,写出NaCN的电子式_______ 。
(3)甲醇的标准燃烧热为726.5kJ/mol,写出甲醇燃烧的热化学方程式_______ 。
(1)①写出高温结构陶瓷氮化硅的化学式
②写出硬脂酸甘油酯的结构简式
(2)已知NaCN中C、N原子最外层均满足8电子结构,写出NaCN的电子式
(3)甲醇的标准燃烧热为726.5kJ/mol,写出甲醇燃烧的热化学方程式
您最近一年使用:0次
名校
解题方法
6 . 回答下列问题:
(1)常用作油漆、涂料的红色颜料(填写化学式)_______ ;
(2)写出NaOH的电子式_______ ;
(3)比较沸点:H2O_______ H2S(填“>”“<”“=”),并解释原因_______ 。
(1)常用作油漆、涂料的红色颜料(填写化学式)
(2)写出NaOH的电子式
(3)比较沸点:H2O
您最近一年使用:0次
2022-02-22更新
|
186次组卷
|
2卷引用:浙江省舟山市定海一中2021-2022学年度高一5月适应性考试化学试题
7 . 非金属及其化合物种类繁多,用途广泛,在化工生产和经济发展中具有重要地位。
(1)写出工业制硝酸的基础——氨的催化氧化___________
(2)为进一步减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2的方法来除去SO2.写出该反应的化学方程式:___________
(3)(NH4)2Fe(SO4)2是一种重要的硫酸盐,写出其电离方程式___________
(4)用电子式表示MgCl2的形成过程___________
(1)写出工业制硝酸的基础——氨的催化氧化
(2)为进一步减少SO2的污染并变废为宝,我国正在探索在一定条件下用CO还原SO2的方法来除去SO2.写出该反应的化学方程式:
(3)(NH4)2Fe(SO4)2是一种重要的硫酸盐,写出其电离方程式
(4)用电子式表示MgCl2的形成过程
您最近一年使用:0次
名校
解题方法
8 . 用化学用语表达:
(1)Na2O2的电子式_______ ,N2H4的电子式为:_______ 。
(2)C2H2的结构式为:_______ ,COS的结构式为:_______ 。
(3)用电子式表示下列过程:
①CaCl2的形成过程_______
②H2O2的形成过程_______
(1)Na2O2的电子式
(2)C2H2的结构式为:
(3)用电子式表示下列过程:
①CaCl2的形成过程
②H2O2的形成过程
您最近一年使用:0次
解题方法
9 . 写出新戊烷的结构简式:_______ ,小苏打的化学式:_______ 。质量数为80,中子数为45的原子符号_______ ,淀粉的分子式_______ 。
您最近一年使用:0次
名校
解题方法
10 . 填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的化学符号:________ 。
(2)周期表中位于第8纵行的铁元素属于第________ 族。
(3)下列几种物质:①Ca(OH)2②H2O2③He④H2S ⑤MgCl2 ,只含有离子键的是(选填序号,下同)_________ ;只含有极性共价键的化合物是________ ;
(4)HClO的结构式______ ,I2的电子式______ 。
(5)下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④蔗糖溶液水⑤硫酸溶于水;未破坏化学键的是_____ ;
(6)下列不能说明氯元素原子得电子能力比硫元素原子得电子能力强的是_____________
①HCl的溶解度比H2S的大 ②HCl的酸性比H2S的强 ③HCl的稳定性比H2S的强④Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑤HClO4的酸性比H2SO4的强 ⑥Cl2能与H2S反应生成S
(1)写出表示含有8个质子、10个中子的原子的化学符号:
(2)周期表中位于第8纵行的铁元素属于第
(3)下列几种物质:①Ca(OH)2②H2O2③He④H2S ⑤MgCl2 ,只含有离子键的是(选填序号,下同)
(4)HClO的结构式
(5)下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④蔗糖溶液水⑤硫酸溶于水;未破坏化学键的是
(6)下列不能说明氯元素原子得电子能力比硫元素原子得电子能力强的是
①HCl的溶解度比H2S的大 ②HCl的酸性比H2S的强 ③HCl的稳定性比H2S的强④Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑤HClO4的酸性比H2SO4的强 ⑥Cl2能与H2S反应生成S
您最近一年使用:0次
2020-07-16更新
|
676次组卷
|
3卷引用:重庆市杨家坪中学2020-2021学年高一上学期1月月考化学试题



