名校
解题方法
1 . 向Fe2O3和铁粉的混合物中加入适量稀H2SO4,各物质恰好完全反应,测得溶液中不含Fe3+,且生成的Fe2+与H2的物质的量之比为4:1,那么该反应中Fe2O3、Fe、H2SO4的物质的量之比为
| A.1:1:1 |
| B.1:2:3 |
| C.1:2:4 |
| D.2:3:5 |
您最近一年使用:0次
2022-01-26更新
|
786次组卷
|
19卷引用:浙江省宁波市慈溪中学2019届高三化学二轮复习:化学计算
浙江省宁波市慈溪中学2019届高三化学二轮复习:化学计算2020届高三化学无机化学二轮专题复习——铁及其化合物的相关计算2【精编24题】山西省忻州市第一中学2016-2017学年高一必修一:3.2.3几种重要的金属化合物同步练习化学试题陕西省西安市长安区第一中学2017-2018学年高一上学期第二次月考化学(实验班)试题山西省朔州市应县第一中学2019届高三9月月考化学试题江西省奉新县第一中学2018-2019学年高一上学期第三次月考化学试题黑龙江省大庆市铁人中学2018-2019学年高一下学期开学考试化学试题湖南省张家界市民族中学2019-2020学年高一上学期第三次月考化学试题安徽省合肥一六八中学2019-2020学年高一下学期入学考试化学试题人教版(2019)高一必修第一册第三章 铁 金属材料 第一节 铁及其化合物 易错疑难集训辽宁省大连市金普新区2020-2021学年高一下学期开学检测化学试题(苏教版2019)必修第二册专题9 金属与人类文明 B 素养拓展区安徽省合肥市部分学校2021-2022学年高一上学期期末考试化学试题安徽省合肥市第六中学2021-2022学年高一上学期期末考试化学试题福建省安溪县第一中学2021-2022学年高一下学期第一次月考化学试题吉林省松原市重点高中2021-2022学年高一3月联考化学试题江西省吉安市宁冈中学2020-2021学年高三上学期开学考试化学试题陕西省西安市第八十九中学2022-2023学年高一下学期开学考试化学试题湖南省永州市第一中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
2 . 如图为  在
在 和
和 气氛中的热重曲线(样品质量随温度变化的曲线)。下列有关说法错误的是
气氛中的热重曲线(样品质量随温度变化的曲线)。下列有关说法错误的是
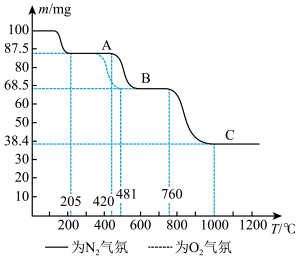
 在
在 和
和 气氛中的热重曲线(样品质量随温度变化的曲线)。下列有关说法错误的是
气氛中的热重曲线(样品质量随温度变化的曲线)。下列有关说法错误的是
A.无论是 气氛还是 气氛还是 气氛,当 气氛,当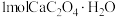 最终转变为 最终转变为 时,转移电子的物质的量相同 时,转移电子的物质的量相同 |
B.无论是 气氛还是 气氛还是 气氛, 气氛, 阶段均发生了氧化还原反应,但两者的气态产物不同 阶段均发生了氧化还原反应,但两者的气态产物不同 |
C.物质 为 为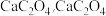 在隔绝空气条件下, 在隔绝空气条件下, 以下热稳定,不会分解 以下热稳定,不会分解 |
D.在酸性 溶液中加入少量 溶液中加入少量 固体样品时,溶液褪色且有少量气泡产生 固体样品时,溶液褪色且有少量气泡产生 |
您最近一年使用:0次
2021-11-24更新
|
739次组卷
|
3卷引用:解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)
(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)重庆市缙云教育联盟2021-2022学年高二11月质量检测化学试题湖南省长沙市第一中学2022-2023学年高三下学期月考(八)化学试题
2021高三·全国·专题练习
3 . 如图是1.00gMgC2O4•nH2O晶体放在坩埚里从25℃徐徐加热至700℃分解时,所得固体产物的质量(m)随温度(t)变化的关系曲线。(已知100℃以上才会逐渐失去结晶水,并约在230℃时完全失去结晶水)
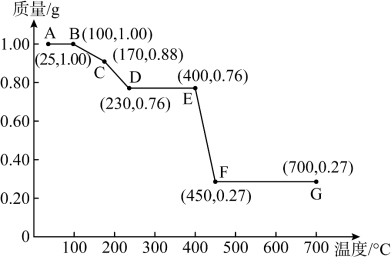
试回答下列问题:
(1)MgC2O4•nH2O中n=___ 。
(2)通过计算确定 C点固体物质的化学式___ (要求写出推断过程);
(3)通过计算确定 从E点到F点过程中的化学方程式___ (要求写出推断过程)。

试回答下列问题:
(1)MgC2O4•nH2O中n=
(2)
(3)
您最近一年使用:0次
4 . 确定Fe2O3和Cu混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别加入30.0 mL某浓度的稀硫酸中,充分反应后, 每组样品剩余固体的质量与原样品质量的关系如图所示。

(1)该混合物中,n(Fe2O3):n(Cu)=___________ 。
(2)稀硫酸的物质的量浓度为___________ 。

(1)该混合物中,n(Fe2O3):n(Cu)=
(2)稀硫酸的物质的量浓度为
您最近一年使用:0次
2021-05-29更新
|
984次组卷
|
5卷引用:考向02 物质的量浓度及其相关计算-备战2022年高考化学一轮复习考点微专题
(已下线)考向02 物质的量浓度及其相关计算-备战2022年高考化学一轮复习考点微专题【省级联考】浙江省2020届普通高校招生选考科目化学模拟试题(六)(已下线)【浙江新东方】【2021.5.19】【SX】【高三下】【高中化学】【SX00147】浙江省宁波市九校2021-2022学年高一上学期期末联考化学试题浙江省舟山市舟山中学2022-2023学年高一上学期12月质量检测化学试题
解题方法
5 . 过氧化钙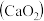 是一种用途广泛的优良供氧剂,常温下为白色固体,能溶于酸,难溶于水、乙醇,且本身无毒,不污染环境,某实验小组制备
是一种用途广泛的优良供氧剂,常温下为白色固体,能溶于酸,难溶于水、乙醇,且本身无毒,不污染环境,某实验小组制备 过程如下。
过程如下。
Ⅰ.制备
利用反应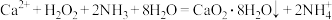 ,在碱性环境下制取
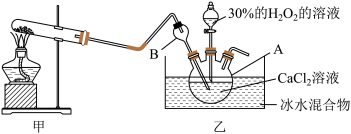
,在碱性环境下制取 的装置如图:
的装置如图:
(1) 的电子式为
的电子式为_______ 。
(2)写出甲装置中反应的化学方程式_______ 。
(3)仪器A的名称为_______ ;仪器B的作用是_______ 。
(4)乙中反应温度需控制在0℃左右的原因是该反应是放热反应,温度低有利于提高 的产率和
的产率和_______ 。
(5)反应结束后,分离提纯 的过程中,洗涤的操作为
的过程中,洗涤的操作为_______ 。
Ⅱ.制得产品并定量检测
(6) 脱水干燥即得
脱水干燥即得 产品。经检测知某
产品。经检测知某 产品中含有
产品中含有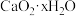 和
和 ,已知
,已知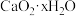 受热分解有
受热分解有 、
、 和
和 生成。①称取
生成。①称取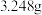 产品,加热,在标准状况下生成
产品,加热,在标准状况下生成 气体。②另取等量产品,溶于适量的稀盐酸后,加入足量的
气体。②另取等量产品,溶于适量的稀盐酸后,加入足量的 溶液得到沉淀
溶液得到沉淀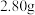 ,则该产品中
,则该产品中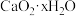 的x值为
的x值为_______ 。
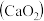 是一种用途广泛的优良供氧剂,常温下为白色固体,能溶于酸,难溶于水、乙醇,且本身无毒,不污染环境,某实验小组制备
是一种用途广泛的优良供氧剂,常温下为白色固体,能溶于酸,难溶于水、乙醇,且本身无毒,不污染环境,某实验小组制备 过程如下。
过程如下。Ⅰ.制备

利用反应
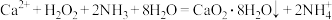 ,在碱性环境下制取
,在碱性环境下制取 的装置如图:
的装置如图:
(1)
 的电子式为
的电子式为(2)写出甲装置中反应的化学方程式
(3)仪器A的名称为
(4)乙中反应温度需控制在0℃左右的原因是该反应是放热反应,温度低有利于提高
 的产率和
的产率和(5)反应结束后,分离提纯
 的过程中,洗涤的操作为
的过程中,洗涤的操作为Ⅱ.制得产品并定量检测
(6)
 脱水干燥即得
脱水干燥即得 产品。经检测知某
产品。经检测知某 产品中含有
产品中含有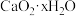 和
和 ,已知
,已知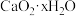 受热分解有
受热分解有 、
、 和
和 生成。①称取
生成。①称取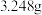 产品,加热,在标准状况下生成
产品,加热,在标准状况下生成 气体。②另取等量产品,溶于适量的稀盐酸后,加入足量的
气体。②另取等量产品,溶于适量的稀盐酸后,加入足量的 溶液得到沉淀
溶液得到沉淀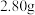 ,则该产品中
,则该产品中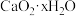 的x值为
的x值为
您最近一年使用:0次
6 . 某小组对固体化合物甲开展探究实验。甲和气体乙以物质的量之比 恰好反应生成固体化合物丙和无色液体丁,甲和丙均由两种元素组成,实验中所加盐酸和NaOH溶液均足量。
恰好反应生成固体化合物丙和无色液体丁,甲和丙均由两种元素组成,实验中所加盐酸和NaOH溶液均足量。
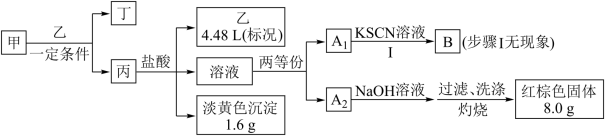
请回答:
(1)组成甲的元素是___________ (填元素符号),甲的化学式是___________ 。
(2)甲与乙反应的化学方程式是___________ 。
(3)丙与盐酸反应的离子方程式是___________ 。
(4)向溶液B中滴加氯水至过量,溶液先变血红色最后褪去。褪色的原因是___________ ,请设计实验方案证明之___________ 。
 恰好反应生成固体化合物丙和无色液体丁,甲和丙均由两种元素组成,实验中所加盐酸和NaOH溶液均足量。
恰好反应生成固体化合物丙和无色液体丁,甲和丙均由两种元素组成,实验中所加盐酸和NaOH溶液均足量。
请回答:
(1)组成甲的元素是
(2)甲与乙反应的化学方程式是
(3)丙与盐酸反应的离子方程式是
(4)向溶液B中滴加氯水至过量,溶液先变血红色最后褪去。褪色的原因是
您最近一年使用:0次
2021高三·全国·专题练习
7 . 按要求解答问题
(1)已知标准状况下,气体A的密度为2.857 g·L-1,则气体A的相对分子质量为_______ ,可能是_______ 气体。
(2)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为_______ 。
(3)CO和CO2的混合气体18 g,完全燃烧后测得CO2体积为11.2 L(标准状况),则
①混合气体在标准状况下的密度是_______ g·L-1。
②混合气体的平均摩尔质量是_______ g·mol-1。
(1)已知标准状况下,气体A的密度为2.857 g·L-1,则气体A的相对分子质量为
(2)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为
(3)CO和CO2的混合气体18 g,完全燃烧后测得CO2体积为11.2 L(标准状况),则
①混合气体在标准状况下的密度是
②混合气体的平均摩尔质量是
您最近一年使用:0次
2021-03-13更新
|
1051次组卷
|
5卷引用:专题02 化学用语及常用物理量——备战2021年高考化学纠错笔记
(已下线)专题02 化学用语及常用物理量——备战2021年高考化学纠错笔记(已下线)专题01 物质的量 气体摩尔体积(热点讲义)-2022届高考化学一轮复习热点题型归纳与变式训练(已下线)第01讲 物质的量 气体摩尔体积(精讲)-2022年一轮复习讲练测(已下线)第01讲 物质的量 气体摩尔体积(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第01讲 物质的量 气体摩尔体积(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
11-12高三上·浙江宁波·阶段练习
名校
解题方法
8 . 将一定质量的镁和铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如下图所示。则下列说法不正确的是:
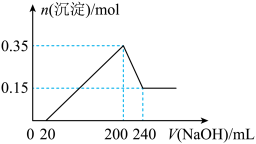
| A.镁和铝的总质量为9 g |
| B.最初20 mLNaOH溶液用于中和过量的硫酸 |
| C.硫酸的物质的量浓度为2.5 mol·L-1 |
| D.生成的氢气在标准状况下的体积为11.2 L |
您最近一年使用:0次
2021-02-05更新
|
1828次组卷
|
34卷引用:专题05 金属及其重要化合物-备战2021届高考化学二轮复习题型专练
(已下线)专题05 金属及其重要化合物-备战2021届高考化学二轮复习题型专练(已下线)微专题02 以物质的量为中心的计算-备战2022年高考化学考点微专题(已下线)周末培优5 物质的量应用于化学方程式的计算专练-2021-2022学年高一化学课后培优练(人教版2019必修第一册)(已下线)易错专题25 物质的量在化学方程式计算中的应用-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)(已下线)2010-2011学年浙江宁海县正学中学高三上学期第一次阶段性测试化学试卷(已下线)2011-2012学年江西省赣州市(十一县市)高三第一学期期中联考化学试卷(已下线)2013-2014云南省玉溪一中高三5月校统测理科综合化学试卷(已下线)2014陕西西安市长安一中高一上学期期末化学(实验班)试卷(已下线)2015届江西省南昌市三校高三10月联考化学试卷2015-2016学年辽宁葫芦岛一中高二上期初考试化学试卷 2016届江西省余江县第一中学高三上学期二次模拟化学试卷2015-2016学年黑龙江省哈尔滨三中高一上期末化学试卷2015-2016学年山西省太原五中高一上学期期末化学试卷2015-2016学年河南省南阳市宛东五校高一下第一次联考化学试卷2015-2016学年黑龙江哈尔滨三中高二下期末化学试卷山东省寿光现代中学2016-2017学年高一下学期第三学段质量监测(期中)化学试题河北省大名县第一中学2018届高三(实验班)上学期第一次月考化学试题安徽省六安市第一中学2017-2018学年高一下学期开学考试化学试题新疆维吾尔自治区阿克苏市高级中学2019届高三上学期第二次月考化学试题黑龙江省双鸭山市第一中学2018-2019学年高二下学期期末考试化学试题黑龙江省双鸭山市第一中学2019-2020学年高一上学期期末考试化学试题安徽省滁州市定远县重点中学2019-2020学年高二下学期期中考试化学试题(已下线)第三章 铁 金属材料(基础过关)-2020-2021学年高一化学单元测试定心卷(人教版2019必修第一册)(已下线)3.1.3 铝与氢氧化钠溶液的反应(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)河南省周口市中英文学校2021届高三上学期期中考试化学试题黑龙江嫩江市高级中学2021届高三上学期第二次月考化学试题(已下线)3.2.2 物质的量在化学方程式计算中的应用(基础练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)江西省南昌市第二中学2020-2021学年高一上学期第三次月考化学试题甘肃省张掖市2020-2021学年高一上学期期末学业水平质量检测化学试题安徽省郎溪中学、泾县中学2020-2021学年高一下学期3月联考化学试题四川省眉山市彭山区第一中学2020-2021学年高一4月月考化学试题山东省新泰市新泰中学2022届高三第一次阶段性考试化学试题江西省丰城市第九中学2021-2022学年高三上学期第二次月考(日新班)化学试题黑龙江省七台河市勃利县高级中学2022-2023学年高三上学期11月期中考试化学试题
解题方法
9 . 试剂级NaCl可用海盐(含泥沙、海藻、K+、 Ca2+、 Mg2+、Fe3+、SO 等杂质)为原料制备。制备流程简图如下:
等杂质)为原料制备。制备流程简图如下:
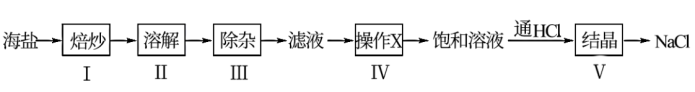
(1)焙炒海盐的目的是______ 。
(2)根据除杂原理,在表中填写除杂时依次添加的试剂及其预期沉淀的离子。
(3)操作X为______ 。
(4)用如图所示装置,以焙炒后的海盐为原料制备HCl气体,并通入NaCl饱和溶液中使NaCl结晶析出。
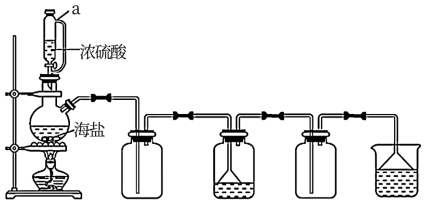
①试剂a为______ 。 相比分液漏斗,选用仪器1的优点是______ 。
②对比实验发现,将烧瓶中的海盐磨细可加快NaCl晶体的析出,其原因是______ 。
(5)已知:CrO + Ba2+ = BaCrO4↓(黄色)
+ Ba2+ = BaCrO4↓(黄色)
CrO +3Fe2++ 8H+ =Cr3+ + 3Fe3++ 4H2O
+3Fe2++ 8H+ =Cr3+ + 3Fe3++ 4H2O
设计如下实验测定NaCl产品中SO 的含量,填写下列表格。
的含量,填写下列表格。
 等杂质)为原料制备。制备流程简图如下:
等杂质)为原料制备。制备流程简图如下:
(1)焙炒海盐的目的是
(2)根据除杂原理,在表中填写除杂时依次添加的试剂及其预期沉淀的离子。
| 实验步骤 | 试剂 | 预期沉淀的离子 |
| 步骤1 | BaCl2溶液 | SO |
| 步骤2 | ||
| 步骤3 |
(4)用如图所示装置,以焙炒后的海盐为原料制备HCl气体,并通入NaCl饱和溶液中使NaCl结晶析出。

①试剂a为
②对比实验发现,将烧瓶中的海盐磨细可加快NaCl晶体的析出,其原因是
(5)已知:CrO
 + Ba2+ = BaCrO4↓(黄色)
+ Ba2+ = BaCrO4↓(黄色)CrO
 +3Fe2++ 8H+ =Cr3+ + 3Fe3++ 4H2O
+3Fe2++ 8H+ =Cr3+ + 3Fe3++ 4H2O设计如下实验测定NaCl产品中SO
 的含量,填写下列表格。
的含量,填写下列表格。| 操作 | 现象 | 目的/结论 | |
| ① | 称取样品m1g,加水溶解,加盐酸调至弱酸性,滴加过量c1mol·L-1BaCl2溶液V1mL | 稍显浑浊 | 目的: |
| ② | 继续滴加过量c2mol ·L-1 K2CrO4溶液V2 mL | 产生黄色沉淀 | 目的:沉淀过量的Ba2+。 |
| ③ | 过滤洗涤,滴加少许指示剂于滤液中,用c3 mol·L-1FeSO4溶液滴定至终点,消耗FeSO4溶液V3 mL | —— | 结论:SO 的质量分数为 的质量分数为 |
您最近一年使用:0次
名校
解题方法
10 . 现有有m g的钠、镁、铝,分别与100mL 1mol/L 的盐酸反应,产生气体在相同条件的体积分别为V1、V2、V3,则V1:V2:V3之比可能是,正确的有几个
① ;②
;②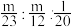 ;③
;③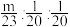 ;④1:1:1;⑤
;④1:1:1;⑤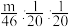
①
 ;②
;②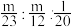 ;③
;③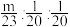 ;④1:1:1;⑤
;④1:1:1;⑤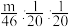
| A.5 | B.4 | C.3 | D.2 |
您最近一年使用:0次



