名校
1 . 设NA为阿伏伽德罗常数的值,下列说法正确的是
| A.100mL 1mol/L NH4Cl溶液中含有阳离子的数目大于0.1NA |
| B.0.1mol的11B中,含有0.6NA个电子 |
| C.25℃时,pH=13的Ba(OH)2溶液中含有氢氧根离子数为0.1NA |
| D.标准状况下,5.6L CO2中含有的共用电子对数为0.5 NA |
您最近一年使用:0次
2 . H2O2在纸张漂白和废水处理等领域有重要应用。一定条件下用H2和O2合成H2O2的反应过程如图所示。设NA为阿伏加德罗常数的值,下列说法正确的是
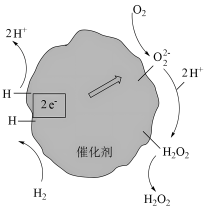

| A.1molH2O2中含2NAσ键,不含π键 |
| B.合成1molH2O2,电子转移数为4NA |
| C.lmol的H2O2含18NA电子 |
| D.标准状况下,4.48LH2O2中含有0.2NAH2O2分子 |
您最近一年使用:0次
3 . 电解重水( )是制取氘气(
)是制取氘气( )的一种方法。设
)的一种方法。设 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是
 )是制取氘气(
)是制取氘气( )的一种方法。设
)的一种方法。设 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是A. 分子间存在氢键 分子间存在氢键 | B. 的熔、沸点比 的熔、沸点比 高 高 |
C.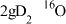 含中子数目为 含中子数目为 | D.制取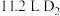 转移的电子数目为 转移的电子数目为 |
您最近一年使用:0次
4 . 反应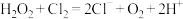 常被用于除去水中残余氯。
常被用于除去水中残余氯。 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
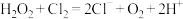 常被用于除去水中残余氯。
常被用于除去水中残余氯。 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.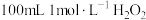 溶液中含有的 溶液中含有的 键数目为 键数目为 |
B.25℃、101kPa时,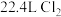 中氯原子的数目为 中氯原子的数目为 |
C.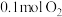 含有质子的数目为 含有质子的数目为 |
D.通过上述反应除去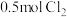 ,电子转移的数目为 ,电子转移的数目为 |
您最近一年使用:0次
5 .  为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.常温常压下, 金刚石含有4NA个共价键 金刚石含有4NA个共价键 |
B. 的乙酸和盐酸混合溶液含0.1NA个 的乙酸和盐酸混合溶液含0.1NA个 |
C.标准状态下,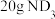 含有的质子数为10NA 含有的质子数为10NA |
D.电解水生成 氢气,外电路通过1NA个电子 氢气,外电路通过1NA个电子 |
您最近一年使用:0次
名校
6 . 火箭表面耐高温涂层的制备反应为 。阿伏伽德罗常数的值为
。阿伏伽德罗常数的值为 ,下列说法正确的是
,下列说法正确的是
 。阿伏伽德罗常数的值为
。阿伏伽德罗常数的值为 ,下列说法正确的是
,下列说法正确的是A. 中共价键的数目为 中共价键的数目为 |
B. 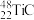 中含有的中子数为 中含有的中子数为 |
C.  固体含有 固体含有 的数目为 的数目为 |
D.消耗 时,该反应中转移的电子数为 时,该反应中转移的电子数为 |
您最近一年使用:0次
2024-01-23更新
|
1139次组卷
|
5卷引用:2024年1月“九省联考”江西卷真题完全解读与考后提升
(已下线)2024年1月“九省联考”江西卷真题完全解读与考后提升(已下线)选择题1-5(已下线)热点04 有关阿伏加德罗常数的正误判断2024年1月江西普通高等学校招生考试适应性测试化学试题辽宁省沈阳市东北育才学校高中部2023-2024学年高三下学期第六次模拟考试化学试题
名校
解题方法
7 . 碱式硫酸镁晶须 是一种无机镁盐晶须,将其添加到以橡胶、塑料为基体的复合材料中,能使该复合材料有良好的阻燃功效。一种以蛇纹石(主要含
是一种无机镁盐晶须,将其添加到以橡胶、塑料为基体的复合材料中,能使该复合材料有良好的阻燃功效。一种以蛇纹石(主要含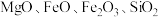 等)为原料制备碱式硫酸镁晶须的流程如图:
等)为原料制备碱式硫酸镁晶须的流程如图:
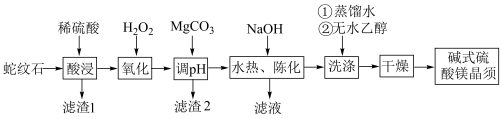
回答下列问题:
(1)酸浸时须将蛇纹石粉碎,其目的是_______ 。
(2)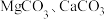 在高温下均易分解,但
在高温下均易分解,但 的分解温度比
的分解温度比 的低,试从结构角度解释其原因:
的低,试从结构角度解释其原因:_______ 。
(3)洗涤步骤中用无水乙醇洗涤的目的是_______ 。
(4)氧化的目的是_______ (用离子方程式表示),为检验溶液中的离子是否完全被氧化,可使用的试剂为_______ (填化学式)。
(5)将碱式硫酸镁晶须 进行热重分析测定其化学式,
进行热重分析测定其化学式,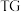 热重曲线[样品的固体残留率(
热重曲线[样品的固体残留率( )随温度变化]
)随温度变化] (微商热重曲线,表示质量的变化速率随温度的变化)如图1所示,第一次失重发生反应的化学方程式为
(微商热重曲线,表示质量的变化速率随温度的变化)如图1所示,第一次失重发生反应的化学方程式为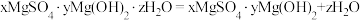 ,第三次失重后获得的晶体的晶胞结构如图2所示。
,第三次失重后获得的晶体的晶胞结构如图2所示。
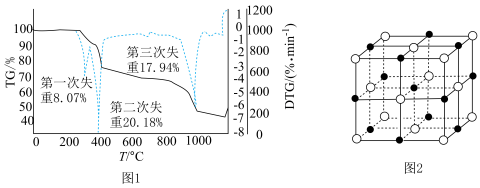
①x、y、z为最简整数比,则碱式硫酸镁晶须的化学式为_______ ;第二次失重发生反应的化学方程式为_______ 。
②图2中的晶胞参数为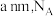 为阿伏加德罗常数的值,则晶胞中白球的配位数为
为阿伏加德罗常数的值,则晶胞中白球的配位数为_______ ,该晶体的密度为_______  。
。
 是一种无机镁盐晶须,将其添加到以橡胶、塑料为基体的复合材料中,能使该复合材料有良好的阻燃功效。一种以蛇纹石(主要含
是一种无机镁盐晶须,将其添加到以橡胶、塑料为基体的复合材料中,能使该复合材料有良好的阻燃功效。一种以蛇纹石(主要含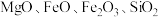 等)为原料制备碱式硫酸镁晶须的流程如图:
等)为原料制备碱式硫酸镁晶须的流程如图:
回答下列问题:
(1)酸浸时须将蛇纹石粉碎,其目的是
(2)
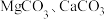 在高温下均易分解,但
在高温下均易分解,但 的分解温度比
的分解温度比 的低,试从结构角度解释其原因:
的低,试从结构角度解释其原因:(3)洗涤步骤中用无水乙醇洗涤的目的是
(4)氧化的目的是
(5)将碱式硫酸镁晶须
 进行热重分析测定其化学式,
进行热重分析测定其化学式, 热重曲线[样品的固体残留率(
热重曲线[样品的固体残留率( )随温度变化]
)随温度变化] (微商热重曲线,表示质量的变化速率随温度的变化)如图1所示,第一次失重发生反应的化学方程式为
(微商热重曲线,表示质量的变化速率随温度的变化)如图1所示,第一次失重发生反应的化学方程式为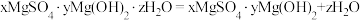 ,第三次失重后获得的晶体的晶胞结构如图2所示。
,第三次失重后获得的晶体的晶胞结构如图2所示。
①x、y、z为最简整数比,则碱式硫酸镁晶须的化学式为
②图2中的晶胞参数为
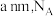 为阿伏加德罗常数的值,则晶胞中白球的配位数为
为阿伏加德罗常数的值,则晶胞中白球的配位数为 。
。
您最近一年使用:0次
2024-01-22更新
|
265次组卷
|
4卷引用:T28-工业流程题
8 . 设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A. 金属钠生成 金属钠生成 ,转移的电子数为 ,转移的电子数为 |
B.标准状况下, 中含 中含 键的数目为 键的数目为 |
C.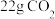 通入水中得到的溶液中含有的 通入水中得到的溶液中含有的 分子数为 分子数为 |
D.由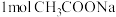 和少量 和少量 形成的中性溶液中, 形成的中性溶液中, 数目小于 数目小于 |
您最近一年使用:0次
2024-01-22更新
|
200次组卷
|
4卷引用:选择题1-5
名校
9 . 火箭推进发生反应的化学方程式为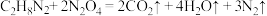 (
(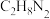 中C、N元素的化合价相等)。下列说法正确的是
中C、N元素的化合价相等)。下列说法正确的是
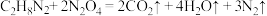 (
(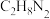 中C、N元素的化合价相等)。下列说法正确的是
中C、N元素的化合价相等)。下列说法正确的是A.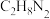 是氧化剂 是氧化剂 | B.氧化产物与还原产物物质的量之比为3∶2 |
C. 被氧化 被氧化 | D. 完全反应,有 完全反应,有 个电子转移 个电子转移 |
您最近一年使用:0次
10 .  2在生活、生产中有重要用途,使用不当会造成环境污染。回答下列问题:
2在生活、生产中有重要用途,使用不当会造成环境污染。回答下列问题:
(1)硫酸亚铁加热至高温会分解,生成三种氧化物。为探究硫酸亚铁的分解产物,将无水硫酸亚铁装入反应管A并连接如图所示的装置,打开 1和
1和 2,缓缓通入
2,缓缓通入 2,加热。实验后反应管A中残留的固体为红色粉末
2,加热。实验后反应管A中残留的固体为红色粉末
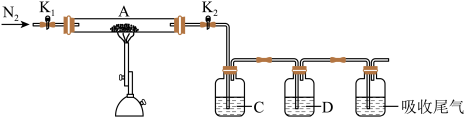
①装置C的溶液为_______ (填标号)。装置D可观察到的实验现象为_______ 。
a.品红 b.NaOH c.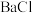 2 d.
2 d. e.浓硫酸
e.浓硫酸
②写出硫酸亚铁高温分解的化学方程式_______ 。
(2)某兴趣小组用如图所示装置模拟测定空气中的二氧化硫的含量。当注入标准状况下VmL空气时,酸性 4溶液恰好褪色,停止实验。
4溶液恰好褪色,停止实验。
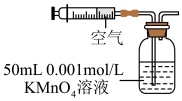
①二氧化硫和酸性 4溶液反应的离子方程式为
4溶液反应的离子方程式为_______ 。
②该空气中二氧化硫的体积分数为_______ (用含Ⅴ的代数式表示)。
(3)某化工厂用如图所示工艺流程除去燃煤产生的 2。
2。

①过程I发生的反应中,氧化剂与还原剂的物质的量之比为_______ 。
②过程Ⅱ发生反应的化学方程式为_______ 。
 2在生活、生产中有重要用途,使用不当会造成环境污染。回答下列问题:
2在生活、生产中有重要用途,使用不当会造成环境污染。回答下列问题:(1)硫酸亚铁加热至高温会分解,生成三种氧化物。为探究硫酸亚铁的分解产物,将无水硫酸亚铁装入反应管A并连接如图所示的装置,打开
 1和
1和 2,缓缓通入
2,缓缓通入 2,加热。实验后反应管A中残留的固体为红色粉末
2,加热。实验后反应管A中残留的固体为红色粉末
①装置C的溶液为
a.品红 b.NaOH c.
 2 d.
2 d. e.浓硫酸
e.浓硫酸②写出硫酸亚铁高温分解的化学方程式
(2)某兴趣小组用如图所示装置模拟测定空气中的二氧化硫的含量。当注入标准状况下VmL空气时,酸性
 4溶液恰好褪色,停止实验。
4溶液恰好褪色,停止实验。
①二氧化硫和酸性
 4溶液反应的离子方程式为
4溶液反应的离子方程式为②该空气中二氧化硫的体积分数为
(3)某化工厂用如图所示工艺流程除去燃煤产生的
 2。
2。
①过程I发生的反应中,氧化剂与还原剂的物质的量之比为
②过程Ⅱ发生反应的化学方程式为
您最近一年使用:0次



