2013·上海闵行·三模
1 . 钠及其化合物在生产和生活中有广泛的应用。例如:Na2O2在医院、潜水、高空飞行中用作供氧剂。
(1)制备Na2O2的反应为:4Na+O2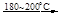 2Na2O 2Na2O +O2
2Na2O 2Na2O +O2 2Na2O2 。
2Na2O2 。
①实验测得某过氧化钠样品含有少量氧化钠杂质,其中钠、氧原子个数比为10︰9.5,该样品中Na2O2的纯度为_________ 。
②取上述过氧化钠样品7.64g放入烧杯中,加入足量水,搅拌,使固体完全溶解,冷却后,在容量瓶中配制成100mL溶液,则该溶液中OH-离子的物质的量浓度为______________ 。
(2)某同学为了检验引起光化学烟雾的气体成分(NO、CO、NO2、HCHO、CH3OH、CH4等),查阅资料得知:Na2O2+2NO→2NaNO2、Na2O2+2NO2→2NaNO3,于是取用a gM气体与b g 氧气混合后,用电火花不断引燃,充分反应后,气体通过足量Na2O2,Na2O2固体质量增加c g。
①若a=c,则M气体的成分可能含有__________________________________ 。
②若2a=c,则M气体可能是什么气体?通过计算回答______ 。
(1)制备Na2O2的反应为:4Na+O2
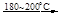 2Na2O 2Na2O +O2
2Na2O 2Na2O +O2 2Na2O2 。
2Na2O2 。①实验测得某过氧化钠样品含有少量氧化钠杂质,其中钠、氧原子个数比为10︰9.5,该样品中Na2O2的纯度为
②取上述过氧化钠样品7.64g放入烧杯中,加入足量水,搅拌,使固体完全溶解,冷却后,在容量瓶中配制成100mL溶液,则该溶液中OH-离子的物质的量浓度为
(2)某同学为了检验引起光化学烟雾的气体成分(NO、CO、NO2、HCHO、CH3OH、CH4等),查阅资料得知:Na2O2+2NO→2NaNO2、Na2O2+2NO2→2NaNO3,于是取用a gM气体与b g 氧气混合后,用电火花不断引燃,充分反应后,气体通过足量Na2O2,Na2O2固体质量增加c g。
①若a=c,则M气体的成分可能含有
②若2a=c,则M气体可能是什么气体?通过计算回答
您最近一年使用:0次
13-14高三上·上海虹口·期末
解题方法
2 . 铁是一种典型的过渡金属,铁和铁的化合物在生产和生活中有广泛的应用。完成下列计算:
(1)将11.802 g钢样粉末(只含铁和碳)于高温下置于足量的纯氧中充分反应,冷却后得到16.240 g磁性氧化铁。
①钢样中含铁________ g。
②生成的CO2在标准状况下体积为________ mL。
(2)向10 mL氯化铁溶液(含盐酸0.001 mol)中加入16.8 g 5%的烧碱溶液(足量),充分反应后过滤。洗涤沉淀,将洗涤液与滤液合并后稀释至250mL。取25mL稀释液,用0.100 mol/L盐酸滴定,终点时消耗盐酸的体积15.50mL。计算原溶液中Fe3+的物质的量浓度_______________ 。
(3)铁锈的主要成分实为羟基氧化铁[化学式FeO(OH)]。将一块带锈铁片放入700mL pH=0的稀硝酸中充分反应,收集到标准状况下NO气体3.584 L,最终剩余2.020g铁。求:
①反应后溶液中溶质的成分与物质的量_____________ 。
②原带锈铁片中铁锈的质量分数_______________ 。
(4)用FeSO4和NaOH制备Fe(OH)2时,往往会形成一种灰绿色的中间物(用X表示)。经分析,X中含有三种阴离子与两种阳离子,阴、阳离子的总质量之比为11:12。已知两种阳离子为Fe2+与Fe3+,物质的量之比为2:1。请通过计算确定X的化学式________________ 。
(1)将11.802 g钢样粉末(只含铁和碳)于高温下置于足量的纯氧中充分反应,冷却后得到16.240 g磁性氧化铁。
①钢样中含铁
②生成的CO2在标准状况下体积为
(2)向10 mL氯化铁溶液(含盐酸0.001 mol)中加入16.8 g 5%的烧碱溶液(足量),充分反应后过滤。洗涤沉淀,将洗涤液与滤液合并后稀释至250mL。取25mL稀释液,用0.100 mol/L盐酸滴定,终点时消耗盐酸的体积15.50mL。计算原溶液中Fe3+的物质的量浓度
(3)铁锈的主要成分实为羟基氧化铁[化学式FeO(OH)]。将一块带锈铁片放入700mL pH=0的稀硝酸中充分反应,收集到标准状况下NO气体3.584 L,最终剩余2.020g铁。求:
①反应后溶液中溶质的成分与物质的量
②原带锈铁片中铁锈的质量分数
(4)用FeSO4和NaOH制备Fe(OH)2时,往往会形成一种灰绿色的中间物(用X表示)。经分析,X中含有三种阴离子与两种阳离子,阴、阳离子的总质量之比为11:12。已知两种阳离子为Fe2+与Fe3+,物质的量之比为2:1。请通过计算确定X的化学式
您最近一年使用:0次
10-11高一上·浙江宁波·期中
3 . 将标准状况下的a升氯化氢气体溶于1000克水中,得到的盐酸的密度为b克/毫升,则该盐酸的物质的量的浓度是
A. | B. | C.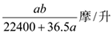 | D. |
您最近一年使用:0次
11-12高三上·江苏泰州·期中
解题方法
4 . 常温下,海水在浓缩过程中析出盐的种类和质量(表中为每升海水析出的各种盐的克数。单位g/L)如下:
海水从密度为1.21 g/mL浓缩到密度为1.22g/mL时发生的变化是:
| 海水密度 (g/mL) | CaSO4 | NaCl | MgCl2 | MgSO4 | NaBr |
| 1.13 | 0.56 | ||||
| 1.20 | 0.91 | ||||
| 1.21 | 0.05 | 3.26 | 0.04 | 0.008 | |
| 1.22 | 0.015 | 9.65 | 0.01 | 0.04 | |
| 1.26 | 0.01 | 2.64 | 0.02 | 0.02 | 0.04 |
| 1.31 | 1.40 | 0.54 | 0.03 | 0.06 |
海水从密度为1.21 g/mL浓缩到密度为1.22g/mL时发生的变化是:
| A.各种盐的溶解度增大 | B.海水中水的质量分数减小 |
| C.析出的粗盐中 NaCl的质量分数增大 | D.海水中Br-浓度不变 |
您最近一年使用:0次
2010·上海浦东新·一模
5 . 烟气中NOx是NO和NO2的混合物(不含N2O4);
(1)根据废气排放标准,1m3烟气最高允许含400mgNOx.若NOx中NO质量分数为0.85,则lm3烟气中最高允许含NO___________ L(标准状况,保留2位小数);
(2)工业上通常用溶质质量分数为0.150的Na2CO3水溶液(密度l.16g/mL)作为NOx吸收剂,该碳酸钠溶液物质的量浓度为_______ mol/L(保留2位小数);
(3)已知:
NO+NO2+Na2CO3→2NaNO2+CO2 ①
2NO2+Na2CO3→NaNO2+NaNO3+CO2 ②
1m3含2000mgNOx的烟气用质量分数为0.150的碳酸钠溶液吸收.若吸收率为80%,吸收后的烟气______ 排放标准(填“符合”或“不符合”),理由:___________ ;
(4)加入硝酸可改变烟气中NO和NO2的比,反应为:NO+2HNO3→3NO2+H2O当烟气中n(NO):n(NO2)=2:3时,吸收率最高;
lm3烟气含2000mgNOx,其中n(NO):n(NO2)=9:1;
计算:
(i)为了达到最高吸收率,1m3烟气需用硝酸的物质的量(保留3位小数)__________ ;
(ii)1m3烟气达到最高吸收率90%时,吸收后生成NaNO2的质量_____________ (假设上述吸收反应中,反应①比反应②迅速.计算结果保留1位小数)。
(1)根据废气排放标准,1m3烟气最高允许含400mgNOx.若NOx中NO质量分数为0.85,则lm3烟气中最高允许含NO
(2)工业上通常用溶质质量分数为0.150的Na2CO3水溶液(密度l.16g/mL)作为NOx吸收剂,该碳酸钠溶液物质的量浓度为
(3)已知:
NO+NO2+Na2CO3→2NaNO2+CO2 ①
2NO2+Na2CO3→NaNO2+NaNO3+CO2 ②
1m3含2000mgNOx的烟气用质量分数为0.150的碳酸钠溶液吸收.若吸收率为80%,吸收后的烟气
(4)加入硝酸可改变烟气中NO和NO2的比,反应为:NO+2HNO3→3NO2+H2O当烟气中n(NO):n(NO2)=2:3时,吸收率最高;
lm3烟气含2000mgNOx,其中n(NO):n(NO2)=9:1;
计算:
(i)为了达到最高吸收率,1m3烟气需用硝酸的物质的量(保留3位小数)
(ii)1m3烟气达到最高吸收率90%时,吸收后生成NaNO2的质量
您最近一年使用:0次
2010·江苏南通·一模
解题方法
6 . 亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:

已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
③160 g/L NaOH溶液是指160 gNaOH固体溶于水所得溶液的体积为1L。
(1)160 g/L NaOH溶液的物质的量浓度为_________ 。若要计算该溶液的质量分数,还需要的一个条件是____________ (用文字说明)。
(2)发生器中鼓入空气的作用可能是__ (选填序号)。
a.将SO2氧化成SO3,增强酸性; b.稀释ClO2以防止爆炸;
c.将NaClO3氧化成ClO2
(3)吸收塔内的反应的离子反应方程式为______________ 。
吸收塔的温度不能超过20℃,其目的是___________________________ 。
(4)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是________________________________ 。
(5)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。除H2O2外,还可以选择的还原剂是_______ (选填序号)。
a.Na2O2b.Na2S c.FeCl2
(6)从滤液中得到NaClO2•3H2O粗晶体的实验操作依次是__ (选填序号)
a.蒸馏 b.蒸发 c.灼烧 d.过滤 e.冷却结晶
要得到更纯的NaClO2•3H2O晶体必须进行的操作是______ (填操作名称)

已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
③160 g/L NaOH溶液是指160 gNaOH固体溶于水所得溶液的体积为1L。
(1)160 g/L NaOH溶液的物质的量浓度为
(2)发生器中鼓入空气的作用可能是
a.将SO2氧化成SO3,增强酸性; b.稀释ClO2以防止爆炸;
c.将NaClO3氧化成ClO2
(3)吸收塔内的反应的离子反应方程式为
吸收塔的温度不能超过20℃,其目的是
(4)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是
(5)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。除H2O2外,还可以选择的还原剂是
a.Na2O2b.Na2S c.FeCl2
(6)从滤液中得到NaClO2•3H2O粗晶体的实验操作依次是
a.蒸馏 b.蒸发 c.灼烧 d.过滤 e.冷却结晶
要得到更纯的NaClO2•3H2O晶体必须进行的操作是
您最近一年使用:0次
2010·江苏扬州·模拟预测
解题方法
7 . 工业上常用废铁屑溶于一定浓度的硫酸溶液制备绿矾( FeSO4·7H2O )。
(1)若用98% 1.84 g/cm3的浓硫酸配制生产用28%的硫酸溶液,则浓硫酸与水的体积比约为1:____ 。
(2)为测定某久置于空气的绿矾样品中Fe2+的氧化率,某同学设计如下实验:取一定量的样品溶于足量的稀硫酸中,然后加入5.00 g铁粉充分反应,收集到224 mL(标准状况)气体,剩余固体质量为3.88 g,测得反应后的溶液中Fe2+的物质的量为0.14 mol(不含Fe3+)。则该样品中Fe2+离子的氧化率为_____ 。
(3)硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O](俗称莫尔盐),较绿矾稳定,在氧化还原滴定分析中常用来配制Fe2+的标准溶液。现取0.4 g Cu2S和CuS的混合物在酸性溶液中用40 mL 0.150 mol/L KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与VmL 0.2 mol/L (NH4)2Fe(SO4)2溶液完全反应。已知:MnO4-+Fe2++H+——Mn2++Fe3++H2O(未配平)
①V的取值范围为______________________ ;
②若V=35,试计算混合物中CuS的质量分数________________
(1)若用98% 1.84 g/cm3的浓硫酸配制生产用28%的硫酸溶液,则浓硫酸与水的体积比约为1:
(2)为测定某久置于空气的绿矾样品中Fe2+的氧化率,某同学设计如下实验:取一定量的样品溶于足量的稀硫酸中,然后加入5.00 g铁粉充分反应,收集到224 mL(标准状况)气体,剩余固体质量为3.88 g,测得反应后的溶液中Fe2+的物质的量为0.14 mol(不含Fe3+)。则该样品中Fe2+离子的氧化率为
(3)硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O](俗称莫尔盐),较绿矾稳定,在氧化还原滴定分析中常用来配制Fe2+的标准溶液。现取0.4 g Cu2S和CuS的混合物在酸性溶液中用40 mL 0.150 mol/L KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与VmL 0.2 mol/L (NH4)2Fe(SO4)2溶液完全反应。已知:MnO4-+Fe2++H+——Mn2++Fe3++H2O(未配平)
①V的取值范围为
②若V=35,试计算混合物中CuS的质量分数
您最近一年使用:0次
2010·上海徐汇·一模
8 . 用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路是成熟的传统工艺,现对某印刷电路生产厂家蚀刻绝缘板后所得的混合溶液(标记为A)进行如下分析:
①取50.0mL A溶液加入足量的硝酸银溶液,析出沉淀86.1g
②取50.0mL A溶液试探性地加入1.12g铁粉,结果全部溶解未见固体析出
③向实验②所得溶液中加入50 mL稀硝酸,产生1.12L NO(标准状况),反应后所得溶液的pH为1。
结合上述信息计算:
(1)所得沉淀的物质的量_____________mol;
(2)该厂所使用的FeCl3溶液的物质的量浓度_____________mol/L;
(3)A溶液中Cu2+的物质的量浓度。
①取50.0mL A溶液加入足量的硝酸银溶液,析出沉淀86.1g
②取50.0mL A溶液试探性地加入1.12g铁粉,结果全部溶解未见固体析出
③向实验②所得溶液中加入50 mL稀硝酸,产生1.12L NO(标准状况),反应后所得溶液的pH为1。
结合上述信息计算:
(1)所得沉淀的物质的量_____________mol;
(2)该厂所使用的FeCl3溶液的物质的量浓度_____________mol/L;
(3)A溶液中Cu2+的物质的量浓度。
您最近一年使用:0次



