名校
1 . 设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.1mol NaOH中含有的阴、阳离子总数是 |
B.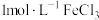 溶液中所含 溶液中所含 的数目为 的数目为 |
C.标准状况下,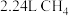 中含有氢原子的数目为 中含有氢原子的数目为 |
D.常温常压下,9.6g由 和 和 组成的混合气体中所含氧原子总数为 组成的混合气体中所含氧原子总数为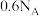 |
您最近一年使用:0次
名校
2 . 实验室需要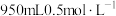 的稀硫酸和
的稀硫酸和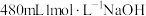 溶液进行实验,请你用98%的浓硫酸(
溶液进行实验,请你用98%的浓硫酸(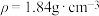 )和NaOH固体进行配制。回答下列问题:
)和NaOH固体进行配制。回答下列问题:
(1)配制稀硫酸时,需要使用的玻璃仪器有量筒、烧杯、胶头滴管、玻璃棒、_______ (填仪器名称)。
(2)配制稀硫酸时,需要量取98%的浓硫酸_______ (精确到0.1)mL。
(3)对所配制的稀硫酸进行测定,发现其浓度为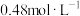 ,下列各项操作可能引起该误差的是
,下列各项操作可能引起该误差的是_______ (填字母)。
A.用量筒量取浓硫酸时仰视
B.转移稀释的硫酸溶液后未洗涤烧杯和玻璃棒
C.浓硫酸稀释后未经冷却即转移到容量瓶中
D.容量瓶未干燥就用来配制溶液
E.定容后摇匀溶液,发现液面低于刻度线,再加入少量蒸馏水使液面与刻度线相平
(4)配制NaOH溶液时,应称量的NaOH固体质量为_______ g。
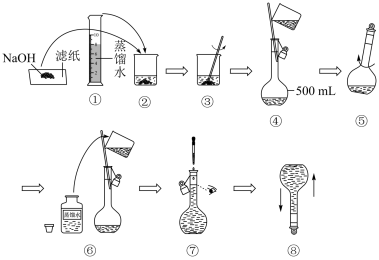
(5)某同学在实验室配制NaOH溶液的过程如图所示,其中有错误的操作是_______ (填序号)。
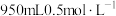 的稀硫酸和
的稀硫酸和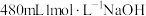 溶液进行实验,请你用98%的浓硫酸(
溶液进行实验,请你用98%的浓硫酸(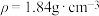 )和NaOH固体进行配制。回答下列问题:
)和NaOH固体进行配制。回答下列问题:(1)配制稀硫酸时,需要使用的玻璃仪器有量筒、烧杯、胶头滴管、玻璃棒、
(2)配制稀硫酸时,需要量取98%的浓硫酸
(3)对所配制的稀硫酸进行测定,发现其浓度为
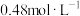 ,下列各项操作可能引起该误差的是
,下列各项操作可能引起该误差的是A.用量筒量取浓硫酸时仰视
B.转移稀释的硫酸溶液后未洗涤烧杯和玻璃棒
C.浓硫酸稀释后未经冷却即转移到容量瓶中
D.容量瓶未干燥就用来配制溶液
E.定容后摇匀溶液,发现液面低于刻度线,再加入少量蒸馏水使液面与刻度线相平
(4)配制NaOH溶液时,应称量的NaOH固体质量为
(5)某同学在实验室配制NaOH溶液的过程如图所示,其中有错误的操作是

您最近一年使用:0次
名校
3 . 某学生需要用烧碱固体配制2.0mol/L的NaOH溶液500mL。实验需要以下仪器:①100mL烧杯②玻璃棒 ③托盘天平(带砝码) ④量筒。
请回答下列问题:
(1)计算结果:需要称取NaOH固体___________ g。
(2)配制时,还需使用的玻璃仪器 为___________ 。
(3)如需配制100mL浓度为0.5mol/LNaOH溶液,需量取___________ mL 2.0mol/L的NaOH溶液稀释。
(4)在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度___________ (“偏大”或“偏小”)。
(5)实验中两次用到玻璃棒,其作用分别是:用于___________ 、用于___________ 。
(6)在容量瓶使用方法中,下列操作不正确的是___________(填序号)
请回答下列问题:
(1)计算结果:需要称取NaOH固体
(2)配制时,还需使用的
(3)如需配制100mL浓度为0.5mol/LNaOH溶液,需量取
(4)在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度
(5)实验中两次用到玻璃棒,其作用分别是:用于
(6)在容量瓶使用方法中,下列操作不正确的是___________(填序号)
| A.使用容量瓶前检查它是否漏水 |
| B.容量瓶用蒸馏水洗净后,未干燥 |
| C.将NaOH固体放在天平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中 |
| D.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀 |
您最近一年使用:0次
解题方法
4 . 现有五种物质:①钠、②新制氯水、③FeCl3、④NaOH、⑤漂白粉,按要求回答下列问题:
(1)上述物质中属于电解质的是_______ (填序号)。
(2)将①长时间放置在潮湿的空气中,最终生成的物质是_______ (填化学式)。
(3)将0.5L 1mol/L③的溶液加水稀释至1L,所得溶液中氯离子的物质的量浓度为_______ mol/L。
(4)实验室制备物质⑤发生反应的化学方程式为_______ 。
(5)实验室欲用固体④配制1.0mol/L的NaOH溶液480mL。
i.配制溶液所需仪器除托盘天平、玻璃棒、烧杯、量筒、胶头滴管外,还需要的玻璃仪器是_______ 。
ii.下列操作会导致所配溶液浓度偏高的是_______ (填字母)。
A.称量所用砝码已生锈
B.溶解、转移溶液后没有洗涤烧杯和玻璃棒
C.定容时俯视
D.定容时,液面超过容量瓶颈上的刻度线,用胶头滴管将过量的液体吸出
(1)上述物质中属于电解质的是
(2)将①长时间放置在潮湿的空气中,最终生成的物质是
(3)将0.5L 1mol/L③的溶液加水稀释至1L,所得溶液中氯离子的物质的量浓度为
(4)实验室制备物质⑤发生反应的化学方程式为
(5)实验室欲用固体④配制1.0mol/L的NaOH溶液480mL。
i.配制溶液所需仪器除托盘天平、玻璃棒、烧杯、量筒、胶头滴管外,还需要的玻璃仪器是
ii.下列操作会导致所配溶液浓度偏高的是
A.称量所用砝码已生锈
B.溶解、转移溶液后没有洗涤烧杯和玻璃棒
C.定容时俯视
D.定容时,液面超过容量瓶颈上的刻度线,用胶头滴管将过量的液体吸出
您最近一年使用:0次
5 . 下列溶液中Cl-浓度由大到小的顺序是
①200 mL2 mol/LMgCl2溶液
②1000 mL2.5 mol/LNaCl溶液
③300 mL5 mol/LKCl溶液
④250 mL1 mol/LFeCl3溶液
①200 mL2 mol/LMgCl2溶液
②1000 mL2.5 mol/LNaCl溶液
③300 mL5 mol/LKCl溶液
④250 mL1 mol/LFeCl3溶液
| A.③①④② | B.④①②③ | C.③②①④ | D.②③①④ |
您最近一年使用:0次
6 . 下列说法中,正确的是
A. 中含有的分子数约为6.02×1023 中含有的分子数约为6.02×1023 |
B. 的体积一定是22.4L 的体积一定是22.4L |
| C.Al的摩尔质量是27g |
D.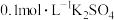 溶液中含有 溶液中含有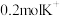 |
您最近一年使用:0次
解题方法
7 . 将一定量Cl2通入NaOH完全吸收,共用去3.00 mol/L的NaOH溶液(密度为1.12 g/mL)80 mL。(反应前后溶液的体积变化忽略不计)请计算:
(1)所用NaOH溶液的质量分数为_______ (保留小数点后两位小数)。
(2)所得溶液中NaCl的物质的量浓度为_______ 。
(3)制取该一定量的Cl2理论上共需MnO2_______ 克。
(1)所用NaOH溶液的质量分数为
(2)所得溶液中NaCl的物质的量浓度为
(3)制取该一定量的Cl2理论上共需MnO2
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
|
解题方法
8 . 实验室需配制450 mL 0.2mol·L−1的NaOH溶液,填空并回答下列问题:
(1)配制450 mL 0.2 mol·L−1的NaOH溶液溶液。
(2)配制时,其正确的操作顺序是_______ (填字母,每个字母只能用一次)。
A.用30 mL水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶,振荡
B.将准确称量的NaOH固体倒入烧杯中,再加适量水溶解
C.将已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.通过玻璃棒继续往容量瓶内小心加水,直到液面接近刻度线下1~2 cm处
上述操作C中,溶液注入容量瓶前需恢复至室温,原因是:_______ 。
(3)在实验中,以下操作造成实验结果偏低的是_______。
(4)若用2.0 mol·L−1的NaOH溶液配制上述溶液,则需要此溶液_______ mL
(1)配制450 mL 0.2 mol·L−1的NaOH溶液溶液。
| 实际应称NaOH质量/g | 应选用容量瓶的规格/mL |
A.用30 mL水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶,振荡
B.将准确称量的NaOH固体倒入烧杯中,再加适量水溶解
C.将已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.通过玻璃棒继续往容量瓶内小心加水,直到液面接近刻度线下1~2 cm处
上述操作C中,溶液注入容量瓶前需恢复至室温,原因是:
(3)在实验中,以下操作造成实验结果偏低的是_______。
| A.在转移溶液时有液体溅到容量瓶外 |
| B.定容时仰视刻度线 |
| C.转移前没有将使用的容量瓶烘干 |
| D.定容摇匀后,发现凹液面低于刻度线,又用胶头滴管加蒸馏水至刻度线 |
您最近一年使用:0次
名校
解题方法
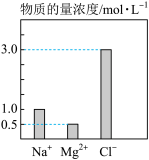
9 . 某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有 、
、 、
、 、
、 、
、 。为了进一步确认,对该溶液进行实验检测:
。为了进一步确认,对该溶液进行实验检测:
步骤一:仔细观察,该溶液呈无色、透明、均一状态:
步骤二:加入足量 溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失。
溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失。
(1)原溶液中除图中的离子外,肯定还含有的离子是_______ ,肯定不含有的离子是_______ 。
(2)步骤二中称量沉淀前的实验操作步骤有:过滤、洗涤、干燥。检验沉淀已洗干净的方法是_______ 。
(3)原溶液中 物质的量浓度为
物质的量浓度为_______ mol/L。
(4)向原溶液中加入 溶液,反应的离子方程式为
溶液,反应的离子方程式为_______ 。
(5)若向100mL原溶液中加入1mol/L的 溶液,当生成的沉淀质量刚好最大时,加入的
溶液,当生成的沉淀质量刚好最大时,加入的 溶液体积为
溶液体积为_______ L。
 、
、 、
、 、
、 、
、 。为了进一步确认,对该溶液进行实验检测:
。为了进一步确认,对该溶液进行实验检测:
步骤一:仔细观察,该溶液呈无色、透明、均一状态:
步骤二:加入足量
 溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失。
溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失。(1)原溶液中除图中的离子外,肯定还含有的离子是
(2)步骤二中称量沉淀前的实验操作步骤有:过滤、洗涤、干燥。检验沉淀已洗干净的方法是
(3)原溶液中
 物质的量浓度为
物质的量浓度为(4)向原溶液中加入
 溶液,反应的离子方程式为
溶液,反应的离子方程式为(5)若向100mL原溶液中加入1mol/L的
 溶液,当生成的沉淀质量刚好最大时,加入的
溶液,当生成的沉淀质量刚好最大时,加入的 溶液体积为
溶液体积为
您最近一年使用:0次
2022-12-28更新
|
250次组卷
|
4卷引用:陕西省渭南市华阴市2021-2022学年高一上学期期末考试化学试题
陕西省渭南市华阴市2021-2022学年高一上学期期末考试化学试题河南省周口中英文学校2019届高三上学期第三次月考化学试题宁夏平罗中学2022-2023学年高二下学期期中考试化学试题(已下线)第11讲 物质的量浓度-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)
名校
解题方法
10 . 将10mL1.0mol/L 溶液加水稀释至100mL,
溶液加水稀释至100mL, 物质的量浓度变为
物质的量浓度变为
 溶液加水稀释至100mL,
溶液加水稀释至100mL, 物质的量浓度变为
物质的量浓度变为| A.0.1mol/L | B.0.2mol/L | C.1.0mol/L | D.0.5mol/L |
您最近一年使用:0次
2022-12-28更新
|
110次组卷
|
10卷引用:陕西省渭南市华阴市2021-2022学年高一上学期期末考试化学试题
陕西省渭南市华阴市2021-2022学年高一上学期期末考试化学试题陕西省汉中市2021-2022学年高一上学期期末校际联考化学试题(已下线)第05讲 物质的量浓度-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)山东省济宁市2019-2020学年高一上学期期末考试化学试题山东省济宁市第二中学2020-2021学年高一上学期第三次阶段检测化学试题浙江省台州市2020-2021学年高一上学期期末质量评估化学试题浙江省台州市2020-2021学年高一上学期期末考试化学试题云南省云天化中学2020-2021学年高一下学期开学考试化学试题(已下线)【浙江新东方】在线化学51高一上(已下线)微专题02 以物质的量为中心的计算-备战2022年高考化学考点微专题



