解题方法
1 . 将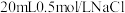 溶液加水稀释到200mL,稀释后溶液中
溶液加水稀释到200mL,稀释后溶液中 的物质的量浓度为
的物质的量浓度为
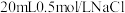 溶液加水稀释到200mL,稀释后溶液中
溶液加水稀释到200mL,稀释后溶液中 的物质的量浓度为
的物质的量浓度为A.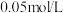 | B. | C.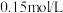 | D.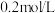 |
您最近一年使用:0次
2022-09-24更新
|
147次组卷
|
2卷引用:陕西省西安市阎良区关山中学2021-2022学年高二下学期第一次质量检测化学(文)试题
解题方法
2 . 将20 mL 0.4 mol·L–1硝酸铵溶液跟50 mL 0.1 mol·L–1氢氧化钡溶液混合,则混合溶液中各离子浓度的大小顺序是
A.[NO ]>[OH-]>[NH ]>[OH-]>[NH ]>[Ba2+] ]>[Ba2+] | B.[NO ]>[Ba2+]>[OH-]>[NH ]>[Ba2+]>[OH-]>[NH ] ] |
C.[Ba2+]>[NO ]>[OH-]>[NH ]>[OH-]>[NH ] ] | D.[NO ]>[Ba2+]>[NH ]>[Ba2+]>[NH ]>[OH-] ]>[OH-] |
您最近一年使用:0次
11-12高三·天津·阶段练习
名校
解题方法
3 . 某硫酸铝和硫酸镁的混合液中,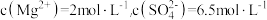 ,若将200mL的此混合液中的
,若将200mL的此混合液中的 和
和 分离,至少应加入1.6mol/L的氢氧化钠溶液
分离,至少应加入1.6mol/L的氢氧化钠溶液
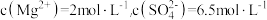 ,若将200mL的此混合液中的
,若将200mL的此混合液中的 和
和 分离,至少应加入1.6mol/L的氢氧化钠溶液
分离,至少应加入1.6mol/L的氢氧化钠溶液| A.0.5L | B.1.5L | C.1.8L | D.2L |
您最近一年使用:0次
2022-09-16更新
|
266次组卷
|
15卷引用:陕西省西安中学 2023 届高三上学期第二次质量检测化学试题
陕西省西安中学 2023 届高三上学期第二次质量检测化学试题(已下线)微专题04 以物质的量为中心的计算-备战2023年高考化学一轮复习考点微专题重庆南开中学2022-2023学年高一上学期期中考试化学试题(已下线)2012届天津市天津一中高三第二次月考化学试卷2016-2017学年辽宁省铁岭市清河高级中学高二下学期第一阶段考试化学试卷天津市杨村第一中学2020届高三上学期第一次月考化学试题(已下线)专题三 化学常用计量与阿伏加德罗常数(提分特训)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训甘肃省天水一中2019-2020学年高一上学期第三学段(期末)考试化学试题江西省宜春市宜丰中学2019-2020高一下学期开学考试化学试题新疆乌鲁木齐市第四中学2019-2020学年高二下学期期末考试化学试题(已下线)第1单元 化学计量在实验中的应用(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷黑龙江省齐齐哈尔市第八中学校2020-2021学年高二下学期6月月考化学试题(已下线)专题一 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)甘肃省礼县第一中学2020-2021学年高一下学期期末测试化学试卷(B)(已下线)微专题 化学计算的思想方法
名校
4 . 下列配制溶液的叙述中错误的是
A.配制 溶液制备 溶液制备 ,需要把蒸馏水煮沸除去氧气后,再溶解配制 ,需要把蒸馏水煮沸除去氧气后,再溶解配制 溶液 溶液 |
| B.容量瓶、滴定管、分液漏斗,使用前均需要检查是否漏液 |
C.配制 溶液时,先把 溶液时,先把 固体溶于浓盐酸然后再加水稀释 固体溶于浓盐酸然后再加水稀释 |
| D.将16g胆矾溶于水配成1L溶液,物质的量浓度为0.1mol/L |
您最近一年使用:0次
2022-09-16更新
|
276次组卷
|
2卷引用:陕西省西安中学 2023 届高三上学期第二次质量检测化学试题
5 . 12月23日凌晨,陕西省西安市下辖村、社区实行封闭式管理,“84消毒液”能有效杀灭新冠肺炎病毒,可用于物品表面的杀菌消毒。小铭同学购买了一瓶“84消毒液”,该消毒液通常稀释到100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如图信息:

(1)该“84消毒液”NaClO物质的量浓度约为____ (保留1位小数)。
(2)工业上可用Cl2与浓氢氧化钠溶液反应制取“84消毒液”,请写出反应的化学方程式____ 。
(3)一瓶上述“84消毒液”理论上能吸收空气中____ L的CO2(标准状况下)而变质。(已知:CO2+NaClO+H2O=NaHCO3+HClO)
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,请用化学方程式解释其原因____ ,某消毒小组人员用18.4mol•L-1的浓硫酸配制500mL2.3mol•L-1的稀硫酸用于增强“84消毒液”的消毒能力,需取用浓硫酸的体积为____ mL。

(1)该“84消毒液”NaClO物质的量浓度约为
(2)工业上可用Cl2与浓氢氧化钠溶液反应制取“84消毒液”,请写出反应的化学方程式
(3)一瓶上述“84消毒液”理论上能吸收空气中
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,请用化学方程式解释其原因
您最近一年使用:0次
2022-09-13更新
|
140次组卷
|
2卷引用:陕西省宝鸡市陈仓区2021-2022学年高一上学期期末考试化学试题
2009·辽宁抚顺·二模
名校
解题方法
6 . 将Cu片放入0.1mol/LFeCl3溶液中,反应一定时间后取出Cu片,溶液中c(Fe3+):c(Fe2+)=2:3,则Cu2+与Fe3+的物质的量之比为
| A.3:2 | B.3:5 | C.4:3 | D.3:4 |
您最近一年使用:0次
2022-09-06更新
|
1649次组卷
|
49卷引用:陕西省咸阳市2022-2023学年高一上学期期末考试化学试题
陕西省咸阳市2022-2023学年高一上学期期末考试化学试题(已下线)2012-2013学年陕西省西安市高陵县第三中学高一第三次月考化学试卷陕西省汉中市汉中中学2019届高三上学期第二次月考化学试题甘肃省武威第七中学2022-2023学年高三上学期第一次质量检测化学试题(已下线)3.2.2物质的量在化学方程式中的计算-同步学习必备知识辽宁省铁岭市昌图县第一高级中学2022-2023学年高一上学期12月化学试题(已下线)辽宁省抚顺市六校联合体2009—2010学年度高三二模(理综)试题化学部分(已下线)2010年杭州市西湖高级中学高三上学期开学考试化学试题(已下线)2011-2012学年广东省中山市高一上学期期末统一考试化学试卷(已下线)2011-2012学年黑龙江哈六中高一上学期期末考试化学试卷(已下线)2013届山西省长治二中高三上学期第一次练考化学试卷(已下线)2013届福建安溪一中、养正中学高三上学期期中联考化学试卷(已下线)2012-2013学年吉林省长春二中高一上学期期末考试化学试卷(已下线)2012-2013学年广东省深圳科学高中高一第一学期期末考试化学试卷B(已下线)2013-2014学年河北冀州中学高一上学期第四次月考化学试卷2015-2016学年湖北省汉川市高一上学期期末考试化学试卷2015-2016学年黑龙江省海林林业局一中高一上学期期末化学试卷2016-2017学年河北省张家口第一中学高一(普通班、实验班)下学期开学检测化学试卷河北省辛集中学2017-2018学年高一上学期12月月考化学试题宁夏银川一中2017-2018学年高一上学期期末考试化学试题黑龙江省伊春中学2017-2018学年高一化学上学期期末考试题北京四中2017-2018学年高一上学期期末考试化学试题【全国百强校】浙江省嘉兴市第一中学2017-2018学年高一下学期期中考试化学试题【全国百强校】河北省石家庄市辛集中学2018-2019学年高一上学期第二次月考化学试题湖南省双峰县第七中学2018-2019学年高一第一学期第三次月考化学试题吉林省扶余市第一中学2018-2019学年高一上学期期末考试化学试题宁夏回族自治区青铜峡市高级中学2018-2019学年高一上学期期末考试化学试题【全国百强校】北京市第四中学2018-2019学年高一上学期期末考试化学试题【全国百强校】河北省张家口市第一中学2018-2019学年高一下学期开学考试化学试题江西省南城县第二中学2018-2019学年高一12月月考化学试题黑龙江省安达市第七中学2019-2020学年高一上学期月考化学试题鲁教版高中化学必修1第四章《材料家族中的元素》测试卷2(已下线)【新东方】2020-80.湖北省武汉外国语学校2019-2020学年高一上学期期末考试化学试题人教版(2019)高一必修第一册第三章 铁 金属材料 第一节 铁及其化合物 课时2 铁盐、亚铁盐鲁科版(2019)高一必修第一册第三章第1节 铁的多样性 课时2 铁及其化合物之间的转化关系高一必修第一册(鲁科2019)第3章 第1节 铁的多样性 教材帮河南省长葛市第一高级中学2020-2021学年高一上学期阶段性测试试卷化学试题(已下线)第三章 金属及其化合物(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版必修1)(已下线)3.2.3 铁的重要化合物(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)河南省豫西名校2020-2021学年高一上学期第二次联考化学试题四川宜宾屏山县中学校2020-2021学年高一下学期第一次月考化学试题河北省石家庄二中2019-2020学年高一上学期期末考试化学试题河北省邯郸市大名县第一中学2020-2021学年高一下学期5月月考化学试题(已下线)微专题13 亚铁离子、三价铁离子的性质及检验-备战2022年高考化学考点微专题上海市杨浦高级中学2020-2021学年高二上学期第一次月考化学试题甘肃天祝藏族自治县第一中学2022-2023学年高一上学期期末考试化学试题湖南省邵阳市第二中学2023-2024学年高二上学期基础知识竞赛化学试题山东省聊城市临清市第一中学2023-2024学年高一上学期期末模拟考试化学试题
名校
7 . 某实验小组用0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液进行中和热的测定。
I.配制0.50 mol·L-1 NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体_______ g。
(2)从下图中选择称量NaOH固体所需要的仪器是_______ (填字母)。
II.50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
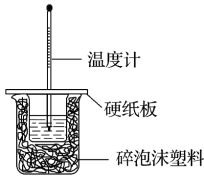
(3)从实验装置上看,图中尚缺少的一种玻璃用品是_______ 。
(4)烧杯间填满碎纸条的作用是_______ 。
(5)大烧杯上如不盖硬纸板,求得的中和热数值_______ (填“偏大”、“偏小”或“无影响”)。
(6)实验中60 mL0.50 mol/L盐酸与50 mL0.55 mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量_______ (填“相等”或“不相等”),所求中和热_______ (填“相等”或“不相等”),简述理由:_______ 。
(7)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:
②近似认为0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18 J·g-1·℃-1。测的中和热ΔH=_______ kJ·mol-1 (取小数点后一位)。
③上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是_______ (填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
I.配制0.50 mol·L-1 NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体
(2)从下图中选择称量NaOH固体所需要的仪器是
| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
II.50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(3)从实验装置上看,图中尚缺少的一种玻璃用品是
(4)烧杯间填满碎纸条的作用是
(5)大烧杯上如不盖硬纸板,求得的中和热数值
(6)实验中60 mL0.50 mol/L盐酸与50 mL0.55 mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量
(7)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:
| 温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 31.2 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
③上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
您最近一年使用:0次
名校
8 . 下列各溶液所指出的某种微粒数目与阿伏加德罗常数的值相等的是
| A.1LCaCl2溶液中的Ca2+ | B.1mol·L-1CaCl2溶液中的Ca2+ |
| C.0.5L1mol·L-1CaCl2溶液中的Cl- | D.1L0.5mol·L-1CaCl2溶液中的Ca2+ |
您最近一年使用:0次
名校
9 . 如果1 L硫酸溶液中含有6.02×1023个H+,则该硫酸的浓度是
| A.2 mol·L-1 | B.1.5 mol·L-1 | C.1 mol·L-1 | D.0.5 mol·L-1 |
您最近一年使用:0次
名校
解题方法
10 . 称取一定质量镁铝合金放入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图(生成沉淀阶段的图象斜率视为恒定)。
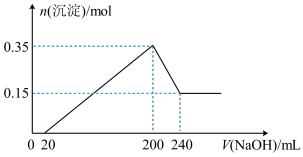
计算:
(1)合金中Al的质量为多少____ ?
(2)所加NaOH溶液的物质的量浓度为多少____ ?

计算:
(1)合金中Al的质量为多少
(2)所加NaOH溶液的物质的量浓度为多少
您最近一年使用:0次



