解题方法
1 . 完成下列小题
(1)现有下列七种物质:① 固体②
固体② ③氯化铁溶液④
③氯化铁溶液④ 固体⑤稀硫酸⑥熔融
固体⑤稀硫酸⑥熔融 ⑦
⑦ 在上述物质中,能导电的是
在上述物质中,能导电的是___________ ;属于电解质的是___________ 。
(2)写出铁在氯气中燃烧的化学方程式___________ 。
(3)质量为 的
的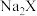 中含有
中含有 的物质的量为
的物质的量为 ,则X的摩尔质量为
,则X的摩尔质量为___________ 。
(1)现有下列七种物质:①
 固体②
固体② ③氯化铁溶液④
③氯化铁溶液④ 固体⑤稀硫酸⑥熔融
固体⑤稀硫酸⑥熔融 ⑦
⑦ 在上述物质中,能导电的是
在上述物质中,能导电的是(2)写出铁在氯气中燃烧的化学方程式
(3)质量为
 的
的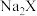 中含有
中含有 的物质的量为
的物质的量为 ,则X的摩尔质量为
,则X的摩尔质量为
您最近一年使用:0次
2 . 完成下列问题。
(1)0.01mol某气体的质量为0.28g,该气体的摩尔质量为_______ 。
(2)下列常见的物质中a. ;b.熔融
;b.熔融 ;c.
;c. 溶液;d.
溶液;d. ;e.
;e. ;f.酒精;属于电解质且能导电的是
;f.酒精;属于电解质且能导电的是______ (填标号)。
(3)向硫酸亚铁溶液中滴入 溶液,①产生的现象是
溶液,①产生的现象是________ ,②其中发生氧化还原反应的化学方程式为:___________ 。
(4)已知 能发生反应:
能发生反应: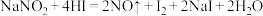 ,用单线桥法表示该反应中电子转移情况
,用单线桥法表示该反应中电子转移情况___________ 。
(1)0.01mol某气体的质量为0.28g,该气体的摩尔质量为
(2)下列常见的物质中a.
 ;b.熔融
;b.熔融 ;c.
;c. 溶液;d.
溶液;d. ;e.
;e. ;f.酒精;属于电解质且能导电的是
;f.酒精;属于电解质且能导电的是(3)向硫酸亚铁溶液中滴入
 溶液,①产生的现象是
溶液,①产生的现象是(4)已知
 能发生反应:
能发生反应: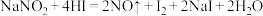 ,用单线桥法表示该反应中电子转移情况
,用单线桥法表示该反应中电子转移情况
您最近一年使用:0次
名校
3 . 定量研究是社会科学领域的一种基本研究范式,也是科学研究的重要步骤和方法之一。 物质是由数目巨大、质量很小、肉眼无法观察到的分子、原子等微粒构成,物质的量可以用于计量这些微粒的数量,它的出现建立起了微粒数与宏观可称量的物质物理量之间的联系。结合定量分析我们可以从微观视角探析物质组成、结构……。
(1)用 表示阿伏加德罗常数,下列说法正确的是_______。
表示阿伏加德罗常数,下列说法正确的是_______。
(2)下列物质中含分子数最多的是_______。
(3)下列有关气体摩尔体积的说法中正确的是_______。
(4)阅读下表后完成以下问题:
①计算, “鲜花保鲜剂”中含
“鲜花保鲜剂”中含___________ 个 ,硫酸钾溶液浓度为
,硫酸钾溶液浓度为___________ 。
②“鲜花保鲜剂”中 的结构示意图为
的结构示意图为___________ ,鉴别含有 的实验方法为
的实验方法为___________ 。
A.显色法 B.沉淀法 C.气体法 D.焰色反应
(1)用
 表示阿伏加德罗常数,下列说法正确的是_______。
表示阿伏加德罗常数,下列说法正确的是_______。| A.摩尔是一个基本物理量 |
B.含有 个氢原子的水,其物质的量为 个氢原子的水,其物质的量为 |
C. 氧气所含氧原子为 氧气所含氧原子为 |
D. 中含原子数 中含原子数 |
A.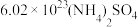 分子 分子 | B.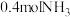 |
C. 氖气 氖气 | D.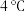 时 时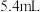 水 水 |
A.气体的摩尔体积为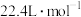 |
B. 2的质量是 2的质量是 ,它所占的体积是 ,它所占的体积是 |
C.在标准状况下, 酒精的物质的量为 酒精的物质的量为 |
D.在标准状况下, 空气的体积约为 空气的体积约为 |
成分( 溶液) 溶液) | 蔗糖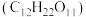 | 硫酸钾 | 阿司匹林 | 高锰酸钾 | 硝酸银 |
| 质量(g) | 25.000 | 0.870 | 0.180 | 0.316 | 0.075 |
 “鲜花保鲜剂”中含
“鲜花保鲜剂”中含 ,硫酸钾溶液浓度为
,硫酸钾溶液浓度为②“鲜花保鲜剂”中
 的结构示意图为
的结构示意图为 的实验方法为
的实验方法为A.显色法 B.沉淀法 C.气体法 D.焰色反应
您最近一年使用:0次
解题方法
4 . 回答下列问题:
(1)等质量的O2、CH4、H2的物质的量之比为_______ 。
(2)44.4g某二价金属氯化物(ACl2)中含有0.8molCl-,则ACl2的摩尔质量是_______ ;A的相对原子质量是_______ ;ACl2的化学式是_______ 。
(3)下列两组物质:①CO2、P2O5、CaO、SO2,②Cu、Mg、Zn、Al。每组中有一种物质在某些化学性质或分类上与其他几种物质不同,这两种物质是①_______ ,②_______ 。
(1)等质量的O2、CH4、H2的物质的量之比为
(2)44.4g某二价金属氯化物(ACl2)中含有0.8molCl-,则ACl2的摩尔质量是
(3)下列两组物质:①CO2、P2O5、CaO、SO2,②Cu、Mg、Zn、Al。每组中有一种物质在某些化学性质或分类上与其他几种物质不同,这两种物质是①
您最近一年使用:0次
2024高三·全国·专题练习
5 . NA为阿伏加德罗常数的值。下列说法正确的是_______ 。
A.(2023·全国卷)标准状况下,2.24LSO3中电子的数目为4.00NA
B.(2023·广东卷)NaCl和NH4Cl的混合物中含1molCl-,则混合物中质子数为28NA
C.(2022·辽宁卷)1.8g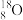 中含有的中子数为NA
中含有的中子数为NA
D.(2022·浙江6月)8g CH4含有中子数为3NA
E.(2022·海南卷)2.8g56Fe含有的中子数为1.3NA
F.(2021·天津卷)180g葡萄糖中,C原子的数目为6NA
G.(2021·广东卷)23gNa与足量H2O反应生成的H2分子数目为NA
H.(2021·河北卷)22.4L(标准状况)氟气所含的质子数为18NA
I.(2021·湖北卷)23gCH3CH2OH中sp3杂化的原子数为NA
J.(2021·湖北卷)0.5molXeF4中氙的价层电子对数为3NA
K.(2021·湖南卷)18gH218O含有的中子数为10NA
L.(2021·海南卷)0.1mol 27Al3+中含有的电子数为1.3NA
M.(2021·海南卷)0.1mol肼(H2N-NH2)含有的孤电子对数为0.2NA
N.(2021·全国甲卷)18g重水(D2O)中含有的质子数为10NA
A.(2023·全国卷)标准状况下,2.24LSO3中电子的数目为4.00NA
B.(2023·广东卷)NaCl和NH4Cl的混合物中含1molCl-,则混合物中质子数为28NA
C.(2022·辽宁卷)1.8g
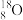 中含有的中子数为NA
中含有的中子数为NAD.(2022·浙江6月)8g CH4含有中子数为3NA
E.(2022·海南卷)2.8g56Fe含有的中子数为1.3NA
F.(2021·天津卷)180g葡萄糖中,C原子的数目为6NA
G.(2021·广东卷)23gNa与足量H2O反应生成的H2分子数目为NA
H.(2021·河北卷)22.4L(标准状况)氟气所含的质子数为18NA
I.(2021·湖北卷)23gCH3CH2OH中sp3杂化的原子数为NA
J.(2021·湖北卷)0.5molXeF4中氙的价层电子对数为3NA
K.(2021·湖南卷)18gH218O含有的中子数为10NA
L.(2021·海南卷)0.1mol 27Al3+中含有的电子数为1.3NA
M.(2021·海南卷)0.1mol肼(H2N-NH2)含有的孤电子对数为0.2NA
N.(2021·全国甲卷)18g重水(D2O)中含有的质子数为10NA
您最近一年使用:0次
名校
解题方法
6 . 计算。
(1) 个
个 的物质的量为
的物质的量为___________  ,所含原子的物质的量为
,所含原子的物质的量为___________  ,所含电子的物质的量为
,所含电子的物质的量为___________  。
。
(2)等质量的 和
和 物质的量之比是
物质的量之比是___________ ,氧原子数之比为___________ 。
(3)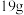 某二价金属的氯化物
某二价金属的氯化物 中含有
中含有 ,则A的摩尔质量为
,则A的摩尔质量为___________ 。
(4)将 的
的 溶液由
溶液由 稀释至
稀释至 ,稀释后溶液中
,稀释后溶液中 的物质的量浓度是
的物质的量浓度是___________  (用含a、b的代数式表示)。
(用含a、b的代数式表示)。
(5)我国科学家研发了一种室温下“可呼吸”的 充电电池。电池的总反应为:
充电电池。电池的总反应为: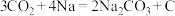 。该电池消耗
。该电池消耗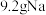 时,可以消耗标准状况下二氧化碳的体积是
时,可以消耗标准状况下二氧化碳的体积是___________ L。
(1)
 个
个 的物质的量为
的物质的量为 ,所含原子的物质的量为
,所含原子的物质的量为 ,所含电子的物质的量为
,所含电子的物质的量为 。
。(2)等质量的
 和
和 物质的量之比是
物质的量之比是(3)
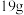 某二价金属的氯化物
某二价金属的氯化物 中含有
中含有 ,则A的摩尔质量为
,则A的摩尔质量为(4)将
 的
的 溶液由
溶液由 稀释至
稀释至 ,稀释后溶液中
,稀释后溶液中 的物质的量浓度是
的物质的量浓度是 (用含a、b的代数式表示)。
(用含a、b的代数式表示)。(5)我国科学家研发了一种室温下“可呼吸”的
 充电电池。电池的总反应为:
充电电池。电池的总反应为: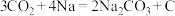 。该电池消耗
。该电池消耗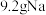 时,可以消耗标准状况下二氧化碳的体积是
时,可以消耗标准状况下二氧化碳的体积是
您最近一年使用:0次
2023-12-12更新
|
160次组卷
|
2卷引用:新疆乌鲁木齐八一中学2023-2024学年高一上学期1月月考化学试卷
24-25高一上·全国·假期作业
7 . 一块表面已经被部分氧化成氧化钠的钠块,质量为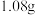 ,投入到
,投入到 水中,完全反应后收集到
水中,完全反应后收集到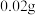 氢气。通过计算回答:
氢气。通过计算回答:
(1)未被氧化的钠的质量是___________ 。
(2)钠块表面被氧化的钠的质量是___________ 。
(3)①若将氧化钠投入紫色石蕊试液中,现象为___________ 。
②若将过氧化钠投入紫色石蕊试液中,现象为___________ 。
(4)若向饱和烧碱溶液中加入一定量过氧化钠,则
___________ (填“变大”“变小”或“不变”,下同),
___________ 。
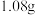 ,投入到
,投入到 水中,完全反应后收集到
水中,完全反应后收集到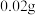 氢气。通过计算回答:
氢气。通过计算回答:(1)未被氧化的钠的质量是
(2)钠块表面被氧化的钠的质量是
(3)①若将氧化钠投入紫色石蕊试液中,现象为
②若将过氧化钠投入紫色石蕊试液中,现象为
(4)若向饱和烧碱溶液中加入一定量过氧化钠,则


您最近一年使用:0次
名校
8 . 利用所学知识进行填空(用NA表示阿伏加德罗常数的值)。
(1)0.4mol氨气中含有NH3分子数是___________ ,其质量是___________ g。
(2)标准状况下,44.8LCH4对应的物质的量是___________ ,其电子数为___________ 。
(3)现有物质:①NaOH溶液;②铜;③熔融KHSO4;④BaCO3固体;⑤液态HCl;⑥CO2,以上物质中属于混合物的是___________  填序号
填序号 ,以上物质中属于电解质的
,以上物质中属于电解质的___________  填序号
填序号 ;以上物质中能导电的是
;以上物质中能导电的是___________  填序号
填序号 。
。
(4)现有CO与O2两种气态物质,试回答下列问题:
①同温同压下,CO与O2的密度之比为___________ 。
②相同温度和压强下,等质量的CO和O2.二者体积比为___________ 。
(5)将4gNaOH溶于水配成1L溶液,然后取出10mL,这10mL溶液的物质的量浓度为___________ 。
(6)18.6gNa2X含有0.6molNa+,则Na2X的物质的量是___________ ,Na2X的摩尔质量是___________ 。
(7)已知O2和CO2的混合气体,在标准状况下体积为11.2L,质量为18g,则混合气体的平均相对分子质量是___________ ,混合气体中O2和CO2物质的量之比为___________ 。
(1)0.4mol氨气中含有NH3分子数是
(2)标准状况下,44.8LCH4对应的物质的量是
(3)现有物质:①NaOH溶液;②铜;③熔融KHSO4;④BaCO3固体;⑤液态HCl;⑥CO2,以上物质中属于混合物的是
 填序号
填序号 ,以上物质中属于电解质的
,以上物质中属于电解质的 填序号
填序号 ;以上物质中能导电的是
;以上物质中能导电的是 填序号
填序号 。
。(4)现有CO与O2两种气态物质,试回答下列问题:
①同温同压下,CO与O2的密度之比为
②相同温度和压强下,等质量的CO和O2.二者体积比为
(5)将4gNaOH溶于水配成1L溶液,然后取出10mL,这10mL溶液的物质的量浓度为
(6)18.6gNa2X含有0.6molNa+,则Na2X的物质的量是
(7)已知O2和CO2的混合气体,在标准状况下体积为11.2L,质量为18g,则混合气体的平均相对分子质量是
您最近一年使用:0次
名校
9 . 化学计量在化学中占有重要地位。请回答下列问题:
(1)22.2g某二价金属氯化物(ACl2)中含有0.4molCl-,则ACl2的摩尔质量是_______ ;
(2)已知 受热分解产生
受热分解产生 和
和 ,且常温常压下气体摩尔体积为
,且常温常压下气体摩尔体积为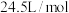 ,则在常温常压下,
,则在常温常压下,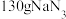 发生分解反应能产生
发生分解反应能产生_______  的
的 。
。
(1)22.2g某二价金属氯化物(ACl2)中含有0.4molCl-,则ACl2的摩尔质量是
(2)已知
 受热分解产生
受热分解产生 和
和 ,且常温常压下气体摩尔体积为
,且常温常压下气体摩尔体积为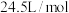 ,则在常温常压下,
,则在常温常压下,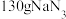 发生分解反应能产生
发生分解反应能产生 的
的 。
。
您最近一年使用:0次
2023-11-23更新
|
125次组卷
|
3卷引用:河南省新乡市原阳县第一高级中学2023-2024学年高一上学期1月月考化学试题
10 . 完成下列问题。
(1)在 的反应中,该反应中
的反应中,该反应中 体现的性质是
体现的性质是___________ 。若反应生成标准状况下11.2L NO,则被还原的 为
为___________ mol,转移电子为___________ mol。
(2)若 为阿伏伽德罗常数,3.4g氨气中所含氢原子数为
为阿伏伽德罗常数,3.4g氨气中所含氢原子数为___________ ,所含质子数为___________ 。
(3)同温同压下,相同体积的氢气和气体A的质量分别是0.2g和2.8g,则气体A的摩尔质量为___________ ,该气体可能是___________ (写化学式)。
(1)在
 的反应中,该反应中
的反应中,该反应中 体现的性质是
体现的性质是 为
为(2)若
 为阿伏伽德罗常数,3.4g氨气中所含氢原子数为
为阿伏伽德罗常数,3.4g氨气中所含氢原子数为(3)同温同压下,相同体积的氢气和气体A的质量分别是0.2g和2.8g,则气体A的摩尔质量为
您最近一年使用:0次
2023-08-28更新
|
125次组卷
|
2卷引用:河北省沧州市盐山中学2023-2024学年高一下学期开学化学试题



