名校
1 . 在两个密闭容器中,分别充有质量相等的甲、乙两种气体,它们的温度和密度均相同。试根据甲、乙的摩尔质量(M)的关系,判断下列说法中正确的是
| A.若M(甲)>M(乙),则分子数:甲>乙 |
| B.若M(甲)<M(乙),则气体摩尔体积:甲>乙 |
| C.若M(甲)<M(乙),则气体的压强:甲>乙 |
| D.若M(甲)>M(乙),则气体体积:甲<乙 |
您最近一年使用:0次
2024-02-01更新
|
149次组卷
|
3卷引用:江西省新余市第一中学2023-2024学年高一下学期开学考试化学试卷
江西省新余市第一中学2023-2024学年高一下学期开学考试化学试卷 海南省农垦中学2023-2024学年高三上学期期末考试化学试题(A卷)(已下线)第01讲 物质的量 气体摩尔体积(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
2 . 用 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A. 的 的 溶液中 溶液中 数目为 数目为 |
B.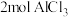 完全与水反应生成的 完全与水反应生成的 胶体粒子数目为 胶体粒子数目为 |
C.由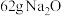 与 与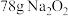 组成的混合物中阴离子总数为 组成的混合物中阴离子总数为 |
D.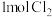 与足量Fe充分反应,转移 与足量Fe充分反应,转移 个电子 个电子 |
您最近一年使用:0次
2024-01-25更新
|
106次组卷
|
3卷引用:吉林省通化市梅河口市第五中学2023-2024学年高一下学期开学化学试题
3 . NA为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,11.2LCO2中含有原子的数目为 |
B.等体积、等物质的量浓度的NaCl和KCl溶液中,阴、阳离子数目之和均为 |
| C.71gCl2与足量的铁完全反应生成FeCl3时,反应转移的电子数为2NA |
| D.常温常压下,48gO2和O3的混合气体含有的氧原子数大于1.5NA小于3NA |
您最近一年使用:0次
2024-01-18更新
|
241次组卷
|
4卷引用:河南省信阳高级中学2023-2024学年高一下学期开学化学试题
名校
解题方法
4 . 下列各物质所含原子数按由多到少的顺序排列的是
①1.0 mol ②8 g He ③4℃时18 g
②8 g He ③4℃时18 g  ④0.4 mol
④0.4 mol 
①1.0 mol
 ②8 g He ③4℃时18 g
②8 g He ③4℃时18 g  ④0.4 mol
④0.4 mol 
| A.①④③② | B.④③②① | C.②③④① | D.①④②③ |
您最近一年使用:0次
2024-01-13更新
|
121次组卷
|
3卷引用: 河北郑口中学2023-2024学年高一下学期2月 作业检测考试 化学试题
名校
解题方法
5 . “侯氏制碱法”是我国化工专家侯德榜为世界制碱工业作出的突出贡献。某实验小组模拟“侯氏制碱法”的工艺流程如下:
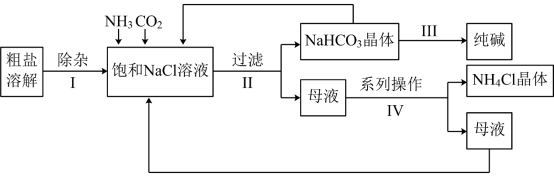
(1)粗盐的溶液中含有 Ca2+、Mg2+、和 ,除杂时可先后依次加入的试剂有BaCl2、NaOH、
,除杂时可先后依次加入的试剂有BaCl2、NaOH、___________ (填化学式)。
(2)系列操作Ⅳ包括:通入NH3、加入NaCl 固体、降温结晶、___________ 得到NH4Cl 晶体。
(3)生成NaHCO3晶体的化学方程式为___________ 。
(4)流程中可循环使用的物质有___________ (填化学式)。
(5)纯碱中可能混有NaHCO3杂质,称取29.6g产品溶于水中,滴加足量Ba(OH)2溶液,过滤,洗涤沉淀。
①将所得沉淀充分干燥,称量,沉淀的质量为59.1g。则产品中Na2CO3的质量分数w(Na2CO3)=___________ (保留三位有效数字)。如果此步骤中,沉淀未干燥充分就称量,则测得w(Na2CO3)___________ (填“偏大” “偏小”或“无影响”)。

(1)粗盐的溶液中含有 Ca2+、Mg2+、和
 ,除杂时可先后依次加入的试剂有BaCl2、NaOH、
,除杂时可先后依次加入的试剂有BaCl2、NaOH、(2)系列操作Ⅳ包括:通入NH3、加入NaCl 固体、降温结晶、
(3)生成NaHCO3晶体的化学方程式为
(4)流程中可循环使用的物质有
(5)纯碱中可能混有NaHCO3杂质,称取29.6g产品溶于水中,滴加足量Ba(OH)2溶液,过滤,洗涤沉淀。
①将所得沉淀充分干燥,称量,沉淀的质量为59.1g。则产品中Na2CO3的质量分数w(Na2CO3)=
您最近一年使用:0次
2024-01-09更新
|
152次组卷
|
4卷引用:四川省泸州市泸县第五中学2023-2024学年高一下学期开学化学试题
名校
6 . 已知R2-核内共有N个中子,R的质量数为A,则mgR2-中含有电子的物质的量为
A. | B.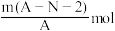 |
C. | D. |
您最近一年使用:0次
2024-01-06更新
|
187次组卷
|
23卷引用:云南省腾冲市第八中学2023-2024学年高一下学期开学化学试题
云南省腾冲市第八中学2023-2024学年高一下学期开学化学试题浙江省宁波市北仑中学2022-2023学年高一下学期期初返校考试(选考)化学试题新疆塔城地区第一高级中学2022-2023学年高一下学期开学考试化学试题【全国百强校】宁夏回族自治区银川一中2018-2019学年高一下学期期中考试化学试题云南省麒麟高中2018-2019学年高一6月份考试化学试题山西省应县第一中学校2018-2019学年高一下学期期中考试化学试题河北省邯郸市第一中学2019—2020学年高一4月月考化学试题四川省三台中学2019-2020学年高一4月空中课堂质量检测化学试题吉林省辽源市辽县第一高级中学2019-2020高一下学期期中考试化学试题四川省棠湖中学2019-2020学年高一下学期期中考试化学试题四川省南充高级中学2020-2021学年高一下学期第一次月考化学试题四川乐山市峨眉二中2020-2021学年高一下学期4月月考化学试题云南省玉溪第二中学2020-2021学年高一下学期第一次月考化学(理)试题甘肃省嘉峪关市第一中学2020-2021学年高一下学期期中考试化学试题四川省内江市资中县球溪中学2021-2022学年高一下学期3月月考化学试题四川省泸县第一中学2021-2022学年高一下学期期中考试化学试题福建省连城县第一中学2021-2022学年高一下学期第一次月考化学试题四川省南充市蓬安中学2021-2022学年高一下学期第一次月考化学试题江苏省洪泽中学六校联考2022-2023学年高一上学期期中考试化学试题陕西省榆林中学2022-2023学年高一上学期期末考试化学试题吉林省长春市实验中学2022-2023学年高一上学期期末考试化学试题(已下线)第15讲 人类对原子结构的认识-【暑假自学课】2023年新高一暑假精品课(苏教版2019)吉林省白山市2023-2024学年高一上学期1月期末考试化学试题
名校
解题方法
7 . 如果ag某气体中所含有的分子数为b,则cg该气体在标准状况下的体积是(式中 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)A. | B. | C.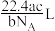 | D.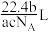 |
您最近一年使用:0次
2023-12-16更新
|
248次组卷
|
44卷引用:安徽省滁州市定远中学2023-2024学年高一下学期开学摸底检测卷化学试题
安徽省滁州市定远中学2023-2024学年高一下学期开学摸底检测卷化学试题宁夏育才中学2022-2023学年高一下学期开学考试化学试题吉林省延边朝鲜族自治州汪清县第四中学2019-2020学年高一上学期第一次阶段考试化学试题深圳市第二高级中学2019-2020学年高一上学期第一学段考试化学试题甘肃省天水市第一中学2020-2021学年高一上学期第一学段考试化学试题河北省保定市徐水区第一中学2020-2021学年高一上学期10月月考化学试题吉林省白城市洮南一中2020-2021学年高一上学期期中考试化学试题湖北省松滋市言程中学2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】92(已下线)练习3 化学中常用的物理量——物质的量-2020-2021学年【补习教材·寒假作业】高一化学(鲁科版2019)陕西省宝鸡市渭滨高中2020-2021学年高一上学期第一次月考化学试题重庆市凤鸣山中学2020-2021学年高一上学期期中考试化学试题安徽省芜湖市第一中学2019-2020学年高一上学期12月月考化学试题福建省南安市柳城中学2020-2021学年高一上学期期中考试化学试题(已下线)衔接点18 气体摩尔体积-2021年初升高化学无忧衔接(已下线)2.3.2 气体摩尔体积-2021-2022学年高一化学10分钟课前预习练(人教版2019必修第一册)(附参考答案)第2章第三节第2课时气体摩尔体积(课中)——课前、课中、课后同步专题精编(人教版2019必修第一册)(已下线)第5讲 物质的量-2020-2021学年秋季班高一上学期化学教材知识点精讲练(沪科版)北京市海淀区中国地质大学附属中学2019-2020学年高一上学期9月月考化学试卷福建省宁化第一中学2021-2022学年高一上学期第一次阶段考试化学试题江苏省淮安市六校联考2021-2022学年高一上学期第一次月考化学试题上海市宝山中学2021-2022学年高一上学期10月考试化学试题陕西省宝鸡市金台区2021-2022学年高一上学期期中考试化学试题陕西省宝鸡市渭滨中学2021-2022学年高一上学期第一次月考化学试题(已下线)衔接点19 气体摩尔体积-2022年初升高化学无忧衔接?宁夏固原市第一中学2023届高三上学期第一次月考化学试题甘肃省镇原县第二中学2021-2022学年高一上学期第一次月月清考试化学试题四川省凉山州宁南中学2022-2023学年高一上学期第一次月考化学试题上海市川沙中学2022-2023学年高一上学期期中考试化学试题河北省张家口市宣化第一中学2022-2023学年高一上学期期中线上考试化学试题(已下线)考点06 物质的量 气体摩尔体积(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)作业(十四) 气体摩尔体积 第2课时 气体摩尔体积宁夏回族自治区中卫市中宁县第一中学2022-2023学年高三上学期10月月考化学试题福建省福州市福清市高中联合体2023-2024学年高一上学期11月期中考试化学试题黑龙江省哈尔滨市2023-2024学年师大附中高一上学期化学期中测试黑龙江省哈尔滨师范大学附属中学2023-2024学年高一上学期11月期中化学试题重庆市广益中学校2023-2024学年高一上学期第二次月考化学试题甘肃省天水市第一中学2023-2024学年高一上学期12月月考化学试题广东省梅州市大埔县虎山中学2023-2024学年高三上学期10月期中考试化学试题辽宁省朝阳市 建平县实验中学2023-2024学年高一上学期12月月考化学试题云南省宣威市第六中学2023-2024学年高一上学期10月月考化学试题上海市华东师范大学附属东昌中学2023-2024学年高一上学期12月月考化学试题河北省邯郸市魏县第五中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
8 . 用NA表示阿伏加德罗常数,下列叙述正确的是
| A.标准状况下,2.24L乙醇中含有的分子数为0.1NA |
B.0.2molNH 中含有的电子数为2.2NA 中含有的电子数为2.2NA |
| C.常温常压下,17gNH3含有的原子数目为4NA |
| D.4.0gNaOH与MgO的混合物中含有的离子数为0.4NA |
您最近一年使用:0次
2023-11-06更新
|
705次组卷
|
5卷引用:湖南省长沙市湖南师范大学附属中学2023-2024学年高一下学期入学考试化学试卷
9 . 完成下列问题。
(1)在 的反应中,该反应中
的反应中,该反应中 体现的性质是
体现的性质是___________ 。若反应生成标准状况下11.2L NO,则被还原的 为
为___________ mol,转移电子为___________ mol。
(2)若 为阿伏伽德罗常数,3.4g氨气中所含氢原子数为
为阿伏伽德罗常数,3.4g氨气中所含氢原子数为___________ ,所含质子数为___________ 。
(3)同温同压下,相同体积的氢气和气体A的质量分别是0.2g和2.8g,则气体A的摩尔质量为___________ ,该气体可能是___________ (写化学式)。
(1)在
 的反应中,该反应中
的反应中,该反应中 体现的性质是
体现的性质是 为
为(2)若
 为阿伏伽德罗常数,3.4g氨气中所含氢原子数为
为阿伏伽德罗常数,3.4g氨气中所含氢原子数为(3)同温同压下,相同体积的氢气和气体A的质量分别是0.2g和2.8g,则气体A的摩尔质量为
您最近一年使用:0次
2023-08-28更新
|
125次组卷
|
2卷引用:河北省沧州市盐山中学2023-2024学年高一下学期开学化学试题
名校
10 .  为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.18g重水( )中含有的质子数为 )中含有的质子数为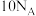 |
B.0.5mol乙醇中含有的共价键数为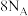 |
C.32g环状 ( ( )分子中含有的S-S键数为 )分子中含有的S-S键数为 |
D.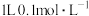 的HClO溶液中 的HClO溶液中 的数目为 的数目为 |
您最近一年使用:0次
2023-07-12更新
|
134次组卷
|
4卷引用:北京市第五中学2023-2024学年高二上学期开学考化学试卷



