名校
解题方法
1 . 某消毒液的主要成分为NaClO,还含有一定量的NaOH,已知饱和NaClO溶液的pH约为11,下列用来解释事实的方程式中不合理的是
A.该消毒液的pH约为12: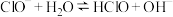 |
B.该消毒液可用NaOH溶液吸收 制备: 制备: |
C.该消毒液与洁厕灵(主要成分为HCl)混用会产生 ; ; |
D.该消毒液加白酯生成HClO,可增强源白作用: |
您最近一年使用:0次
名校
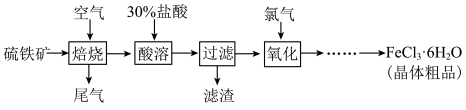
2 . 以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:___________ ,检验氧化生成的阳离子的试剂是___________ 。
(2)尾气中主要含N2、O2、SO2和少量的CO2、H2O,取标准状况下的尾气VL测定SO2含量:
方案一:让尾气缓慢通过以下装置。___________ ,该装置的作用是___________ 。
②实验时先通入尾气,再通入一定量氮气。若通过B装置的增重来测量SO2的体积分数。你认为该方案是否合理___________ (填“是”或“否”)。
方案二:将尾气缓慢通过足量溴水,在所得的溶液中加入过量氯化钡溶液后,过滤,将沉淀洗涤、干燥,称得其质量为mg。
①加入过量氯化钡溶液的目的是___________ 。
②进行沉淀洗涤的方法是___________ 。
③SO2含量的表达式是___________ (用含m、V的代数式表示)。
(3)从FeCl3溶液中得到FeCl3·6H2O晶体的操作包括___________ 、冷却结晶、过滤,该过程需保持盐酸过量,抑制Fe3+水解。
(2)尾气中主要含N2、O2、SO2和少量的CO2、H2O,取标准状况下的尾气VL测定SO2含量:
方案一:让尾气缓慢通过以下装置。
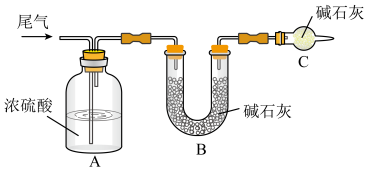
②实验时先通入尾气,再通入一定量氮气。若通过B装置的增重来测量SO2的体积分数。你认为该方案是否合理
方案二:将尾气缓慢通过足量溴水,在所得的溶液中加入过量氯化钡溶液后,过滤,将沉淀洗涤、干燥,称得其质量为mg。
①加入过量氯化钡溶液的目的是
②进行沉淀洗涤的方法是
③SO2含量的表达式是
(3)从FeCl3溶液中得到FeCl3·6H2O晶体的操作包括
您最近一年使用:0次
名校
3 . 某铜镉渣的主要成分为单质Zn、ZnSO4以及铜、镉(Cd)、铁、钴(Co)等金属单质或它们的氧化物。某同学以其为原料设计如图工艺流程回收铜、镉、铁、钴。
(1)“浸出”过程生成大量气体是___________ (填化学式),写出一种提高“浸出”效率和浸出率的措施:___________ 。
(2)“氧化除铁”原理是空气中的氧气将浸出液中的Fe2+氧化为α-FeOOH,写出该反应的离子方程式:___________ 。
(3)“除锰”时,参加反应的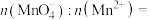
___________ 。
(4)若在实验室进行萃取“除铜”,所必须用到的仪器是___________ ,萃取前对仪器进行的操作是___________ ,放液时,上层液体由___________ (填“上口”或“下口”)倒(放)出。
(5)水相中主要含Co2+,经检测c(Co2+)=0.01mol·L-1。向水相通入氨气调节pH=___________ 时,水相中Co2+沉淀完全(已知常温下,Ksp[Co(OH)2]=1.0×10-15;溶液中c(Co2+)=1×10-5mol·L-1视为沉淀完全)。
(6)控制一定条件,用惰性电极电解ZnSO4溶液可制备单质锌,电解时阳极反应式为___________ 。
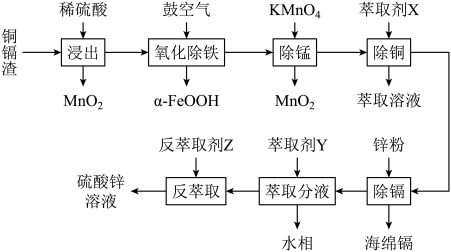
(1)“浸出”过程生成大量气体是
(2)“氧化除铁”原理是空气中的氧气将浸出液中的Fe2+氧化为α-FeOOH,写出该反应的离子方程式:
(3)“除锰”时,参加反应的
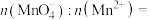
(4)若在实验室进行萃取“除铜”,所必须用到的仪器是
(5)水相中主要含Co2+,经检测c(Co2+)=0.01mol·L-1。向水相通入氨气调节pH=
(6)控制一定条件,用惰性电极电解ZnSO4溶液可制备单质锌,电解时阳极反应式为
您最近一年使用:0次
名校
4 . 磁选后的炼铁高钛炉渣,主要成分有 、
、 、
、 、MgO、CaO以及少量的
、MgO、CaO以及少量的 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
已知:①“焙烧”中, 、
、 几乎不发生反应,
几乎不发生反应, 、MgO、CaO、
、MgO、CaO、 转化为相应的硫酸盐;②
转化为相应的硫酸盐;② 。回答下列问题:
。回答下列问题:
(1)为了加快“焙烧”速率,可采用的物理方法为______ (填一种即可)。
(2) “焙烧”时,转化为
“焙烧”时,转化为 ;在
;在 的
的 溶液中,各离子浓度由大到小的顺序为
溶液中,各离子浓度由大到小的顺序为______ (填离子符号)。
(3)“水浸”后的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至11.6,最先析出的离子为______ (填离子符号)。
(4)水浸渣在160℃“酸溶”,最适合的加热方式为______ (填“水浴”或“油浴”)加热。
(5)“酸溶”后,将溶液适当稀释并加热, 水解析出
水解析出 沉淀,该反应的离子方程式为
沉淀,该反应的离子方程式为______ 。
 、
、 、
、 、MgO、CaO以及少量的
、MgO、CaO以及少量的 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。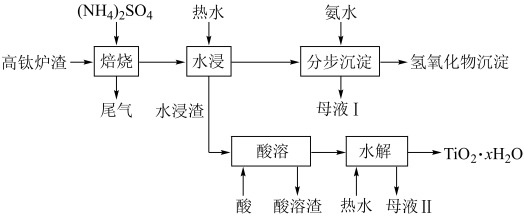
金属离子 |
|
|
|
|
开始沉淀( | 1.5 | 3.4 | 8.9 | 12.0 |
沉淀完全( | 2.8 | 4.7 | 10.9 | 13.8 |
 、
、 几乎不发生反应,
几乎不发生反应, 、MgO、CaO、
、MgO、CaO、 转化为相应的硫酸盐;②
转化为相应的硫酸盐;② 。回答下列问题:
。回答下列问题:(1)为了加快“焙烧”速率,可采用的物理方法为
(2)
 “焙烧”时,转化为
“焙烧”时,转化为 ;在
;在 的
的 溶液中,各离子浓度由大到小的顺序为
溶液中,各离子浓度由大到小的顺序为(3)“水浸”后的pH约为2.0,在“分步沉淀”时用氨水逐步调节pH至11.6,最先析出的离子为
(4)水浸渣在160℃“酸溶”,最适合的加热方式为
(5)“酸溶”后,将溶液适当稀释并加热,
 水解析出
水解析出 沉淀,该反应的离子方程式为
沉淀,该反应的离子方程式为
您最近一年使用:0次
5 . 下列离子方程式书写错误的是
A.过氧化钠溶于硫酸铜溶液中: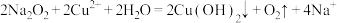 |
B.向 溶液中通入少量 溶液中通入少量 气体: 气体: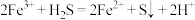 |
C.向碳酸氢钠溶液中滴加盐酸: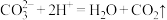 |
D.向次氯酸钠溶液中通入少量 : :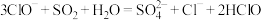 |
您最近一年使用:0次
6 . 下列化学用语不正确 的是
A.硫酸铝的电离方程式: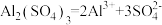 |
B.碳酸氢钠受热分解的化学方程式: 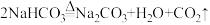 |
C.用电子式表示氯化钠的形成过程: 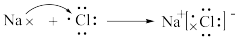 |
D.碳酸钙与盐酸反应的离子方程式: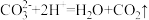 |
您最近一年使用:0次
解题方法
7 . 下列反应的离子方程式书写正确的是
A. 与足量NaOH溶液: 与足量NaOH溶液: |
B. 溶液与 溶液与 溶液: 溶液: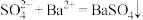 |
C. 与浓盐酸: 与浓盐酸: |
D. 与NaOH溶液: 与NaOH溶液: |
您最近一年使用:0次
8 . A和B两支试管所盛的溶液中共含有K+、Ag+、Mg2+、Cl−、OH−、 六种离子,向试管A的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题:
六种离子,向试管A的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题:
(1)若向某试管中滴入稀盐酸产生沉淀,则该试管为___________ (填“A”或“B”)。
(2)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是___________ (填化学式)。
(3)若将试管A和试管B中的溶液按一定体积比混合后过滤,蒸干所得滤液可得到一种纯净物,该物质为___________ ( 写化学式),则混合过程中发生反应的离子方程式为Ag++Cl-=AgCl↓与___________ (不考虑Ag+与OH−的反应)。
(4)按如图所示操作,充分反应后:___________ 。
②结合Ⅰ、Ⅱ实验现象可知 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为___________ 。
(5)已知 可发生反应:
可发生反应:
①该反应中氧化剂是___________ (填化学式)。
②用双线桥法标出电子转移的数目和方向:___________ 。
 六种离子,向试管A的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题:
六种离子,向试管A的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题:(1)若向某试管中滴入稀盐酸产生沉淀,则该试管为
(2)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是
(3)若将试管A和试管B中的溶液按一定体积比混合后过滤,蒸干所得滤液可得到一种纯净物,该物质为
(4)按如图所示操作,充分反应后:
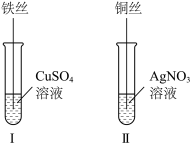
②结合Ⅰ、Ⅱ实验现象可知
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(5)已知
 可发生反应:
可发生反应:
①该反应中氧化剂是
②用双线桥法标出电子转移的数目和方向:
您最近一年使用:0次
9 . 下列反应的离子方程式或电离方程式正确的是
A.氧化铜与稀硫酸反应: |
B.向 NaHSO4溶液中滴加 Ba(OH)2溶液至SO 恰好沉淀完全: 恰好沉淀完全: |
C.盐酸和足量碳酸钠反应:  |
D.硫酸氢钠溶于水的电离方程式: |
您最近一年使用:0次
10 . 某矿物炼铜后的矿渣固体主要成分为 、
、 、
、 以及少量的CuO、PbO、
以及少量的CuO、PbO、 等。一种利用这种碱性渣提取高纯碲和粗硒的工艺流程如下图所示。
等。一种利用这种碱性渣提取高纯碲和粗硒的工艺流程如下图所示。 ;
;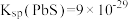 ;
;
②CuO和PbO均具有一定的“两性”,“碱浸”时均能溶于氢氧化钠溶液。
回答下列问题:
(1)“碱浸”时应进行加热、搅拌等操作,目的是___________ 。
(2)下图为温度和NaOH溶液浓度对确浸出率的影响,实际生产中“碱浸”工序的反应条件为80℃、 的NaOH溶液,而不用更高温度和更大浓度NaOH溶液的原因是
的NaOH溶液,而不用更高温度和更大浓度NaOH溶液的原因是___________ 。 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(4)滤渣3的主要成分为___________ 。滤液1中 沉淀完全时,
沉淀完全时, 的最大值是
的最大值是___________  (保留小数点后2位。某离子浓度低于
(保留小数点后2位。某离子浓度低于 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。
(5)在 溶液中通入
溶液中通入 制Se的离子方程式为
制Se的离子方程式为___________ 。
(6)电解后电解液可返回___________ 工序循环使用。
 、
、 、
、 以及少量的CuO、PbO、
以及少量的CuO、PbO、 等。一种利用这种碱性渣提取高纯碲和粗硒的工艺流程如下图所示。
等。一种利用这种碱性渣提取高纯碲和粗硒的工艺流程如下图所示。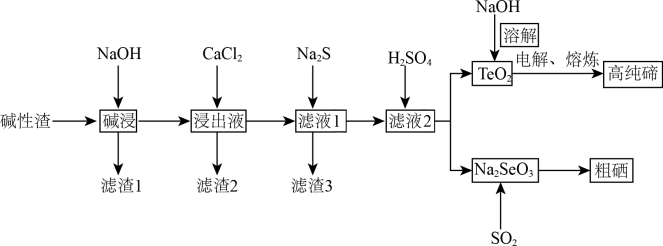
 ;
;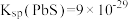 ;
;②CuO和PbO均具有一定的“两性”,“碱浸”时均能溶于氢氧化钠溶液。
回答下列问题:
(1)“碱浸”时应进行加热、搅拌等操作,目的是
(2)下图为温度和NaOH溶液浓度对确浸出率的影响,实际生产中“碱浸”工序的反应条件为80℃、
 的NaOH溶液,而不用更高温度和更大浓度NaOH溶液的原因是
的NaOH溶液,而不用更高温度和更大浓度NaOH溶液的原因是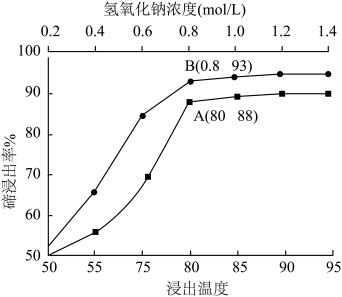
 发生反应的离子方程式为
发生反应的离子方程式为(4)滤渣3的主要成分为
 沉淀完全时,
沉淀完全时, 的最大值是
的最大值是 (保留小数点后2位。某离子浓度低于
(保留小数点后2位。某离子浓度低于 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。(5)在
 溶液中通入
溶液中通入 制Se的离子方程式为
制Se的离子方程式为(6)电解后电解液可返回
您最近一年使用:0次





 )的pH
)的pH )的pH
)的pH

