解题方法
1 . 为了减少煤燃烧产生的二氧化硫的排放,可以采取各种方法,其中一种方法是使用微生物脱硫技术。煤炭中以FeS2形式存在的硫,在有水和空气存在的条件下,用脱硫微生物起氧化还原作用:在细菌作用下FeS2 中的硫元素首先被氧化最高价态,然后亚铁离子继续被氧化成高价铁离子。
(1)请分别写出上述过程总离子反应方程式___________ 。
(2)某大型电厂使用的煤炭中含有FeS2的质量分数为1.2%,若每月燃烧该种煤炭100万吨,理论上回收硫酸___________ 吨;硫酸铁___________ 吨。
(1)请分别写出上述过程总离子反应方程式
(2)某大型电厂使用的煤炭中含有FeS2的质量分数为1.2%,若每月燃烧该种煤炭100万吨,理论上回收硫酸
您最近一年使用:0次
解题方法
2 .
(1) I向硫酸锌水溶液中滴加适当浓度的氨水至过量,发生两步主要反应。简述实验现象_____ ,写出两步主要反应的离子方程式______
II化合物[Cu(pydc)(amp)]·3H2O的组成为C11H14CuN4O7,热重分析曲线表明,该化合物受热分解发生两步失重,第一个失重峰在200~250°C,失重的质量分数为15.2%。第二个失重峰在400~500°C,失重后的固态残渣质量为原化合物质量的20.0%。pydc和amp是含芳环的有机配体。
通过计算回答:
(2)第一步失重失去的组分_____ 。
(3)第二步失重后的固态残渣是______ ,解释理由______ 。
(1) I向硫酸锌水溶液中滴加适当浓度的氨水至过量,发生两步主要反应。简述实验现象
II化合物[Cu(pydc)(amp)]·3H2O的组成为C11H14CuN4O7,热重分析曲线表明,该化合物受热分解发生两步失重,第一个失重峰在200~250°C,失重的质量分数为15.2%。第二个失重峰在400~500°C,失重后的固态残渣质量为原化合物质量的20.0%。pydc和amp是含芳环的有机配体。
通过计算回答:
(2)第一步失重失去的组分
(3)第二步失重后的固态残渣是
您最近一年使用:0次
解题方法
3 . 某厂以工业粗盐(含Ca2+、 Mg2+、SO 等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,其工艺流程如下图所示:
等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,其工艺流程如下图所示:
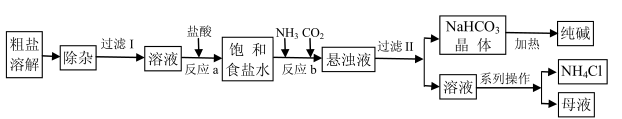
请回答下列问题:
(1)“除杂”步骤中需加入两种试剂,按加入顺序写出其名称____________ 。
(2)写出“反应a”的离子方程式___________ ;写出“反应b”的化学方程式___________ 。
(3)“过滤II”所得“溶液”中除NH 和Cl-外,还存在的阳离子有
和Cl-外,还存在的阳离子有___________ ,阴离子有___________ ;对该溶液进行的“系列操作”包括___________ 。
(4)上述工艺流程中可循环利用的物质有___________ 。
(5)工业纯碱的等级标准如下表所示:
称取某纯碱样品10.00g, 加入适量水溶解,再加入过量CaCl2溶液,充分反应后过滤、洗涤沉淀、干燥,称得沉淀质量为9.33g。请通过计算判断该纯碱样品的等级___________ 。
 等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,其工艺流程如下图所示:
等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,其工艺流程如下图所示:
请回答下列问题:
(1)“除杂”步骤中需加入两种试剂,按加入顺序写出其名称
(2)写出“反应a”的离子方程式
(3)“过滤II”所得“溶液”中除NH
 和Cl-外,还存在的阳离子有
和Cl-外,还存在的阳离子有(4)上述工艺流程中可循环利用的物质有
(5)工业纯碱的等级标准如下表所示:
| 等级 | 优等品 | 一等品 | 合格品 |
| Na2CO3含量1% | ≥99.2 | ≥98.8 | ≥98.0 |
称取某纯碱样品10.00g, 加入适量水溶解,再加入过量CaCl2溶液,充分反应后过滤、洗涤沉淀、干燥,称得沉淀质量为9.33g。请通过计算判断该纯碱样品的等级
您最近一年使用:0次
解题方法
4 . 下列说法不正确 的是
A.向磷酸二氢钠溶液中加入过量澄清石灰水: |
B.用重铬酸钾法测定白酒中乙醇的含量: |
C.用碳酸钠溶液处理锅炉水垢中的硫酸钙: |
| D.制摩尔盐时用酒精洗涤产品,制阿司匹林时用冷水洗涤产品 |
您最近一年使用:0次
9-10高三·江苏·阶段练习
5 . 氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
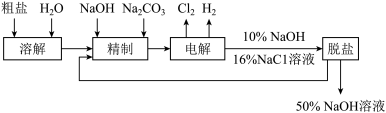
依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应式为__________ 。 与电源负极相连的电极附近,溶液pH ________ (选填:不变,升高或下降)。
(2)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为___________ ,
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是______ 。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为_________ 。
a. 先加NaOH,后加Na2CO3,再加钡试剂
b. 先加NaOH,后加钡试剂,再加Na2CO3
c. 先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________ 、冷却、_________ (填写操作名称)除去NaCl。
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷 的食盐水时,Cl2与NaOH充分接触,产物仅是 NaClO和H2,相应的化学方程式为_____ 。

依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应式为
(2)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为
a. 先加NaOH,后加Na2CO3,再加钡试剂
b. 先加NaOH,后加钡试剂,再加Na2CO3
c. 先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解
您最近一年使用:0次
2020-03-05更新
|
394次组卷
|
8卷引用:山东省枣庄市滕州市第一中学2019-2020学年高二下学期学习竞赛化学试题
山东省枣庄市滕州市第一中学2019-2020学年高二下学期学习竞赛化学试题(已下线)江苏省2011届高三化学一轮过关测试(7)2015-2016学年吉林省松原高中、白城一中高二上期末联考化学试卷(已下线)同步君 选修4 第4章 第3节 电解原理的应用高中化学人教版 选修四 第四章 电化学基础 第三节 电解池 电解池第二课时(电解原理的应用)(已下线)2018年12月3日 《每日一题》人教选修4-电解饱和食盐水北京市通州区2019-2020学年高二下学期期末考试化学试题宁夏石嘴山市第三中学2020-2021学年高二上学期第一次月考化学试题



