名校
1 . KMnO4是化工生产中的一种重要氧化剂。实验室制备并对产品含量进行测定。请回答下列问题:
(一)制备K2MnO4碱性溶液
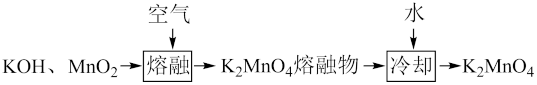 碱性溶液
碱性溶液
(1)“熔融"时应选用的仪器为______ (填选项字母);原因为_____________ 。
a.蒸发皿 b. 普通坩埚 c.铁坩埚 d.烧杯
(2)制备K2MnO4过程中消耗氧化剂和还原剂的物质的量之比为_____________ 。
(二)制备KMnO4
向所得K2MnO4溶液中通入过量CO2,溶液由墨绿色逐渐变为紫黑色并产生黑色沉淀,待反应完全,静置、抽滤,将所得溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得产品。
(3)实验室常用下图装置制备CO2。实验过程中,石灰石应放在装置的______ 部位(填“甲”、“乙”或“丙”);制取CO2时以下操作步骤正确的排列顺序是_______ (填序号)。
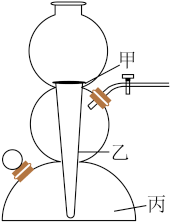
①注入稀盐酸②检查装置气密性③装入大理石
(4)制备KMnO4的离子方程式为_______________________
(三) KMnO4纯度检验
称取2.0gKMnO4产品,配成1000mL溶液,取20.00mL于锥形瓶中,并加入足量稀硫酸酸化,然后用0.02mol·L-1的亚硫酸氢钠(NaHSO3)标准溶液滴定,达到滴定终点时消耗标准溶液的体积为25.00mL。
(5)滴定时发生反应的离子方程式为______________ ;滴定到终点的现象为_____ 产品中KMnO4的质量分数为_______________
(一)制备K2MnO4碱性溶液
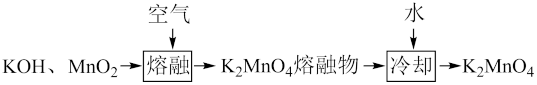 碱性溶液
碱性溶液(1)“熔融"时应选用的仪器为
a.蒸发皿 b. 普通坩埚 c.铁坩埚 d.烧杯
(2)制备K2MnO4过程中消耗氧化剂和还原剂的物质的量之比为
(二)制备KMnO4
向所得K2MnO4溶液中通入过量CO2,溶液由墨绿色逐渐变为紫黑色并产生黑色沉淀,待反应完全,静置、抽滤,将所得溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得产品。
(3)实验室常用下图装置制备CO2。实验过程中,石灰石应放在装置的

①注入稀盐酸②检查装置气密性③装入大理石
(4)制备KMnO4的离子方程式为
(三) KMnO4纯度检验
称取2.0gKMnO4产品,配成1000mL溶液,取20.00mL于锥形瓶中,并加入足量稀硫酸酸化,然后用0.02mol·L-1的亚硫酸氢钠(NaHSO3)标准溶液滴定,达到滴定终点时消耗标准溶液的体积为25.00mL。
(5)滴定时发生反应的离子方程式为
您最近一年使用:0次
2020-10-03更新
|
477次组卷
|
3卷引用:陕西省西安市第一中学2021届高三上学期模拟调研考试化学试题
陕西省西安市第一中学2021届高三上学期模拟调研考试化学试题陕西省宝鸡市凤翔中学2021届高三上学期期中考试化学试题(已下线)专题27 物质制备类综合性实验题(学生版)-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
2 . 为了降低电子垃圾对环境构成的影响,将一批废弃的线路板简单处理后,得到含 、
、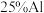 、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:

 第
第 步Cu与混酸反应的离子方程式为
步Cu与混酸反应的离子方程式为______  得到滤渣1的主要成分为
得到滤渣1的主要成分为______ 。
 第
第 步中加入
步中加入 的作用是
的作用是______ ,使用 的优点是
的优点是______ ;调溶液pH的目的是______ 。
 简述第
简述第 步由滤液2得到
步由滤液2得到 的方法是
的方法是______ 。
 由滤渣2制取
由滤渣2制取 ,设计了以下三种方案:
,设计了以下三种方案:
甲:滤渣 酸浸液
酸浸液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O
乙:滤渣 酸浸液
酸浸液 滤液
滤液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O
丙:滤渣2 滤液
滤液 溶液
溶液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O
上述三种方案中,______ 方案不可行,原因是______ ;从原子利用率角度考虑,______ 方案更合理。
 用滴定法测定
用滴定法测定 含量.取a g试样配成100mL溶液,每次取
含量.取a g试样配成100mL溶液,每次取 ,消除干扰离子后,用c
,消除干扰离子后,用c
 标准溶液滴定至终点,平均消耗EDTA溶液b
标准溶液滴定至终点,平均消耗EDTA溶液b  滴定反应如下:
滴定反应如下: 写出计算
写出计算 质量分数的表达式
质量分数的表达式
______ 。
 、
、 、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
| 方法Ⅰ | 用炭粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法:  |
| 方法Ⅲ | 用肼 还原新制 还原新制 |
 第
第 步Cu与混酸反应的离子方程式为
步Cu与混酸反应的离子方程式为 得到滤渣1的主要成分为
得到滤渣1的主要成分为 第
第 步中加入
步中加入 的作用是
的作用是 的优点是
的优点是 简述第
简述第 步由滤液2得到
步由滤液2得到 的方法是
的方法是 由滤渣2制取
由滤渣2制取 ,设计了以下三种方案:
,设计了以下三种方案:甲:滤渣
 酸浸液
酸浸液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O乙:滤渣
 酸浸液
酸浸液 滤液
滤液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O丙:滤渣2
 滤液
滤液 溶液
溶液 Al2(SO4)3﹒18H2O
Al2(SO4)3﹒18H2O上述三种方案中,
 用滴定法测定
用滴定法测定 含量.取a g试样配成100mL溶液,每次取
含量.取a g试样配成100mL溶液,每次取 ,消除干扰离子后,用c
,消除干扰离子后,用c
 标准溶液滴定至终点,平均消耗EDTA溶液b
标准溶液滴定至终点,平均消耗EDTA溶液b  滴定反应如下:
滴定反应如下: 写出计算
写出计算 质量分数的表达式
质量分数的表达式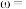
您最近一年使用:0次
名校
解题方法
3 . 2020年初,突如其来的新型冠状肺炎在全世界肆虐,依据研究,含氯消毒剂可以有效灭活新冠病毒,为阻断疫情做出了巨大贡献。二氧化氯(C1O2)就是其中一种高效消毒灭菌剂。但其稳定性较差,可转化为NaClO2保存。分别利用吸收法和电解法两种方法得到较稳定的NaClO2。其工艺流程示意图如图所示:

已知:1.纯C1O2易分解爆炸,一般用稀有气体或空气稀释到10%以下。
2.长期放置或高于60℃时NaClO2易分解生成NaClO3和NaCl
(1)步骤1中,生成C1O2的离子方程式是___ ,通入空气的作用是___ 。
(2)方法1中,反应的离子方程式是___ ,利用方法1制NaClO2时,温度不能超过20℃,可能的原因是___ 。
(3)方法2中,NaClO2在___ 生成(选填“阴极”或“阳极”)。
(4)NaClO2的溶解度曲线如图所示,步骤3中从NaClO2溶液中获得NaClO2的操作是___ 。

(5)为测定制得的晶体中NaClO2的含量,做如下操作:
①称取a克样品于烧杯中,加入适量蒸馏水溶解后加过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应。将所得混合液配成100mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,用bmol•L-1Na2S2O3标准液滴定,至滴定终点。重复2次,测得消耗标准溶液的体积的平均值为cmL(已知:I2+2S2O32-=2I-+S4O62-)。样品中NaClO2的质量分数为___ 。(用含a、b、c的代数式表小)。在滴定操作正确无误的情况下,测得结果偏高,可能的原因是___ (用离子方程式和文字表示)。
(6)NaClO2使用时,加入稀盐酸即可迅速得到C1O2。但若加入盐酸浓度过大,则气体产物中Cl2的含量会增大,原因是___ 。

已知:1.纯C1O2易分解爆炸,一般用稀有气体或空气稀释到10%以下。
2.长期放置或高于60℃时NaClO2易分解生成NaClO3和NaCl
(1)步骤1中,生成C1O2的离子方程式是
(2)方法1中,反应的离子方程式是
(3)方法2中,NaClO2在
(4)NaClO2的溶解度曲线如图所示,步骤3中从NaClO2溶液中获得NaClO2的操作是

(5)为测定制得的晶体中NaClO2的含量,做如下操作:
①称取a克样品于烧杯中,加入适量蒸馏水溶解后加过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应。将所得混合液配成100mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,用bmol•L-1Na2S2O3标准液滴定,至滴定终点。重复2次,测得消耗标准溶液的体积的平均值为cmL(已知:I2+2S2O32-=2I-+S4O62-)。样品中NaClO2的质量分数为
(6)NaClO2使用时,加入稀盐酸即可迅速得到C1O2。但若加入盐酸浓度过大,则气体产物中Cl2的含量会增大,原因是
您最近一年使用:0次
2020-05-15更新
|
529次组卷
|
6卷引用:第3讲 离子反应-2021年高考化学一轮复习名师精讲练
名校
解题方法
4 . 高纯硝酸锶 可用于制造信号灯、光学玻璃等。工业级硝酸锶含硝酸钙、硝酸钡等杂质,提纯流程如下:
可用于制造信号灯、光学玻璃等。工业级硝酸锶含硝酸钙、硝酸钡等杂质,提纯流程如下:

已知: 滤渣1的成分为
滤渣1的成分为 、
、 ;
; 铬酸
铬酸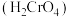 为弱酸。
为弱酸。
 酸浸不能采用高温的原因是
酸浸不能采用高温的原因是____________ ,滤液1的主要溶质是________ 。
 相对于水洗,用浓硝酸洗涤的优点是
相对于水洗,用浓硝酸洗涤的优点是___________ 。
 滤液2中过量的
滤液2中过量的 被
被 还原为
还原为 ,同时放出无污染的气体,写出发生反应的离子方程式:
,同时放出无污染的气体,写出发生反应的离子方程式:________ 。
 已知
已知 类似氢氧化铝,还原后溶液的pH不能大于8的原因是
类似氢氧化铝,还原后溶液的pH不能大于8的原因是 结合离子方程式说明理由
结合离子方程式说明理由
__________ 。
 为了测定滤渣2中
为了测定滤渣2中 的含量,进行以下实验:
的含量,进行以下实验:
mg滤渣2 溶液
溶液
滴定终点时消耗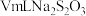 溶液
溶液 已知:
已知: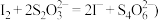 。
。
 滤渣2中
滤渣2中 摩尔质量为
摩尔质量为 的质量分数为
的质量分数为___________  用代数式表示
用代数式表示 。
。
 若加入的HI溶液过量太多,测定结果会
若加入的HI溶液过量太多,测定结果会_________  “偏高”“偏低”或“无影响”
“偏高”“偏低”或“无影响” 。
。
 可用于制造信号灯、光学玻璃等。工业级硝酸锶含硝酸钙、硝酸钡等杂质,提纯流程如下:
可用于制造信号灯、光学玻璃等。工业级硝酸锶含硝酸钙、硝酸钡等杂质,提纯流程如下:
已知:
 滤渣1的成分为
滤渣1的成分为 、
、 ;
; 铬酸
铬酸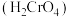 为弱酸。
为弱酸。 酸浸不能采用高温的原因是
酸浸不能采用高温的原因是 相对于水洗,用浓硝酸洗涤的优点是
相对于水洗,用浓硝酸洗涤的优点是 滤液2中过量的
滤液2中过量的 被
被 还原为
还原为 ,同时放出无污染的气体,写出发生反应的离子方程式:
,同时放出无污染的气体,写出发生反应的离子方程式: 已知
已知 类似氢氧化铝,还原后溶液的pH不能大于8的原因是
类似氢氧化铝,还原后溶液的pH不能大于8的原因是 结合离子方程式说明理由
结合离子方程式说明理由
 为了测定滤渣2中
为了测定滤渣2中 的含量,进行以下实验:
的含量,进行以下实验:mg滤渣2
 溶液
溶液
滴定终点时消耗
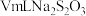 溶液
溶液 已知:
已知: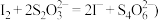 。
。 滤渣2中
滤渣2中 摩尔质量为
摩尔质量为 的质量分数为
的质量分数为 用代数式表示
用代数式表示 。
。 若加入的HI溶液过量太多,测定结果会
若加入的HI溶液过量太多,测定结果会 “偏高”“偏低”或“无影响”
“偏高”“偏低”或“无影响” 。
。
您最近一年使用:0次
2020-02-04更新
|
350次组卷
|
2卷引用:2020届高考化学二轮复习大题精准训练 ——侧重提纯类无机工艺流程题
解题方法
5 . I.水中溶解氧气的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I-完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,反应方程式为2S2O +I2=S4O
+I2=S4O +2I-,测定过程中物质的转化关系如下:O2
+2I-,测定过程中物质的转化关系如下:O2 2MnO(OH)2
2MnO(OH)2 I2
I2 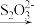 S4O
S4O 。
。
(1)写出O2将Mn2+氧化成MnO(OH)2的离子方程式:____________________ 。
(2)取池塘水样100.00 mL,按上述方法测定水中溶解的氧气浓度,消耗0.01000 mol·L-1 Na2S2O3标准溶液13.50 mL。计算该水样中溶解的氧气浓度为_________ mg·L-1。
Ⅱ.益源生(药品名叫复方硫酸亚铁叶酸片)是一种治疗缺铁性贫血的药物其主要成分有硫酸亚铁、叶酸、干酵母、当归、黄芪、白术等,下面是测定益源生中硫酸亚铁质量分数的实验。取10片复方硫酸亚铁片(每片a毫克)研成粉末,加水溶解,过滤,再将滤液配成100 mL溶液,取出25 mL与双氧水反应(假设叶酸、干酵母、当归、黄芪、白术均不与双氧水反应)。
(1)配制一定浓度的双氧水溶液用质量分数30%、密度1.l g/cm3)的双氧水配制1.0 mol/L的双氧水100 mL,则30%双氧水物质的量浓度为________ mol/L(保留一位小数),需用量筒量取30%的双氧水_________ mL。
(2)该实验在酸性条件下进行,则实验设计的反应原理是_____________ (用离子方程式表示)。
(3)若上述实验消耗1.0 mol/L的双氧水b mL,则每片复方硫酸亚铁叶酸片中硫酸亚铁的质量分数为_________ (用含a、b的式子表示)。
 +I2=S4O
+I2=S4O +2I-,测定过程中物质的转化关系如下:O2
+2I-,测定过程中物质的转化关系如下:O2 2MnO(OH)2
2MnO(OH)2 I2
I2 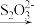 S4O
S4O 。
。(1)写出O2将Mn2+氧化成MnO(OH)2的离子方程式:
(2)取池塘水样100.00 mL,按上述方法测定水中溶解的氧气浓度,消耗0.01000 mol·L-1 Na2S2O3标准溶液13.50 mL。计算该水样中溶解的氧气浓度为
Ⅱ.益源生(药品名叫复方硫酸亚铁叶酸片)是一种治疗缺铁性贫血的药物其主要成分有硫酸亚铁、叶酸、干酵母、当归、黄芪、白术等,下面是测定益源生中硫酸亚铁质量分数的实验。取10片复方硫酸亚铁片(每片a毫克)研成粉末,加水溶解,过滤,再将滤液配成100 mL溶液,取出25 mL与双氧水反应(假设叶酸、干酵母、当归、黄芪、白术均不与双氧水反应)。
(1)配制一定浓度的双氧水溶液用质量分数30%、密度1.l g/cm3)的双氧水配制1.0 mol/L的双氧水100 mL,则30%双氧水物质的量浓度为
(2)该实验在酸性条件下进行,则实验设计的反应原理是
(3)若上述实验消耗1.0 mol/L的双氧水b mL,则每片复方硫酸亚铁叶酸片中硫酸亚铁的质量分数为
您最近一年使用:0次
名校
6 . 向50g质量分数为10.6%的Na2CO3溶液中,逐滴加入CaCl2稀溶液。测得溶液中离子的数量变化如图。请据此分析以下问题:
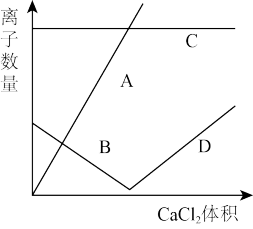
(1)请指出以下曲线表示的离子化学式:
A___________________
C___________________
D___________________
(2)反应的化学反应方程式为_______________________________________ 。
(3)当A、C曲线相交时,生成的沉淀质量为____________ g。

(1)请指出以下曲线表示的离子化学式:
A
C
D
(2)反应的化学反应方程式为
(3)当A、C曲线相交时,生成的沉淀质量为
您最近一年使用:0次
2020-11-19更新
|
226次组卷
|
4卷引用:安徽省舒城中学2020-2021学年高一上学期第一次统考化学试题
安徽省舒城中学2020-2021学年高一上学期第一次统考化学试题江西省南昌市进贤一中2020-2021学年高一上学期第二次月考化学试题(已下线)1.2.2 离子反应和离子方程式(好题帮)-备战2023年高考化学一轮复习考点帮(新教材新高考)?(已下线)2.2.2 离子方程式的书写-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)
7 . MnO2是重要的化工原料,山软锰矿制备MnO2的一种工艺流程如图:
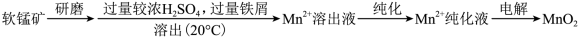
资料:①软锰矿的主要成分为MnO2,主要杂质有Al2O3和SiO2
②金属离于沉淀的pH
③该工艺条件下,MnO2与H2SO4反应。
(1)溶出
①溶出前,软锰矿需研磨。目的是____ 。
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示:
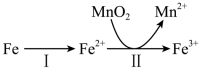
i.步骤II是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是____ 。
ii.若Fe2+全部来自于反应Fe+2H+=Fe2++H2↑,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2。而实际比值(0.9)小于2,原因是____ 。
(2)纯化。已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2,后加入NH3·H2O,调溶液pH≈5,说明试剂加入顺序及调节pH的原因:____ 。
(3)电解。Mn2+纯化液经电解得MnO2。生成MnO2的电极反应式是____ 。
(4)产品纯度测定。向ag产品中依次加入足量bgNa2C2O4和足量稀H2SO4,加热至充分反应。再用cmol·L-1KMnO4溶液滴定剩余Na2C2O4至终点,消耗KMnO4溶液的体积为dL(已知:MnO2及MnO 均被还原为Mn2+。相对分子质量:MnO2-86.94;Na2C2O4-134.0)
均被还原为Mn2+。相对分子质量:MnO2-86.94;Na2C2O4-134.0)
产品纯度为____ (用质量分数表示)。
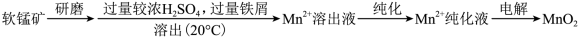
资料:①软锰矿的主要成分为MnO2,主要杂质有Al2O3和SiO2
②金属离于沉淀的pH
| Fe3+ | Al3+ | Mn2+ | Fe2+ | |
| 开始沉淀时 | 1.5 | 3.4 | 5.8 | 6.3 |
| 完全沉淀时 | 2.8 | 4.7 | 7.8 | 8.3 |
(1)溶出
①溶出前,软锰矿需研磨。目的是
②溶出时,Fe的氧化过程及得到Mn2+的主要途径如图所示:

i.步骤II是从软锰矿中溶出Mn2+的主要反应,反应的离子方程式是
ii.若Fe2+全部来自于反应Fe+2H+=Fe2++H2↑,完全溶出Mn2+所需Fe与MnO2的物质的量比值为2。而实际比值(0.9)小于2,原因是
(2)纯化。已知:MnO2的氧化性与溶液pH有关。纯化时先加入MnO2,后加入NH3·H2O,调溶液pH≈5,说明试剂加入顺序及调节pH的原因:
(3)电解。Mn2+纯化液经电解得MnO2。生成MnO2的电极反应式是
(4)产品纯度测定。向ag产品中依次加入足量bgNa2C2O4和足量稀H2SO4,加热至充分反应。再用cmol·L-1KMnO4溶液滴定剩余Na2C2O4至终点,消耗KMnO4溶液的体积为dL(已知:MnO2及MnO
 均被还原为Mn2+。相对分子质量:MnO2-86.94;Na2C2O4-134.0)
均被还原为Mn2+。相对分子质量:MnO2-86.94;Na2C2O4-134.0)产品纯度为
您最近一年使用:0次
2020-08-19更新
|
5643次组卷
|
12卷引用:2020年北京市高考化学试卷
2020年北京市高考化学试卷(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)2020年北京高考化学真题变式题11-19(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)专题11 无机工艺流程题—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)专题18 工艺流程题北京市第四十三中学2021届高三上学期1月月考化学试题安徽省阜阳市2020-2021学年高二下学期段考化学试题北京市第一○一中学2023-2024学年高二上学期12月统练四化学试题北京市第一○一中学2023-2024学年高二上学期12月统练四化学试题
解题方法
8 .  是石油化学工业的一种重要催化剂,其中Ag起催化作用,
是石油化学工业的一种重要催化剂,其中Ag起催化作用,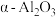 是载体且不溶于硝酸,该催化剂的回收实验如图1所示.其中的转化反应为:
是载体且不溶于硝酸,该催化剂的回收实验如图1所示.其中的转化反应为:

阅读上述实验流程,完成下列填空:
 加酸溶解应该选用装置
加酸溶解应该选用装置 图
图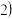
______  选填a、b、
选填a、b、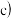 .
.
 在实验操作
在实验操作 Ⅱ
Ⅱ ,如果用自来水代替蒸馏水进行洗涤,将会发生化学反应的离子方程式
,如果用自来水代替蒸馏水进行洗涤,将会发生化学反应的离子方程式 ______ .
 实验操作
实验操作 Ⅳ
Ⅳ 所需玻璃仪器为
所需玻璃仪器为 ______  填写三种
填写三种 .
.
 实验操作
实验操作 Ⅶ
Ⅶ 从
从 溶液获得
溶液获得 晶体需要进行的实验操作依次为:
晶体需要进行的实验操作依次为: ______  多选扣分
多选扣分 .
.
 蒸馏
蒸馏 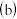 蒸发
蒸发 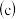 灼烧
灼烧 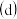 冷却结晶
冷却结晶
 已知:
已知: ;
;

NO和 的混合气体的组成可表示为
的混合气体的组成可表示为 该混合气体通入NaOH溶液被完全吸收时,x的值为
该混合气体通入NaOH溶液被完全吸收时,x的值为 ______
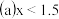
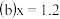

 已知
已知 中Ag的质量分数,若计算Ag的回收率,还必须知道的实验数据为
中Ag的质量分数,若计算Ag的回收率,还必须知道的实验数据为 ______ 和 ______ .
 是石油化学工业的一种重要催化剂,其中Ag起催化作用,
是石油化学工业的一种重要催化剂,其中Ag起催化作用,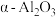 是载体且不溶于硝酸,该催化剂的回收实验如图1所示.其中的转化反应为:
是载体且不溶于硝酸,该催化剂的回收实验如图1所示.其中的转化反应为:

阅读上述实验流程,完成下列填空:
 加酸溶解应该选用装置
加酸溶解应该选用装置 图
图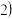
 选填a、b、
选填a、b、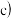 .
. 在实验操作
在实验操作 Ⅱ
Ⅱ ,如果用自来水代替蒸馏水进行洗涤,将会发生化学反应的离子方程式
,如果用自来水代替蒸馏水进行洗涤,将会发生化学反应的离子方程式  实验操作
实验操作 Ⅳ
Ⅳ 所需玻璃仪器为
所需玻璃仪器为  填写三种
填写三种 .
. 实验操作
实验操作 Ⅶ
Ⅶ 从
从 溶液获得
溶液获得 晶体需要进行的实验操作依次为:
晶体需要进行的实验操作依次为:  多选扣分
多选扣分 .
. 蒸馏
蒸馏  蒸发
蒸发  灼烧
灼烧  冷却结晶
冷却结晶  已知:
已知: ;
; 
NO和
 的混合气体的组成可表示为
的混合气体的组成可表示为 该混合气体通入NaOH溶液被完全吸收时,x的值为
该混合气体通入NaOH溶液被完全吸收时,x的值为 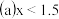

 已知
已知 中Ag的质量分数,若计算Ag的回收率,还必须知道的实验数据为
中Ag的质量分数,若计算Ag的回收率,还必须知道的实验数据为
您最近一年使用:0次
9 . 金属的回收是工业生产中的重要课题,利用某工业冶炼废渣 主要成分为
主要成分为 和铁、锡、铅、铜的氧化物
和铁、锡、铅、铜的氧化物 回收锡、铜、铅的工艺流程如图所示:
回收锡、铜、铅的工艺流程如图所示:
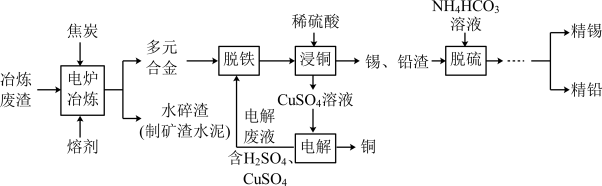
回答下列问题:
 电炉冶炼时,焦炭的作用是
电炉冶炼时,焦炭的作用是______  填“氧化剂”或“还原剂”
填“氧化剂”或“还原剂” ,将焦炭粉碎的目的是
,将焦炭粉碎的目的是______ 。熔剂的主要成分是氟石 ,高温下能与
,高温下能与 反应生成两种钙盐,其中之一为CaSiF6,该反应的化学方程式为
反应生成两种钙盐,其中之一为CaSiF6,该反应的化学方程式为______ 。
 脱铁后的溶液中含有少量的
脱铁后的溶液中含有少量的  ,为减少锡的损失,可用锡、铜、铅、铁多元合金回收处理,反应的离子方程式为
,为减少锡的损失,可用锡、铜、铅、铁多元合金回收处理,反应的离子方程式为______ 。
 已知
已知  可表示为:
可表示为: ,则
,则  也可用氧化物表示为:
也可用氧化物表示为:______ 。
 脱硫后需过滤、洗涤再进入下一步工序,检验滤渣是否洗涤干净的方法是
脱硫后需过滤、洗涤再进入下一步工序,检验滤渣是否洗涤干净的方法是______ 。
 若该冶炼废渣中锡的质量分数为
若该冶炼废渣中锡的质量分数为  ,30t 废渣制得精锡
,30t 废渣制得精锡  ,则锡的回收率为
,则锡的回收率为______ 。
 主要成分为
主要成分为 和铁、锡、铅、铜的氧化物
和铁、锡、铅、铜的氧化物 回收锡、铜、铅的工艺流程如图所示:
回收锡、铜、铅的工艺流程如图所示:
回答下列问题:
 电炉冶炼时,焦炭的作用是
电炉冶炼时,焦炭的作用是 填“氧化剂”或“还原剂”
填“氧化剂”或“还原剂” ,将焦炭粉碎的目的是
,将焦炭粉碎的目的是 ,高温下能与
,高温下能与 反应生成两种钙盐,其中之一为CaSiF6,该反应的化学方程式为
反应生成两种钙盐,其中之一为CaSiF6,该反应的化学方程式为 脱铁后的溶液中含有少量的
脱铁后的溶液中含有少量的  ,为减少锡的损失,可用锡、铜、铅、铁多元合金回收处理,反应的离子方程式为
,为减少锡的损失,可用锡、铜、铅、铁多元合金回收处理,反应的离子方程式为 已知
已知  可表示为:
可表示为: ,则
,则  也可用氧化物表示为:
也可用氧化物表示为: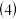 脱硫后需过滤、洗涤再进入下一步工序,检验滤渣是否洗涤干净的方法是
脱硫后需过滤、洗涤再进入下一步工序,检验滤渣是否洗涤干净的方法是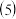 若该冶炼废渣中锡的质量分数为
若该冶炼废渣中锡的质量分数为  ,30t 废渣制得精锡
,30t 废渣制得精锡  ,则锡的回收率为
,则锡的回收率为
您最近一年使用:0次
10 . 某化学兴趣小组同学设计实验制备亚氯酸钠 并对其性质进行研究。
并对其性质进行研究。
实验Ⅰ:制取
利用如图所示装置进行实验。
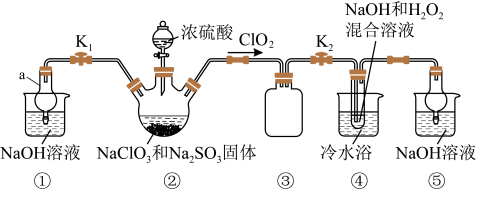
 仪器a的名称是
仪器a的名称是_______ ,其作用是_______ 。
 装置
装置 发生的反应中氧化剂和还原剂的物质的量之比为
发生的反应中氧化剂和还原剂的物质的量之比为_______ 。
 装置
装置 中制备
中制备 的离子方程式为
的离子方程式为_______ 。
 用电解
用电解 和
和 的混合溶液也可以制备
的混合溶液也可以制备 ,阴极的电极反应式为
,阴极的电极反应式为_______ 。
实验Ⅱ:研究 的性质
的性质
 利用所提供的试剂
利用所提供的试剂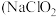 样品、
样品、 溶液、KI溶液、稀硫酸、稀硝酸
溶液、KI溶液、稀硫酸、稀硝酸 验证
验证 的氧化性,并测定
的氧化性,并测定 样品的纯度。
样品的纯度。
 准确称取所得
准确称取所得 样品5.5g于烧杯中,加入适量蒸馏水和过量的
样品5.5g于烧杯中,加入适量蒸馏水和过量的_______ ,再滴入适量的_______ ,充分反应,反应的离子方程式为_______ 。将所得混合液配成250mL待测溶液。
 移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用
移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用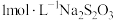 标准液滴定,至滴定终点。重复2次,测得消耗标准液的平均体积为24.00mL已知:
标准液滴定,至滴定终点。重复2次,测得消耗标准液的平均体积为24.00mL已知: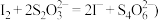 。该样品中
。该样品中 的质量分数为
的质量分数为_______ 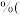 保留一位小数
保留一位小数 。
。
 并对其性质进行研究。
并对其性质进行研究。实验Ⅰ:制取

利用如图所示装置进行实验。

 仪器a的名称是
仪器a的名称是 装置
装置 发生的反应中氧化剂和还原剂的物质的量之比为
发生的反应中氧化剂和还原剂的物质的量之比为 装置
装置 中制备
中制备 的离子方程式为
的离子方程式为 用电解
用电解 和
和 的混合溶液也可以制备
的混合溶液也可以制备 ,阴极的电极反应式为
,阴极的电极反应式为实验Ⅱ:研究
 的性质
的性质 利用所提供的试剂
利用所提供的试剂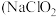 样品、
样品、 溶液、KI溶液、稀硫酸、稀硝酸
溶液、KI溶液、稀硫酸、稀硝酸 验证
验证 的氧化性,并测定
的氧化性,并测定 样品的纯度。
样品的纯度。 准确称取所得
准确称取所得 样品5.5g于烧杯中,加入适量蒸馏水和过量的
样品5.5g于烧杯中,加入适量蒸馏水和过量的 移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用
移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用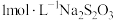 标准液滴定,至滴定终点。重复2次,测得消耗标准液的平均体积为24.00mL已知:
标准液滴定,至滴定终点。重复2次,测得消耗标准液的平均体积为24.00mL已知: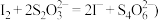 。该样品中
。该样品中 的质量分数为
的质量分数为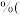 保留一位小数
保留一位小数 。
。
您最近一年使用:0次



