名校
1 . 按要求完成以下各题:
I.生活和生产中常利用到胶体的性质,根据胶体的性质,用语言表述完成以下各空。
(1)做实验时,手指不慎被玻璃划破,可从急救箱中取氯化铁应急止血,其原理是________ 。
(2)明矾能净化水的原因是___________ 。
Ⅱ.根据信息完成相应的离子反应方程式:
(3)用过量氨水吸收工业尾气中的SO2___________ 。
(4)向NH4HCO3溶液中加少量NaOH溶液___________ 。
Ⅲ.根据信息完成相应的氧化还原反应方程式:
(5)Pb与C同主族,铅元素的化合价有+2价和+4价,PbO与PbO2是铅的两种常见氧化物。已知PbO2具有强氧化性,与浓盐酸共热可生成Cl2和PbCl2。试写出Pb3O4与浓盐酸反应的化学方程式:_____ 。
(6)尖晶石型锰酸锂(LiMn2O4)是一种环保绿色能源新型材料。实验室通过下列方法制取:将MnO2和Li2CO3按4∶1的个数比配料,球磨3~5小时,然后升温至600~750℃,保温24小时,自然冷却到室温得产品,反应过程中生成两种常见气体,其中一种气体能够使澄清石灰石变浑浊,写出该反应的化学方程式:___________ 。
I.生活和生产中常利用到胶体的性质,根据胶体的性质,用语言表述完成以下各空。
(1)做实验时,手指不慎被玻璃划破,可从急救箱中取氯化铁应急止血,其原理是
(2)明矾能净化水的原因是
Ⅱ.根据信息完成相应的离子反应方程式:
(3)用过量氨水吸收工业尾气中的SO2
(4)向NH4HCO3溶液中加少量NaOH溶液
Ⅲ.根据信息完成相应的氧化还原反应方程式:
(5)Pb与C同主族,铅元素的化合价有+2价和+4价,PbO与PbO2是铅的两种常见氧化物。已知PbO2具有强氧化性,与浓盐酸共热可生成Cl2和PbCl2。试写出Pb3O4与浓盐酸反应的化学方程式:
(6)尖晶石型锰酸锂(LiMn2O4)是一种环保绿色能源新型材料。实验室通过下列方法制取:将MnO2和Li2CO3按4∶1的个数比配料,球磨3~5小时,然后升温至600~750℃,保温24小时,自然冷却到室温得产品,反应过程中生成两种常见气体,其中一种气体能够使澄清石灰石变浑浊,写出该反应的化学方程式:
您最近一年使用:0次
名校
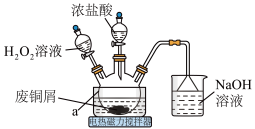
2 . CuCl2是常见的化学试剂,某小组利用废铜屑“湿法”制备CuCl2·2H2O并开展相关探究。
回答下列问题:
(1)仪器a的名称为___________ 。
(2)上述方法制备CuCl2的离子方程式为___________ 。
(3)为得到纯净的CuCl2·2H2O晶体,反应完全后要进行的操作是:除去其他可能的金属离子后,过滤,向滤液中持续通入 气体,加热蒸发浓缩,
气体,加热蒸发浓缩,___________ ,过滤,洗涤,低温干燥。持续通入 气体的目的是
气体的目的是___________ 。
(4)实验中,H2O2的实际用量要大于理论用量,可能因素为:原因1:___________ ;原因2:生成的CuCl2催化了H2O2的分解。
(5)该小组对“原因2”进行拓展探究。为验证CuCl2对H2O2分解的催化作用,该小组向5支盛有10mL5%H2O2的试管中滴加不同溶液,实验记录如下表(忽略溶液体积的微小变化;已知一定条件下,还原产物的浓度越小,氧化剂的氧化性越强):
①实验Ⅳ过程中观察到有白色沉淀(经检验为CuCl)生成,反应的机理表示为
第一步:H2O2+2Cu2++2Cl-=O2↑+2CuCl+2H+;
第二步:___________ (写离子方程式)。
②已知化学反应速率第一步<第二步,则气泡产生速率实验Ⅳ比实验Ⅲ加快的原因:___________ 。
③分析上述实验,下列说法正确的是___________ (填字母)。
A.实验Ⅰ的目的是证明仅有NaCl对H2O2分解没有催化作用
B. 对H2O2分解有显著催化作用
对H2O2分解有显著催化作用
C.Cl-增强了Cu2+对H2O2分解的催化效果,且Cl-浓度越大催化效果越强
④写出一种H2O2的用途___________ 。
| 温度 | 15℃以下 | 15~25.7℃ | 26~42℃ | 42℃以上 |
| 结晶水合物 | CuCl2·4H2O | CuCl2·3H2O | CuCl2·2H2O | CuCl2·H2O |
(1)仪器a的名称为
(2)上述方法制备CuCl2的离子方程式为
(3)为得到纯净的CuCl2·2H2O晶体,反应完全后要进行的操作是:除去其他可能的金属离子后,过滤,向滤液中持续通入
 气体,加热蒸发浓缩,
气体,加热蒸发浓缩, 气体的目的是
气体的目的是(4)实验中,H2O2的实际用量要大于理论用量,可能因素为:原因1:
(5)该小组对“原因2”进行拓展探究。为验证CuCl2对H2O2分解的催化作用,该小组向5支盛有10mL5%H2O2的试管中滴加不同溶液,实验记录如下表(忽略溶液体积的微小变化;已知一定条件下,还原产物的浓度越小,氧化剂的氧化性越强):
| 实验 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ |
| 滴加试剂 | 2滴1mol/LNaCl | 2滴1mol/LNa2SO4 | 2滴1mol/LCuSO4 | 2滴1mol/LCuSO4和2滴1mol/LNaCl | 2滴1mol/LCuSO4和4滴1mol/LNaCl |
| 现象 | 无气泡产生 | 无气泡产生 | 均产生气泡,且气泡速率从Ⅲ到Ⅴ依次加快 | ||
第一步:H2O2+2Cu2++2Cl-=O2↑+2CuCl+2H+;
第二步:
②已知化学反应速率第一步<第二步,则气泡产生速率实验Ⅳ比实验Ⅲ加快的原因:
③分析上述实验,下列说法正确的是
A.实验Ⅰ的目的是证明仅有NaCl对H2O2分解没有催化作用
B.
 对H2O2分解有显著催化作用
对H2O2分解有显著催化作用C.Cl-增强了Cu2+对H2O2分解的催化效果,且Cl-浓度越大催化效果越强
④写出一种H2O2的用途
您最近一年使用:0次
名校
3 . 回答下列问题:
(1)关于甲、乙、丙、丁四套装置的说法正确的是_______ 。

(2)以下物质(或粒子)与其用途之间关联正确的是_______ 。
(3)实验室制取Cl2的化学方程式:_______ 。浓盐酸表现的性质是_______ 。
(4)已知:在稀硫酸中,MnO 与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。_______
(1)关于甲、乙、丙、丁四套装置的说法正确的是

| A.用装置甲制取氯气 | B.用丙装置可以较长时间看到白色Fe(OH)2白色沉淀 |
| C.用丁装置证明碳酸氢钠受热易分解 | D.用装置乙除去氢气中的少量氯化氢 |
| A.硬铝——制导线 | B.14C——测定文物年代 |
| C.锗——作半导体材料 | D.Ti-Fe合金——作不锈钢材料 |
(4)已知:在稀硫酸中,MnO
 与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
您最近一年使用:0次
2023-09-24更新
|
325次组卷
|
4卷引用:天津市宁河区芦台第一中学2022-2023学年高一上学期期末考试化学试题
天津市宁河区芦台第一中学2022-2023学年高一上学期期末考试化学试题(已下线)专题07 铁及其化合物 金属材料-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(天津专用)(已下线)专项02 氧化还原反应的概念、规律及综合应用-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(天津专用)山西运城盐湖五中2023-2024学年高一上学期化学期末练兵卷(三)
名校
4 . 海水提溴过程中溴元素的变化如下图所示:
(2)过程II中,用热空气将溴赶出,再用浓 (aq)吸收。将该过程中反应的化学方程式补充完整,并用单线桥标出电子转移的方向和数目。
(aq)吸收。将该过程中反应的化学方程式补充完整,并用单线桥标出电子转移的方向和数目。___________

向盛有KI(aq)的试管中加入少许 后滴加氯水,振荡、静置后,
后滴加氯水,振荡、静置后, 层变成紫色,如果继续向试管中滴加氯水,振荡,
层变成紫色,如果继续向试管中滴加氯水,振荡, 层会逐渐变浅,最后变成无色。
层会逐渐变浅,最后变成无色。
(3)写出 层由紫色变成无色(生成
层由紫色变成无色(生成 )的化学方程式:
)的化学方程式:___________ 。
(4)整个过程两步反应的还原剂分别是:第一步___________ 、第二步___________ 。
(5)把KI换成KBr,则 层变为
层变为___________ 色,继续滴加氯水, 层的颜色没有变化。向用硫酸酸化的NaI(aq)中逐滴加入
层的颜色没有变化。向用硫酸酸化的NaI(aq)中逐滴加入 (aq),当加入2.6mol
(aq),当加入2.6mol  时,测得反应后溶液中溴和碘的存在形式及物质的量(n)如下表。则原溶液中NaI的物质的量是
时,测得反应后溶液中溴和碘的存在形式及物质的量(n)如下表。则原溶液中NaI的物质的量是___________ mol。
 、
、 、
、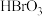 氧化性由强到弱的顺序合理的是
氧化性由强到弱的顺序合理的是___________ 。
A.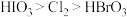 B.
B.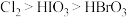
C. D.
D.

A. | B.HCl | C. | D. |
(2)过程II中,用热空气将溴赶出,再用浓
 (aq)吸收。将该过程中反应的化学方程式补充完整,并用单线桥标出电子转移的方向和数目。
(aq)吸收。将该过程中反应的化学方程式补充完整,并用单线桥标出电子转移的方向和数目。
向盛有KI(aq)的试管中加入少许
 后滴加氯水,振荡、静置后,
后滴加氯水,振荡、静置后, 层变成紫色,如果继续向试管中滴加氯水,振荡,
层变成紫色,如果继续向试管中滴加氯水,振荡, 层会逐渐变浅,最后变成无色。
层会逐渐变浅,最后变成无色。(3)写出
 层由紫色变成无色(生成
层由紫色变成无色(生成 )的化学方程式:
)的化学方程式:(4)整个过程两步反应的还原剂分别是:第一步
(5)把KI换成KBr,则
 层变为
层变为 层的颜色没有变化。向用硫酸酸化的NaI(aq)中逐滴加入
层的颜色没有变化。向用硫酸酸化的NaI(aq)中逐滴加入 (aq),当加入2.6mol
(aq),当加入2.6mol  时,测得反应后溶液中溴和碘的存在形式及物质的量(n)如下表。则原溶液中NaI的物质的量是
时,测得反应后溶液中溴和碘的存在形式及物质的量(n)如下表。则原溶液中NaI的物质的量是| 粒子 |  |  | 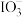 |
| n/mol | 0.5 | 1.3 | 未知 |
 、
、 、
、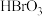 氧化性由强到弱的顺序合理的是
氧化性由强到弱的顺序合理的是A.
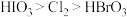 B.
B.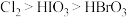
C.
 D.
D.
您最近一年使用:0次
2024-01-21更新
|
209次组卷
|
2卷引用:上海市南洋模范中学2023-2024学年高一上学期期末考试化学试卷
5 . 化学材料在生产、生活中应用广泛。下列有关说法错误的是
| A.还原铁粉可用作食品包装袋内的脱氧剂 |
B.用 对自来水进行消毒,改善水质 对自来水进行消毒,改善水质 |
| C.维生素C常用作抗氧化剂,说明它具有氧化性 |
| D.“雨后彩虹”“海市蜃楼”既是光学现象,也与胶体的知识有关 |
您最近一年使用:0次
名校
6 . 已知:① ,②
,②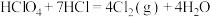 。
。 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 ,②
,②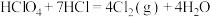 。
。 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.反应①中物质的氧化性: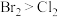 |
B.标准状况下,11.2L 参与反应时转移的电子数为5NA 参与反应时转移的电子数为5NA |
C.1L0.5  溶液含有的 溶液含有的 分子数为0.5 分子数为0.5 |
D.反应②生成28.4g 时,还原产物分子数为0.05 时,还原产物分子数为0.05 |
您最近一年使用:0次
2024-04-16更新
|
705次组卷
|
5卷引用:辽宁省锦州市渤海大学附属高级中学2023-2024学年高三下学期3月摸底考试化学试题
辽宁省锦州市渤海大学附属高级中学2023-2024学年高三下学期3月摸底考试化学试题河北省邢台市五岳联盟2024届高三下学期模拟预测化学试题贵州省安顺市部分学校2024届高三下学期二模考试化学试题(已下线)通关练01 化学基本概念再回归-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)选择题1-5
名校
解题方法
7 . 中药材铁华粉的主要成分为醋酸亚铁,可用如图所示方法检测。下列相关说法不正确的是
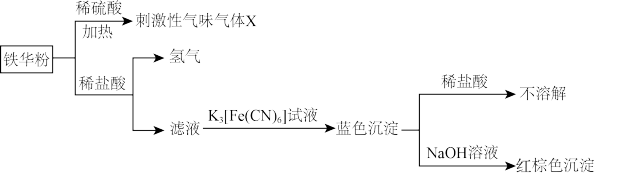
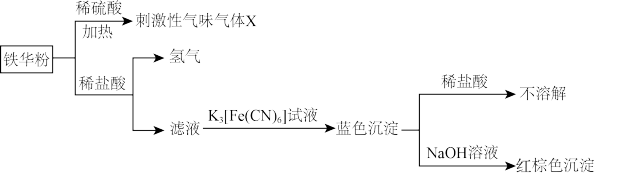
A.制备铁华粉的主要反应为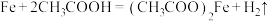 |
| B.气体X中含有醋酸蒸气 |
C.向滤液中滴加酸性高锰酸钾溶液,可证明 具有还原性 具有还原性 |
D.由上述实验可知, 结合 结合 的能力大于 的能力大于 |
您最近一年使用:0次
2022-11-11更新
|
1380次组卷
|
8卷引用:安徽省安庆市第二中学2022-2023学年高三上学期11月月考化学试题
安徽省安庆市第二中学2022-2023学年高三上学期11月月考化学试题 安徽省阜阳市江淮十校2022-2023学年高三上学期第二次联考化学试题(已下线)化学(湖南A卷)-学易金卷:2023年高考化学第一次模拟考试卷(已下线)化学(山东A卷)-学易金卷:2023年高考第一次模拟考试卷(已下线)专题14 工艺流程选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)湖南省长沙市明达中学2022-2023学年高三下学期2月月考化学试题山东省实验中学2022-2023学年高三下学期开学考试化学试题 (已下线)回归教材重难点04 “9种”物质的性质及应用-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)
8 . “实践出真知”,下列对劳动实践的化学解读错误的是
| 选项 | 劳动实践 | 化学解读 |
| A | 给苹果树喷洒波尔多液 |  为重金属离子,可使蛋白质变性 为重金属离子,可使蛋白质变性 |
| B | 给农田施用碳铵肥料时应及时掩埋 | 碳铵易分解 |
| C | 用醋酸除水壶中的水垢 | 水垢与醋酸发生了氧化还原反应 |
| D | 用臭氧消毒柜给碗筷消毒 | 臭氧具有强氧化性,可杀菌消毒 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 化学和生活、社会发展息息相关。下列说法正确的组合是
①飞船返回舱表层材料中的玻璃纤维属于天然有机高分子材料
②液化石油气、汽油、煤油、柴油的主要成分都是烃
③工业上通过石油分馏得到大量化工原料苯
④活性炭疏松多孔,可用于除异味和杀菌
⑤维生素C是NaNO2中毒的急救药之一,利用了维生素C的氧化性
⑥“光化学烟雾”“臭氧空洞”“硝酸型酸雨”的形成都与氮氧化物有关
⑦用四氯乙烯干洗剂除去衣服上油污,发生的是物理变化
⑧波尔多液(硫酸铜、石灰和水配成)用作农药,利用Cu2+使病毒蛋白变性
⑨漂白粉与盐酸可混合使用以提高漂白效果
①飞船返回舱表层材料中的玻璃纤维属于天然有机高分子材料
②液化石油气、汽油、煤油、柴油的主要成分都是烃
③工业上通过石油分馏得到大量化工原料苯
④活性炭疏松多孔,可用于除异味和杀菌
⑤维生素C是NaNO2中毒的急救药之一,利用了维生素C的氧化性
⑥“光化学烟雾”“臭氧空洞”“硝酸型酸雨”的形成都与氮氧化物有关
⑦用四氯乙烯干洗剂除去衣服上油污,发生的是物理变化
⑧波尔多液(硫酸铜、石灰和水配成)用作农药,利用Cu2+使病毒蛋白变性
⑨漂白粉与盐酸可混合使用以提高漂白效果
| A.②⑤⑦⑨ | B.②⑥⑦⑧ | C.③④⑥⑧ | D.①③④⑤ |
您最近一年使用:0次
2023-09-10更新
|
260次组卷
|
2卷引用:辽宁省沈阳市第二十中学2023-2024学年高三上学期一模考试化学试题
名校
10 . 《南村辍耕录》中记载:“杭人削松木为小片,其薄如纸,熔硫磺涂木片顶分许,名曰发烛”。文中的“发烛”就是原始的火柴。K2Cr2O7在工业中用作制造火柴头的氧化剂。
已知:K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O
(1)___________ (填化学式)是氧化剂,___________ (填元素名称)元素被氧化。
(2)在参加反应的HCl中,起还原剂作用的HCl与起酸的作用的HCl的质量比为___________ 。
(3)该反应中每生成1个KCl转移电子个数为___________ 。
(4)+6价铬的毒性很强,具有一定的致癌作用,需要转化为低毒的Cr3+,再除去,废水中含有的Cr2O 可以用绿矾(FeSO4·7H2O)除去。测得反应后的溶液中含Cr3+、Fe2+、Fe3+、H+等阳离子。写出该反应的离子方程式:
可以用绿矾(FeSO4·7H2O)除去。测得反应后的溶液中含Cr3+、Fe2+、Fe3+、H+等阳离子。写出该反应的离子方程式:___________ 。
(5)已知:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O;KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。K2Cr2O7、MnO2、KClO3三种物质氧化性由大到小的顺序为
MnCl2+Cl2↑+2H2O;KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。K2Cr2O7、MnO2、KClO3三种物质氧化性由大到小的顺序为___________ 。
已知:K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O
(1)
(2)在参加反应的HCl中,起还原剂作用的HCl与起酸的作用的HCl的质量比为
(3)该反应中每生成1个KCl转移电子个数为
(4)+6价铬的毒性很强,具有一定的致癌作用,需要转化为低毒的Cr3+,再除去,废水中含有的Cr2O
 可以用绿矾(FeSO4·7H2O)除去。测得反应后的溶液中含Cr3+、Fe2+、Fe3+、H+等阳离子。写出该反应的离子方程式:
可以用绿矾(FeSO4·7H2O)除去。测得反应后的溶液中含Cr3+、Fe2+、Fe3+、H+等阳离子。写出该反应的离子方程式:(5)已知:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O;KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。K2Cr2O7、MnO2、KClO3三种物质氧化性由大到小的顺序为
MnCl2+Cl2↑+2H2O;KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。K2Cr2O7、MnO2、KClO3三种物质氧化性由大到小的顺序为
您最近一年使用:0次



